Clear Sky Science · it
Diazotizzazione diretta degli indoli con nitrito di 2-metossipropile
Trasformare un gas problematico in chimica utile
L'ossido nitrico è spesso considerato un gas industriale problematico: è tossico, difficile da gestire e di solito trattato come rifiuto. Eppure è anche ricco di azoto, un elemento chiave in molti medicinali. Questo studio mostra come i chimici possano domare l'ossido nitrico convertendolo in un reagente liquido stabile che, a sua volta, aiuta a costruire molecole complesse rilevanti per candidati farmaceutici. Il lavoro offre un modo per trasformare un sottoprodotto pericoloso in uno strumento per ottenere composti di valore in modo più sicuro e pulito.
Un nuovo composto aiuto per reazioni difficili
I chimici fanno spesso affidamento su composti “diazo” — molecole che portano una coppia di atomi di azoto molto reattiva — per costruire scheletri di carbonio intricati. Questi scheletri sono presenti in molti farmaci, in particolare quelli basati sugli indoli, un sistema ad anello comune nei prodotti naturali e nei farmaci. I metodi tradizionali per ottenere composti diazo utilizzano spesso azidi esplosivi o grandi quantità di acidi e basi forti, creando problemi di sicurezza e ambientali. Gli autori si concentrano su un’alternativa più sicura: un liquido chiamato nitrito di 2-metossietile, o MOE-ONO, che può essere ottenuto direttamente dal gas di ossido nitrico, dall'ossigeno e da un alcol semplice, generando come unico sottoprodotto acqua.
Rielaborare direttamente un anello importante per i farmaci
Il team ha cercato di introdurre gruppi diazo direttamente sugli indoli, modificandoli in una posizione precisa sull'anello senza condizioni aggressive. Hanno scoperto che la combinazione di MOE-ONO con un comune radicale organico, TEMPO, e una piccola quantità di un sale metallico catalizzatore a base di scandio innesca questa trasformazione in modo efficiente. Rispetto alle miscele classiche di nitrito di sodio e acido, o ad altri donatori liquidi di ossido nitrico come il nitrito di tert-butile, la nuova combinazione fornisce rese più elevate, molti meno prodotti indesiderati e opera in tempi molto più brevi. Anche indoli che avevano resistito ai metodi più vecchi — come quelli con gruppi fenilici ingombranti — potevano essere convertiti in modo pulito con questo approccio.
Un metodo, molti mattoni di costruzione
Dopo aver ottimizzato la reazione, i ricercatori hanno testato l'ampiezza della sua applicabilità. Hanno scoperto che una vasta gamma di derivati dell'indolo tollera le condizioni, inclusi quelli contenenti esteri, chetoni, ammidi e diversi sostituenti sull'anello, da gruppi alchilici e metossili ricchi di elettroni fino ad alogeni e gruppi ciano. Il metodo si è esteso anche oltre gli indoli a composti correlati come i naftoli, formando derivati diazo che in precedenza richiedevano procedure più lunghe e a più step. È degno di nota che la reazione funzionasse anche eseguita in acqua, nonostante i reagenti di partenza non siano molto solubili in essa. Questo comportamento cosiddetto “on-water” suggerisce che semplicemente agitare la miscela in acqua fornisce un mezzo più ecologico che aiuta la reazione a procedere riducendo la dipendenza da solventi organici.
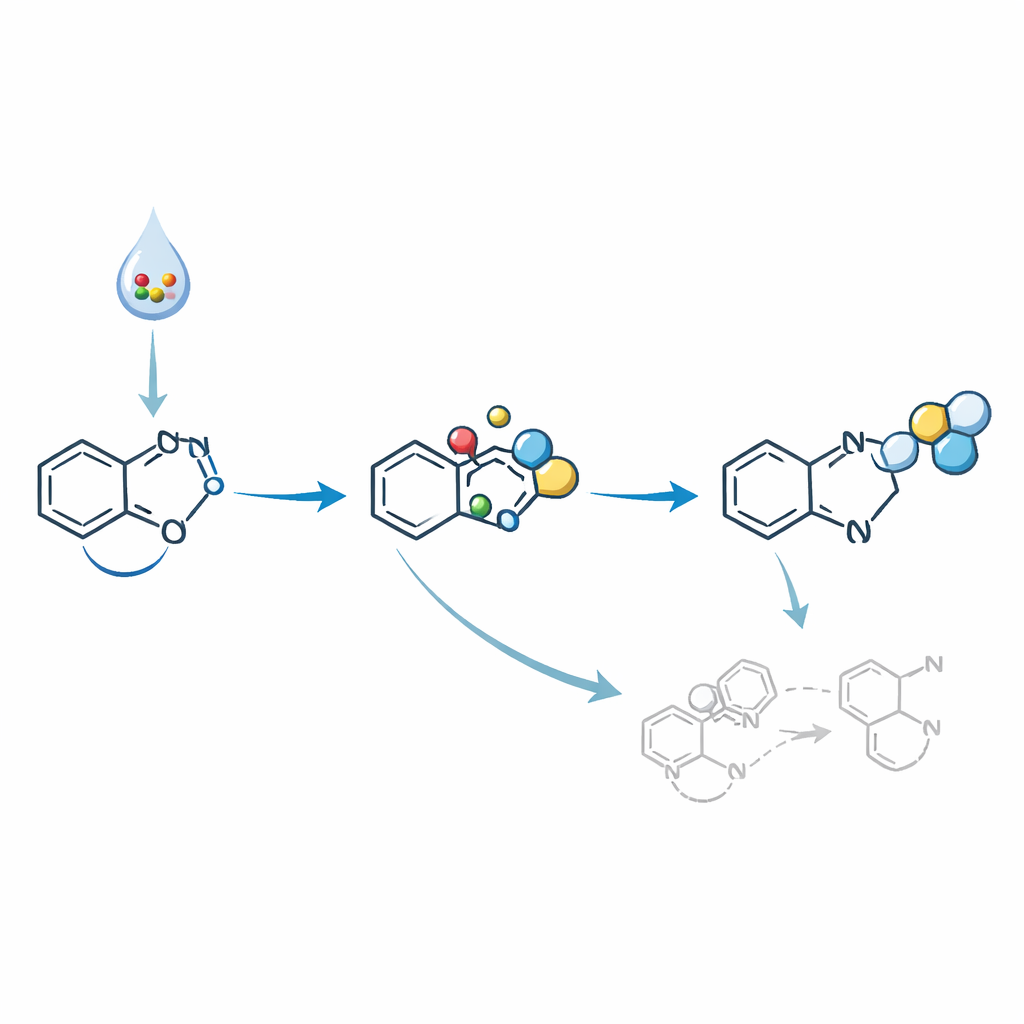
Dagli intermedi reattivi ai candidati farmaceutici
Per dimostrare il valore di questi diazoindoli, gli autori li hanno trasformati ulteriormente in molecole più elaborate. Usando un catalizzatore al rodio, hanno convertito il gruppo diazo in un intermedio altamente reattivo chiamato carbene, che poi ha formato nuovi legami per costruire anelli ciclopropanici in posizioni specifiche sull'indolo. In un'altra sequenza, hanno assemblato un candidato modulatore per un recettore coinvolto nel controllo della glicemia, dimostrando la rilevanza del metodo per la chimica medicinale. Hanno anche mostrato che i reattivi di Grignard — strumenti classici per l'aggiunta di carbonio — possono attaccarsi selettivamente in una posizione sull diazoindolo lasciando intatto il gruppo diazo, aprendo la strada alla costruzione stepwise di strutture indoliche e indoliniche densamente sostituite.
Come la reazione rimane sulla strada giusta
Dietro le quinte, diversi percorsi concorrenti potrebbero portare a prodotti indesiderati come nitro o ossimi invece dei diazo desiderati. Esperimenti meccanicistici suggeriscono che il TEMPO aiuta a indirizzare la chimica intrappolando radicali dannosi e catturando un effimero intermedio nitroso prima che possa riarrangiarsi. Ulteriori molecole di ossido nitrico poi si aggiungono in sequenza, producendo infine il gruppo diazo e rilasciando nitrato innocuo. Il sale di scandio sembra favorire la scissione di MOE-ONO in specie reattive e attivare il nucleo indolico, migliorando ulteriormente l'efficienza. Il rilevamento del nitrato nella miscela finale supporta questa via proposta dal donatore di ossido nitrico al prodotto diazo.
Una via sicura e sostenibile verso molecole complesse
Complessivamente, questo lavoro introduce un modo pratico per installare gruppi diazo altamente utili sugli anelli indolici senza fare affidamento su reagenti esplosivi o condizioni aggressive. Usando un liquido stabile derivato dal gas di ossido nitrico, il metodo sia “upcycle” di una emissione industriale problematica sia semplifica l'accesso a molecole complesse e con caratteristiche da farmaco. Per i non specialisti, il messaggio chiave è che una chimica intelligente può trasformare un gas di scarto tossico in un blocco di costruzione versatile per i futuri medicinali, riducendo al contempo l'impatto ambientale lungo il processo.
Citazione: Hashidoko, A., Kitanosono, T., Nakao, Y. et al. Direct diazotization of indoles with 2-Methoxyethyl nitrite. Commun Chem 9, 104 (2026). https://doi.org/10.1038/s42004-026-01910-1
Parole chiave: riutilizzo dell'ossido nitrico, diazoindoli, sintesi organica sostenibile, farmaci a base di indolo, reagenti donatori di NO