Clear Sky Science · it
Consumo di campione ridotto per cristallografia seriale risolta nel tempo applicata al ciclo redox della NQO1 umana
Osservare gli enzimi in azione con meno campione prezioso
La biologia moderna si affida spesso a potenti laser a raggi X per vedere come le molecole della vita si muovono e cambiano forma, ma questi esperimenti consumano normalmente grandi quantità di proteine preparate con cura. Questo studio introduce un nuovo modo di "nutrire" minuscoli cristalli proteici in un laser a elettrone libero a raggi X in modo molto più efficiente, riducendo il materiale necessario fino al 97%. Dimostra anche che questo approccio più parsimonioso può comunque catturare i primi passaggi dell’attività di un enzima umano di rilevanza medica, aprendo la strada a filmati più routinari delle proteine al lavoro. 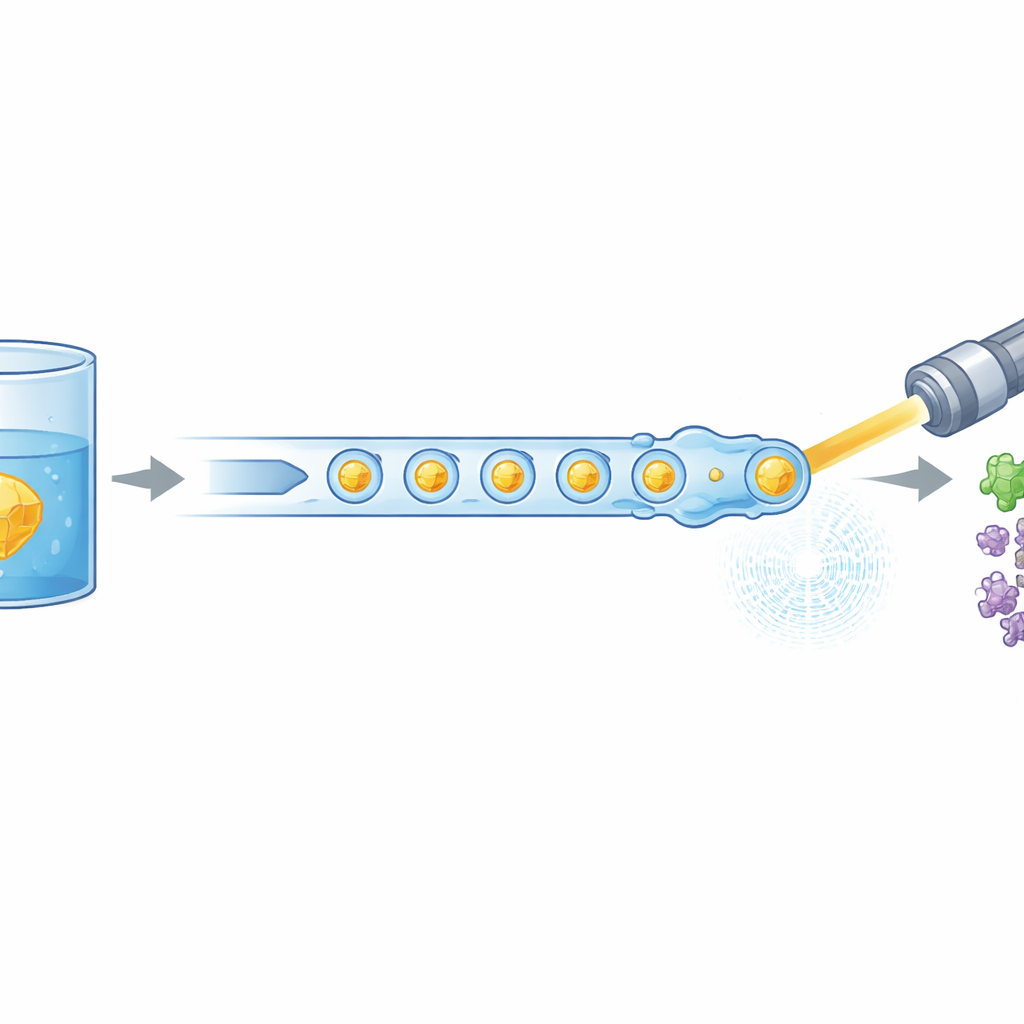
Perché girare filmati molecolari è così costoso
Per capire come le proteine svolgono realmente le loro funzioni, i ricercatori si rivolgono sempre più spesso a "filmati" a intervalli temporali che seguono le reazioni in tempo reale invece di immagini fisse. Un approccio di punta, la cristallografia seriale risolta nel tempo, spruzza milioni di microscopici cristalli di una proteina attraverso un fascio di raggi X ultra-luminoso. Ogni cristallo viene colpito una sola volta, fornendo una visione priva di danno della struttura, e migliaia di tali immagini vengono combinate per ottenere un quadro completo. Il problema è che ogni istante di una reazione — decimi di secondo, un secondo intero e così via — richiede un nuovo lotto di cristalli. Poiché la preparazione delle proteine può essere lenta e costosa, il consumo di campione è diventato un collo di bottiglia importante, specialmente in strutture d’avanguardia come l’European XFEL, dove gli impulsi di raggi X arrivano in treni rapidi a frequenze megahertz.
Un nuovo modo per consegnare minuscole gocce su richiesta
I ricercatori hanno affrontato questo problema riprogettando la modalità di consegna dei cristalli al fascio di raggi X. Invece di un flusso continuo di liquido, generano un treno accuratamente spaziato di microscopiche gocce, ciascuna contenente cristalli proteici, separate da una fase di olio. Un piccolo dispositivo stampato in 3D combina due flussi — cristalli di proteina e un partner di reazione dissolto — in minuscoli volumi miscelati, che vengono poi staccati in gocce. Queste gocce sono indirizzate attraverso un ugello a focalizzazione di gas che forma un getto stretto compatibile con il vuoto e la velocità dell’XFEL. In modo cruciale, la produzione delle gocce è sincronizzata elettricamente con il timing dei treni di impulsi a raggi X in modo che quasi ogni impulso utile colpisca una goccia, anziché liquido vuoto. 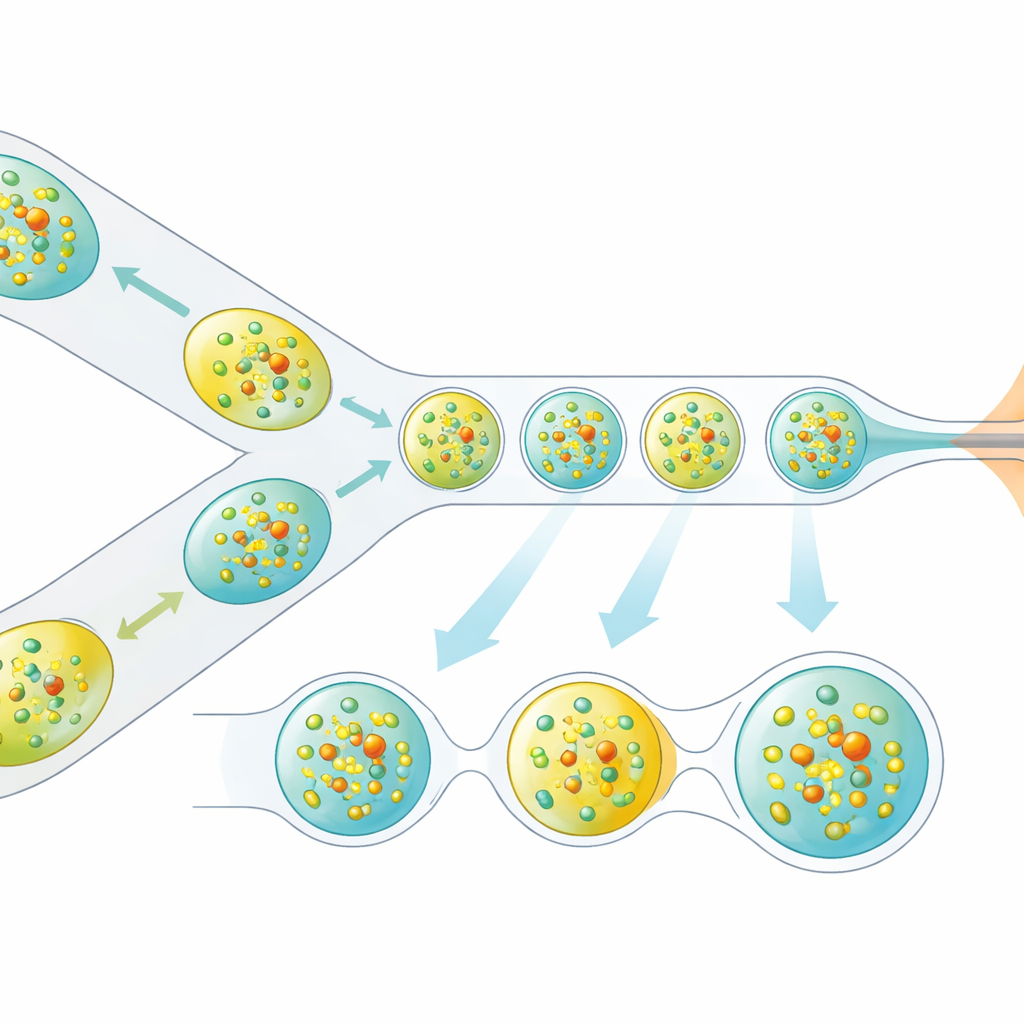
Mettere alla prova il metodo con un enzima umano
Per dimostrare che questo approccio a gocce funziona per domande biologiche reali, il team ha studiato la NAD(P)H:chinone ossidoreduttasi 1 (NQO1), un enzima umano coinvolto nella gestione dell’equilibrio redox cellulare e collegato a malattie. Hanno miscelato microcristalli di NQO1 con il suo cofattore naturale, NADH, e sondato il sistema a due tempi iniziali: 0,3 secondi e 1,2 secondi dopo la miscelazione. Esaminando i modelli di diffrazione a raggi X risultanti, hanno ricostruito strutture tridimensionali dell’enzima per ciascun ritardo. Nonostante l’uso di quantità di proteina drasticamente inferiori rispetto agli esperimenti convenzionali a flusso continuo, la qualità dei dati è stata sufficiente a rivelare sottili caratteristiche di densità elettronica nei siti attivi dell’enzima, coerenti con molecole di NADH che iniziano a legarsi a bassa occupazione.
Cosa rivelano gli istantanei strutturali precoci
Le strutture mostrano che subito dopo la miscelazione non tutti i siti attivi nel cristallo si comportano allo stesso modo. A 0,3 secondi, i segnali di NADH appaiono chiaramente in tre dei quattro siti attivi nella cella unitaria, e spesso in più di una conformazione, suggerendo che il cofattore esplora diverse posizioni prima di stabilizzarsi. A 1,2 secondi, alcune di queste caratteristiche si definiscono in una modalità di legame dominante, ma il quadro generale rimane quello di un’interazione flessibile e solo parzialmente occupata. Questo comportamento irregolare e mutevole è in linea con precedenti evidenze biochimiche secondo cui le due unità partner di un dimer di NQO1 non agiscono in perfetta sincronia, ma mostrano invece un’attività "metà dei siti", dove un lato del paio si impegna per primo mentre l’altro resta indietro. I dati risolti nel tempo offrono quindi un primo scorcio strutturale di come questa asimmetria si manifesti nello spazio reale.
Risparmiare campione mantenendo la scienza
Dal punto di vista pratico, il metodo a gocce segmentate ha ridotto l’uso di proteina di circa sei volte per le misurazioni a 0,3 secondi e fino al 97% per gli esperimenti a 1,2 secondi, rispetto ai getti continui tradizionali in condizioni simili. Eppure ha fornito informazioni strutturali affidabili a temperatura ambiente, compatibili con l’esigente struttura di impulsi dell’European XFEL. Per i non specialisti, la conclusione è che i ricercatori possono ora osservare enzimi come la NQO1 mentre iniziano il loro lavoro in quasi tempo reale, utilizzando solo milligrammi di campione prezioso per punto temporale. Questo rende molto più realistico esplorare molti tempi di reazione e molte proteine diverse, contribuendo infine a rivelare come gli enzimi di importanza medica si muovono, si flettono e cooperano mentre svolgono la chimica della vita.
Citazione: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Parole chiave: cristallografia seriale, laser a elettrone libero a raggi X, microfluidica a gocce, dinamica degli enzimi, NQO1