Clear Sky Science · it
Varianti oncogeniche di PI3Kα rivelano uno spettro conformazionale graduato con tasche criptiche specifiche per mutazione
Quando una singola modifica del DNA non basta
Il cancro è spesso descritto come una malattia delle mutazioni, ma questo studio mostra che non tutte le mutazioni agiscono da sole. I ricercatori hanno esaminato un enzima chiave nel controllo della crescita, PI3Kα, e hanno scoperto che quando due specifiche modifiche del DNA si verificano insieme nella stessa copia del gene, possono spingere questa proteina verso conformazioni più attive rispetto a ciascuna delle due mutazioni singolarmente. Questo è importante perché la PI3Kα iperattiva non solo promuove i tumori, ma è coinvolta anche in sindromi da iperaccrescimento benigno e in disturbi dello sviluppo cerebrale — e aiuta a spiegare perché alcuni tumori rispondono male ai farmaci attuali.
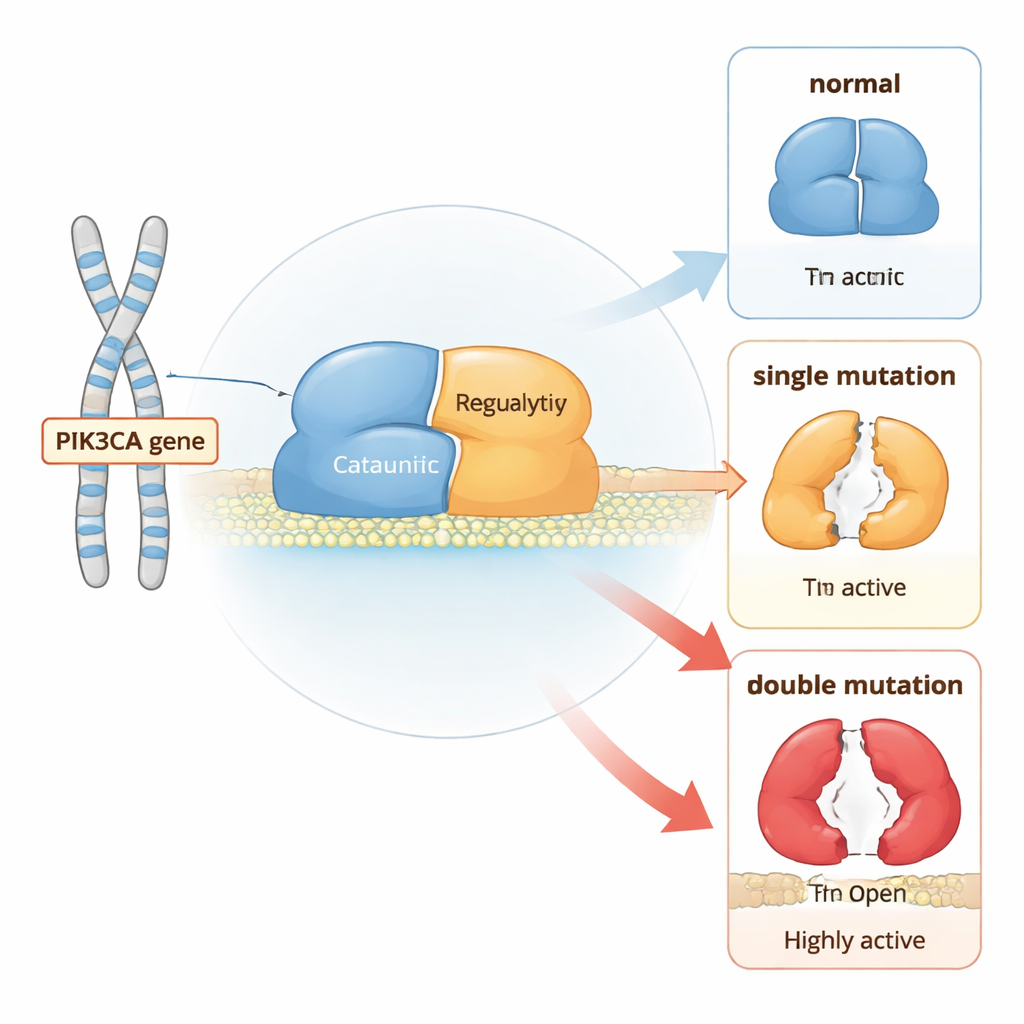
Un interruttore molecolare per la crescita cellulare
PI3Kα è una proteina composta da due parti che si trova vicino alla membrana cellulare e trasmette segnali di crescita. In condizioni normali rimane per lo più in una posizione “spenta” finché i recettori sulla superficie cellulare non vengono stimolati. A quel punto PI3Kα si sposta verso la membrana e converte un lipide chiamato PIP2 in PIP3, che manda il segnale alla cellula di crescere e dividersi. Per evitare una crescita incontrollata, diverse regioni della proteina funzionano come freni incorporati: una zona blocca il nucleo catalitico, un’altra tiene vicino un anello di attivazione flessibile e una subunità partner contribuisce a mantenere l’intero complesso sotto controllo.
Come mutazioni singole e doppie inclinano l’equilibrio
Utilizzando lunghe simulazioni al livello atomico, gli autori hanno confrontato la PI3Kα normale con versioni portatrici di singole mutazioni “hotspot” o di combinazioni formate da uno hotspot e una mutazione più debole nella stessa molecola. Hanno scoperto che ogni mutazione cambia la frequenza con cui la proteina visita conformazioni più aperte e attive, ma i doppi mutanti spostano l’equilibrio molto oltre rispetto ai singoli. In particolare, alcune coppie di mutazioni cooperano allentando i contatti che tengono in posizione un elemento regolatorio (chiamato nSH2) e spostando un altro segmento (iSH2) lontano dal suo sito di ancoraggio. Questo movimento coordinato scardina il nucleo catalitico, rendendo più facile per la proteina spostarsi verso la membrana e iniziare la segnalazione.
Aiutare il substrato a raggiungere il sito di reazione
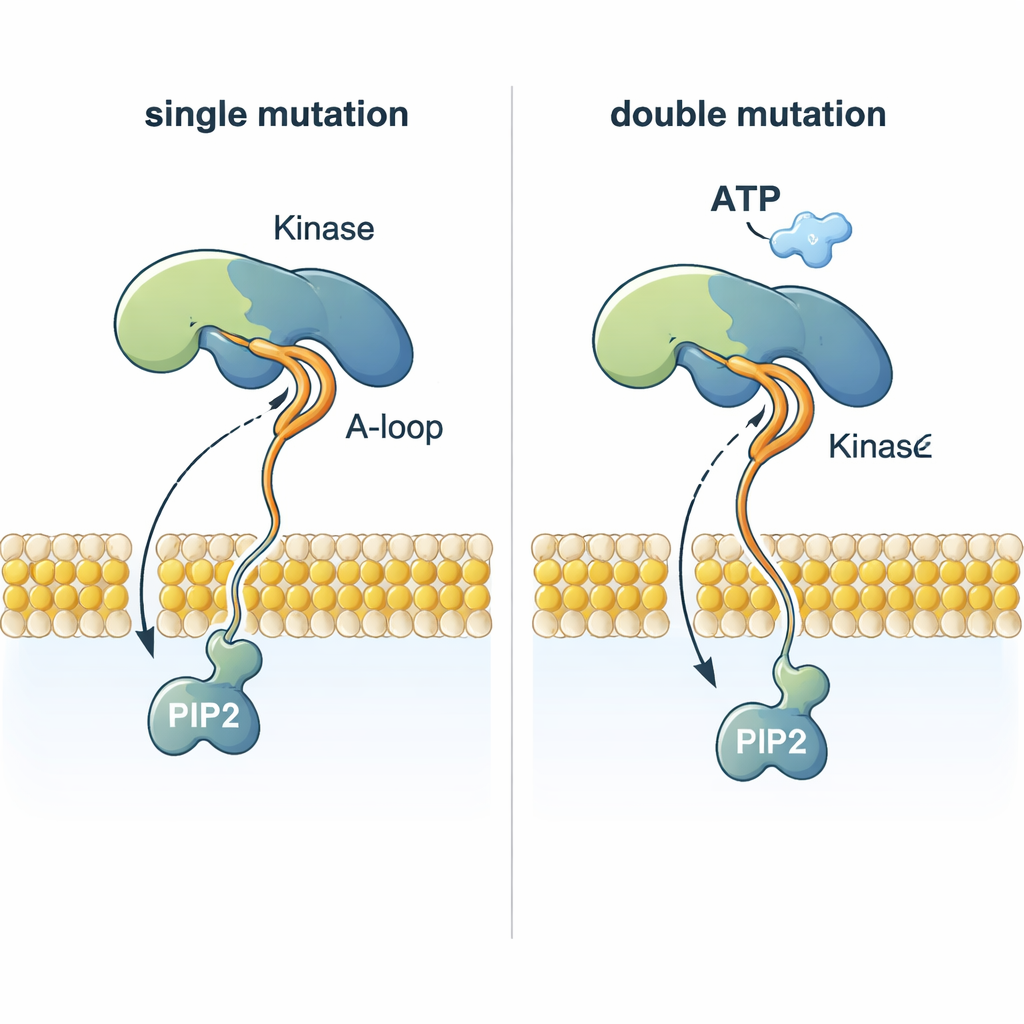
Un enigma sorprendente è come PI3Kα possa trasferire un gruppo fosfato dall’ATP — che si trova quasi 2 nanometri sopra la membrana — al PIP2, che è inserito nella membrana stessa. Le simulazioni mostrano che certe mutazioni rimodellano un anello di attivazione flessibile in modo che una porzione altamente caricata positivamente si protenda verso la membrana. Questo anello può afferrare la testa negativamente caricata del PIP2, estrarla dal doppio strato lipidico e guidarla verso l’ATP. I doppi mutanti che combinano una mutazione che ancora alla membrana con una che modifica questo anello coordinano il PIP2 molto più efficacemente rispetto alla PI3Kα normale o ai singoli mutanti, offrendo una spiegazione strutturale del perché i tumori con due mutazioni di PI3Kα possano essere particolarmente aggressivi.
Siti farmacologici nascosti rivelati dal movimento
Poiché PI3Kα è grande e flessibile, un singolo farmaco mirato al sito attivo spesso fatica a funzionare su tutte le forme mutanti e può causare effetti collaterali come gravi alterazioni della glicemia. Tracciando come la proteina “respira” e si flette nel tempo, i ricercatori hanno scoperto tasche “criptiche” — solchi temporanei che si aprono solo in particolari conformazioni mutanti e sono invisibili alle strutture cristallografiche statiche. Queste tasche emergono in posizioni specifiche per mutazione, per esempio vicino a regioni che si muovono maggiormente in certi doppi mutanti. Ciò suggerisce che farmaci allosterici disegnati con cura, che si legano lontano dal sito attivo, potrebbero essere tarati per bloccare varianti mutanti individuali in conformazioni più sicure e meno attive.
Verso terapie combinate più intelligenti
Nel complesso, il lavoro supporta una visione a “colpo doppio” della genetica del cancro: una mutazione hotspot forte più una compagna più debole nella stessa molecola di PI3Kα possono creare uno spettro graduato di conformazioni più attive, spesso associate a esiti clinici più gravi. Per la terapia, gli autori sostengono che invece di fare affidamento su un singolo inibitore potrebbe essere più efficace combinare farmaci che prendono di mira tasche diverse — una al sito attivo e una o più siti allosterici che esistono solo in specifici mutanti. Tali cocktail potrebbero, in teoria, ridurre l’attività di PI3Kα in modo più preciso, diminuire la tossicità e adattare meglio il trattamento al profilo di mutazioni esatto presente nel tumore di un paziente.
Citazione: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Parole chiave: PI3K alpha, mutazioni oncogeniche, inibitori allosterici, dinamica molecolare, trasduzione del segnale