Clear Sky Science · it
Dinamicità dipendente dalla sequenza e dalla scala di lunghezza nei biocondensati di proteine disordinate altamente cariche
Perché contano le goccioline proteiche
All’interno delle nostre cellule, molte reazioni vitali avvengono in strutture soffici a forma di goccia che non sono racchiuse da membrane. Questi “condensati biomolecolari” si comportano come piccoli compartimenti liquidi e sono spesso costituiti da proteine flessibili e altamente cariche. Esperimenti hanno mostrato che le molecole all’interno di alcune di queste goccioline possono muoversi sorprendentemente velocemente, nonostante le goccioline nel loro insieme possano essere piuttosto dense e appiccicose. Questo articolo pone una domanda semplice ma importante: in che modo l’ordine esatto di cariche positive e negative lungo queste proteine controlla la velocità dei movimenti all’interno di tali goccioline?
Costruire goccioline da catene cariche e flessibili
Gli autori si concentrano sulle proteine intrinsecamente disordinate—catene lunghe e flessibili che non si ripiegano in forme rigide. Molte di queste catene possiedono sia cariche positive sia negative, disposte in schemi diversi lungo la loro lunghezza. Usando simulazioni al computer su larga scala, il gruppo ha creato modelli di goccioline formate da molte copie di tali proteine, insieme ad acqua e piccoli ioni, per imitare l’ambiente affollato dei condensati reali. Hanno variato in modo sistematico quanto fosse “a blocchi” la distribuzione delle cariche, passando da sequenze in cui cariche positive e negative si alternano a sequenze in cui tutte le cariche positive sono raggruppate e tutte quelle negative formano un blocco separato.
Contenuto d’acqua e flusso fluido modellano il moto
Le simulazioni hanno rivelato che queste goccioline possono comunque comportarsi come veri liquidi con un contenuto d’acqua molto elevato—tra circa il 55% e l’84%, a seconda dello schema di cariche. Tale quantità di acqua significa che il flusso del fluido, o idrodinamica, non è completamente soppresso come suggerirebbero molte teorie sulle soluzioni polimeriche dense. Tracciando come i segmenti proteici vagano nel tempo, gli autori hanno trovato schemi di movimento caratteristici di catene il cui moto è favorito dal fluido circostante, piuttosto che rallentato soltanto dall’attrito. Questa influenza idrodinamica persiste fino e oltre la dimensione di un’intera catena proteica, specialmente nelle goccioline formate da sequenze con cariche più miste e quindi con più acqua.
Gli schemi locali di carica controllano la flessibilità a micro-scala
Esaminando più da vicino, gli autori hanno studiato come brevi porzioni di ogni catena si rilassano e si riorganizzano all’interno della gocciolina. Diverse porzioni della stessa proteina, contenenti lo stesso numero di unità costitutive, potevano muoversi a velocità molto diverse a seconda della loro miscela locale di cariche positive e negative. Le sezioni più bilanciate nelle cariche si rilassavano più rapidamente, mentre tratti dominati da un solo tipo di carica si muovevano con lentezza. Sorprendentemente, queste differenze rimanevano marcate nonostante argomentazioni semplici di schermatura prevedessero che gli effetti elettrostatici dovessero essere a corto raggio in condizioni così salate e affollate. Il lavoro mostra che il fatto che le cariche siano vincolate lungo una catena conserva correlazioni elettriche a lungo raggio che influenzano fortemente il moto locale.
La viscosità dipende dalla scala a cui si misura
Il gruppo ha quindi chiesto quanto «denso» appaiano queste goccioline a diverse scale di lunghezza. Utilizzando un metodo che collega piccole increspature nel momento del fluido alla sua resistenza al flusso, hanno calcolato una viscosità che dipende dalla lunghezza di indagine. Per tutte le sequenze, il fluido sembra meno viscoso quando sondato a scale molto piccole e più spesso quando sondato su tutta la gocciolina. Questa dipendenza dalla scala è particolarmente drammatica per le sequenze a blocchi di carica: per lo schema più segregato, la viscosità allo stato macroscopico è più di venti volte superiore rispetto alla viscosità locale a livello di monomero. Al contrario, le goccioline da sequenze ben miste mostrano una differenza molto più piccola. Nel complesso, la viscosità macroscopica cresce rapidamente con la concentrazione proteica, in linea con il comportamento delle soluzioni di polimeri neutri dense, nonostante le proteine siano esse stesse altamente cariche.
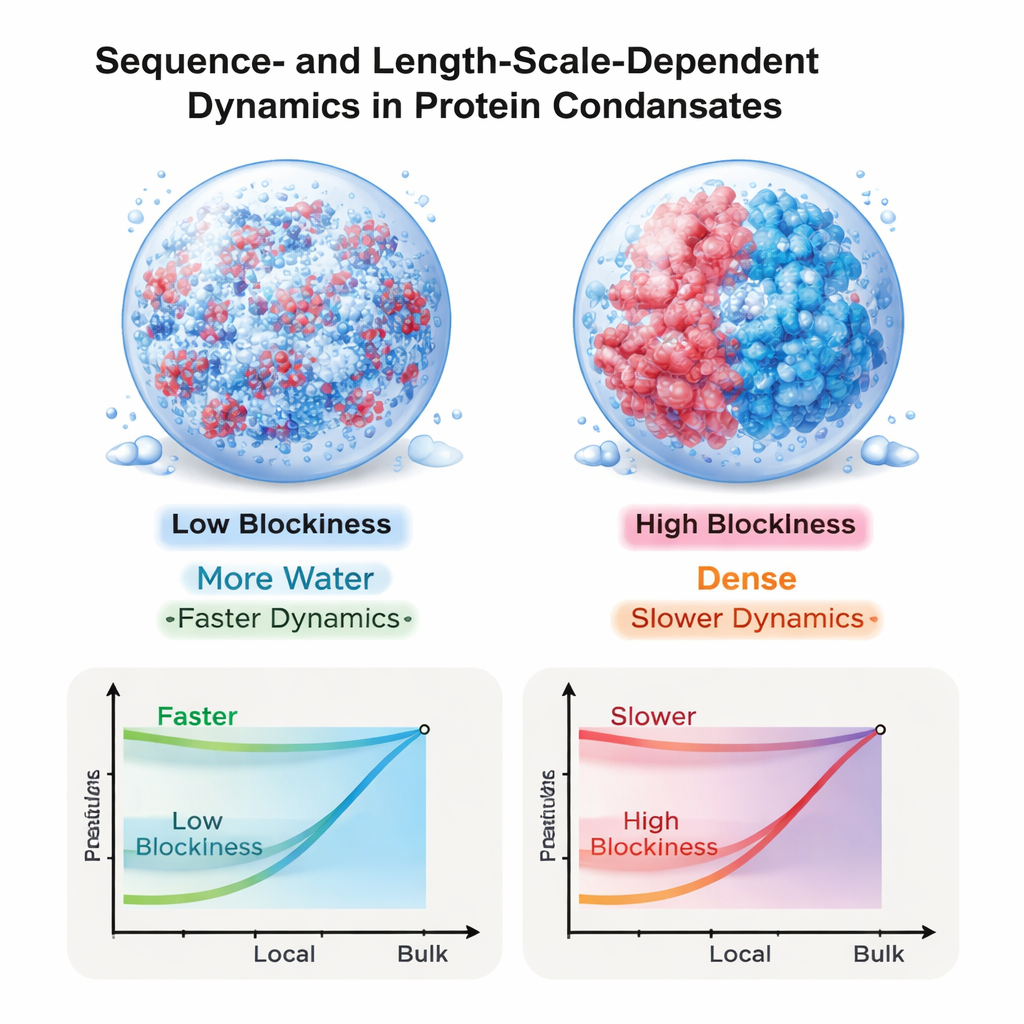
Collegare le simulazioni a esperimenti sconcertanti
Questi risultati aiutano a risolvere un apparente paradosso emerso da esperimenti recenti: come possono piccole molecole e segmenti proteici diffondere così rapidamente all’interno di condensati che, misurati nel loro insieme, appaiono estremamente viscosi? La risposta che emerge da questo lavoro è che sia il flusso dell’acqua sia le interazioni elettriche a lungo raggio rimangono importanti in queste goccioline, e il loro impatto è strettamente controllato da come le cariche sono ordinate lungo ogni catena. Le sequenze con schemi a blocchi producono goccioline dense e altamente viscose che tuttavia restano relativamente fluide su scale microscopiche, mentre sequenze più miste generano ambienti complessivamente più mobili. Dimostrando che la sequenza di cariche può modulare il movimento in modo diverso a differenti scale di lunghezza, lo studio offre un principio di progettazione per ingegnerizzare materiali sintetici a base di proteine e fa luce su come le cellule possano programmare il comportamento dei condensati attraverso la sequenza dettagliata delle loro proteine disordinate.
Citazione: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Parole chiave: condensati biomolecolari, proteine intrinsecamente disordinate, distribuzione delle cariche, dinamica delle proteine, viscosità