Clear Sky Science · it
Dinamicità della fotoossidazione del CO in CO2 sul rutile (110)
Perché osservare le molecole in un trilionesimo di secondo è importante
La vita moderna dipende da reazioni chimiche che depurano aria e acqua e trasformano la luce solare in energia utilizzabile. Molte di queste reazioni avvengono sulle superfici di materiali solidi detti fotocatalizzatori, alimentati dalla luce. Questo studio esplora una di quelle reazioni: come il velenoso monossido di carbonio (CO) viene trasformato in anidride carbonica (CO2) su una superficie di biossido di titanio — in scale temporali dell’ordine di pochi quadrilionesimi di secondo. Comprendere questi passaggi ultraveloci può aiutare gli scienziati a progettare materiali più intelligenti per il controllo dell’inquinamento, superfici autopulenti e tecnologie solari.
Una squadra di pulizia guidata dalla luce
Il biossido di titanio è un materiale ampiamente usato che si trova in vetri autopulenti, rivestimenti purificanti per l’aria e dispositivi sperimentali per combustibili solari. È economico, stabile e può usare la luce per innescare potenti reazioni di pulizia sulla sua superficie. Ma non tutte le forme di biossido di titanio si comportano allo stesso modo. Due forme comuni, chiamate anatase e rutile, differiscono nell’efficienza con cui guidano reazioni come la trasformazione del CO in CO2. Pur essendo generalmente più attiva complessivamente l’anatase, i dettagli temporali dei singoli passaggi della reazione — in particolare come l’ossigeno dall’aria viene attivato — non erano chiari. Questo studio si concentra sulla forma rutile con una specifica orientazione di superficie, nota come (110), per vedere esattamente quanto rapidamente il CO viene ossidato una volta che la luce colpisce il materiale.
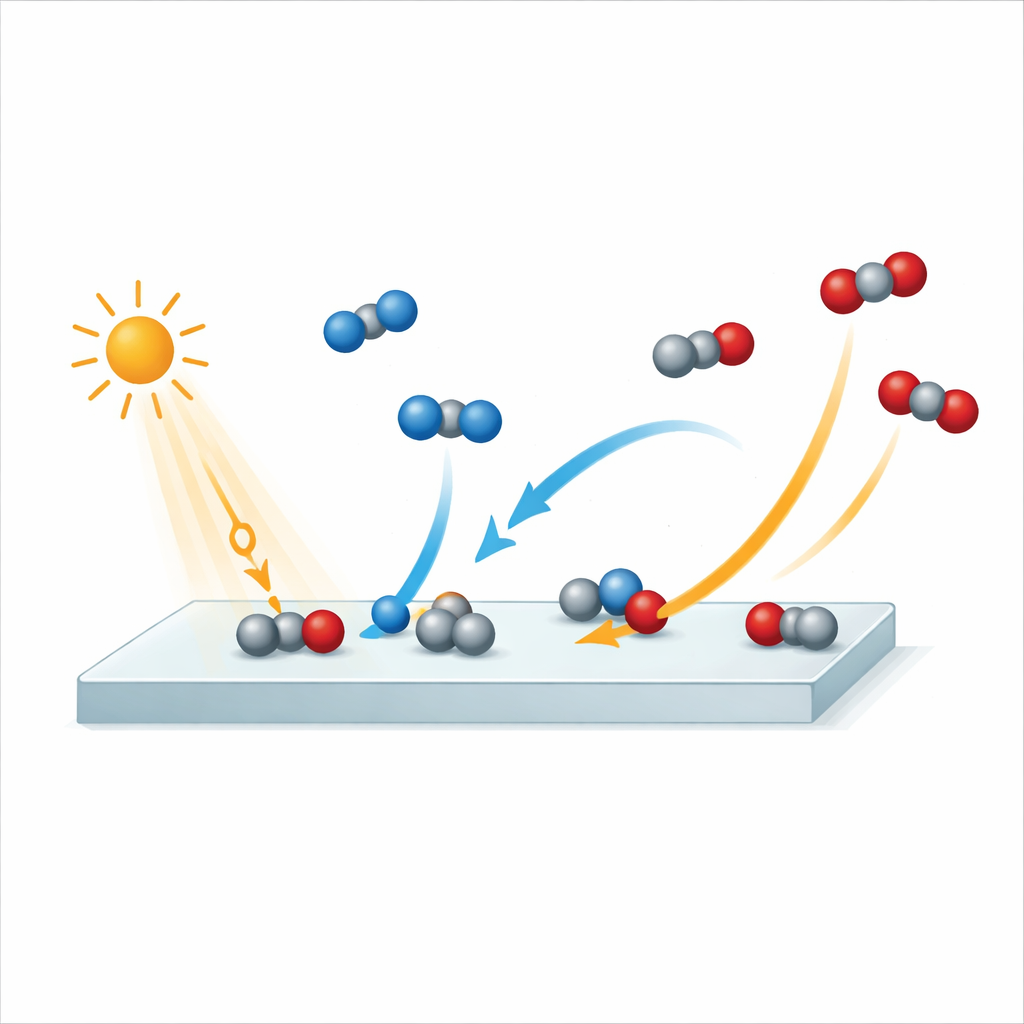
Riprendere una reazione a velocità estrema
Per catturare questo processo, i ricercatori hanno utilizzato un impianto a laser a elettroni liberi ad Amburgo che produce flash estremamente brevi di raggi X. Hanno prima colpito la superficie di rutile con un impulso di luce infrarossa, che funge da piccolo lampo fotografico che avvia la reazione. Un impulso di raggi X attentamente temporizzato ha quindi sondato come sono cambiati gli atomi e gli elettroni sulla superficie. Ripetendo questa sequenza con diversi ritardi tra gli impulsi di luce e di raggi X, hanno costruito una sorta di “film molecolare” della reazione con una risoluzione temporale di circa 250 femtosecondi — un femtosecondo è un milionesimo di miliardesimo di secondo. Il team ha monitorato segnali provenienti dagli atomi di ossigeno sulla superficie e nelle molecole gassose, permettendo di distinguere tra CO, CO2, acqua e l’ossido stesso mentre la reazione si svolgeva.
Catturare CO2 in meno di un trilionesimo di secondo
L’osservazione chiave è che nuova CO2 compare sulla superficie di rutile in tempi compresi tra circa 200 e 800 femtosecondi dopo l’impulso di luce. Ciò significa che l’ossigeno da molecole O2 vicine viene attivato, i legami si rompono e il CO viene convertito in CO2 in meno di un trilionesimo di secondo. Dopo circa 0,8 picosecondi, il segnale della CO2 fresca si affievolisce mano a mano che il prodotto desorbe dalla superficie. È sorprendente che tutta questa sequenza avvenga più rapidamente sul rutile rispetto all’anatase, dove lavori precedenti avevano osservato la prima comparsa di CO2 solo dopo circa 1,2–2,8 picosecondi in condizioni paragonabili. Anche se l’anatase produce complessivamente più CO2 ed è considerata il fotocatalizzatore più efficace, il rutile esegue il passo cruciale dell’ossidazione in modo più veloce.
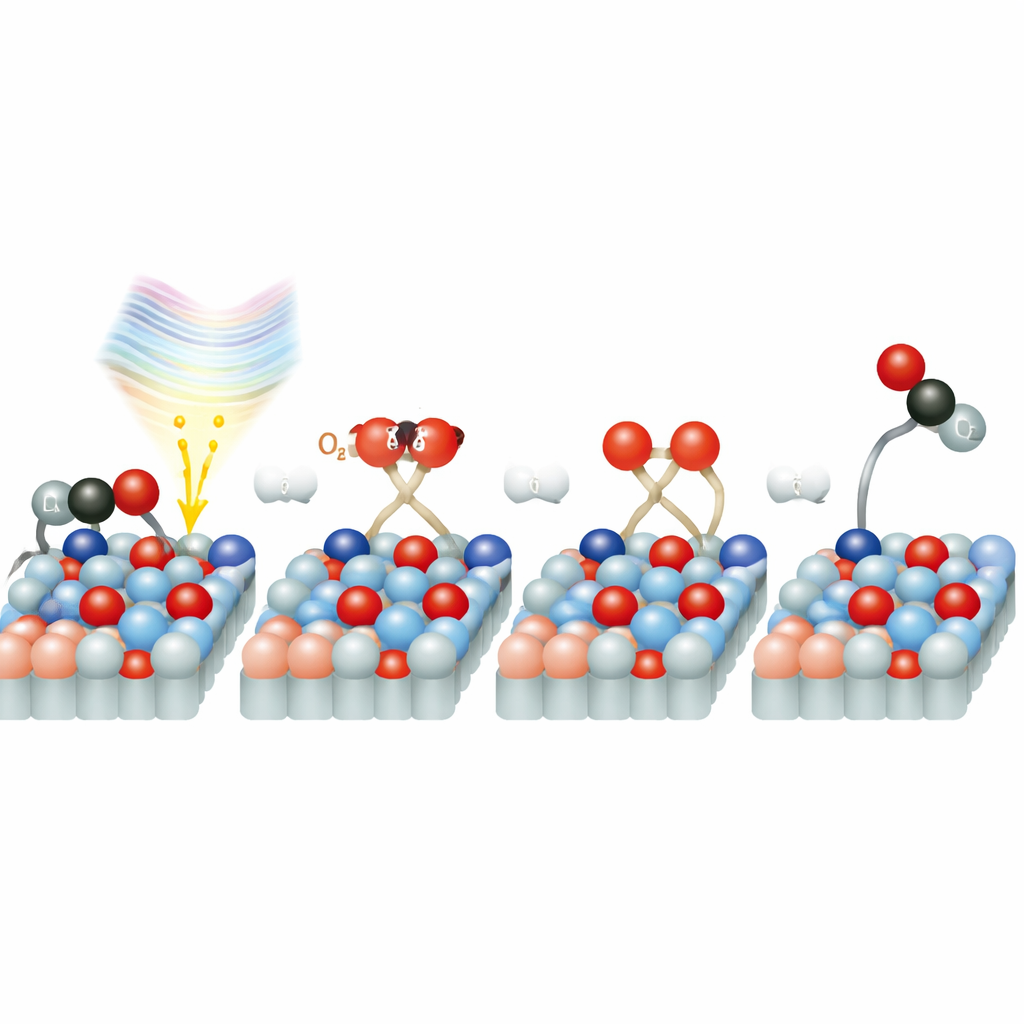
Un percorso di scorciatoia per l’ossigeno
Perché la reazione è così rapida sul rutile? Simulazioni dettagliate suggeriscono che le molecole di ossigeno poste sulla superficie creano stati elettronici speciali che agiscono da ponte tra il solido e l’O2. Quando la luce laser a 770 nanometri viene assorbita, può spostare direttamente un elettrone dal biossido di titanio nella molecola di ossigeno, formando una specie ossigenata carica e attivata. Questa “scorciatoia” evita il percorso più lento in cui gli elettroni viaggiano prima attraverso il volume del solido per poi migrare verso la superficie. Una volta attivato, l’ossigeno si scinde rapidamente e un atomo di ossigeno si combina con il CO per formare CO2. Lo studio rileva anche che tracce di acqua sulla superficie possono sia bloccare siti reattivi sia, a bassi livelli, potenzialmente aiutare questo trasferimento di carica e l’attivazione dell’ossigeno, aggiungendo un ulteriore livello di complessità.
Collegare la struttura elettronica alle prestazioni reali
Nel complesso, il lavoro mostra che dettagli minimi nel modo in cui gli elettroni si muovono tra una superficie e le molecole vicine possono cambiare drammaticamente la velocità delle reazioni, anche tra due materiali strettamente correlati. Pur mantenendo l’anatase il vantaggio in termini di resa fotocatalitica complessiva, il rutile evidenzia un passo di attivazione dell’ossigeno più rapido legato a questa speciale via di trasferimento di carica. Collegando misure ultrarapide e simulazioni avanzate, lo studio fornisce una roadmap per progettare superfici in modo che le reazioni innescate dalla luce avvengano con maggiore efficienza. A lungo termine, tali intuizioni potrebbero aiutare gli ingegneri a realizzare rivestimenti migliori per la purificazione dell’aria, superfici antibatteriche più efficaci e materiali migliorati per la produzione di combustibili solari e la scissione dell’acqua.
Citazione: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Parole chiave: fotocatalisi, biossido di titanio, spettroscopia ultrarapida, chimica di superficie, ossidazione del monossido di carbonio