Clear Sky Science · it
Sviluppo di un nanomodello a punti di carbonio con quadrupla coniugazione per la terapia mirata del glioma
Nuova speranza per tumori cerebrali ostinati
I tumori cerebrali ad alto grado come il glioblastoma sono tra i più difficili da trattare. Molti farmaci efficaci in altre parti del corpo non riescono a attraversare la barriera emato-encefalica protettiva o danneggiano il tessuto sano nel tragitto. Questo studio descrive una nanoparticella “intelligente” realizzata in laboratorio che mira a infiltrarsi più precisamente nei tumori cerebrali, trasportare un potente cocktail farmacologico e rilasciarlo direttamente all’interno dei nuclei delle cellule tumorali, dove può arrecare il massimo danno alle cellule cancerose risparmiando quelle normali.
Un piccolo camioncino di consegna costruito dal carbonio
Al centro del nuovo approccio ci sono i punti di carbonio—particelle su scala nanometrica fatte di carbonio, economiche da produrre, compatibili con l’acqua e fluorescenti sotto alcuni tipi di luce. Poiché le loro superfici sono ricche di ancoraggi chimici, possono essere decorate simultaneamente con molteplici componenti biologiche. In questo lavoro, i ricercatori hanno creato un nanomodello “a quadrupla coniugazione”: ogni punto di carbonio è stato legato chimicamente, in un’unica reazione in una sola vasca, a due peptidi di targeting diversi e a due carichi anticancro. Questo design modulare trasforma ogni punto in un piccolo camioncino che può riconoscere le cellule tumorali, attraversare barriere cellulari e portare i farmaci all’indirizzo intracellulare corretto.
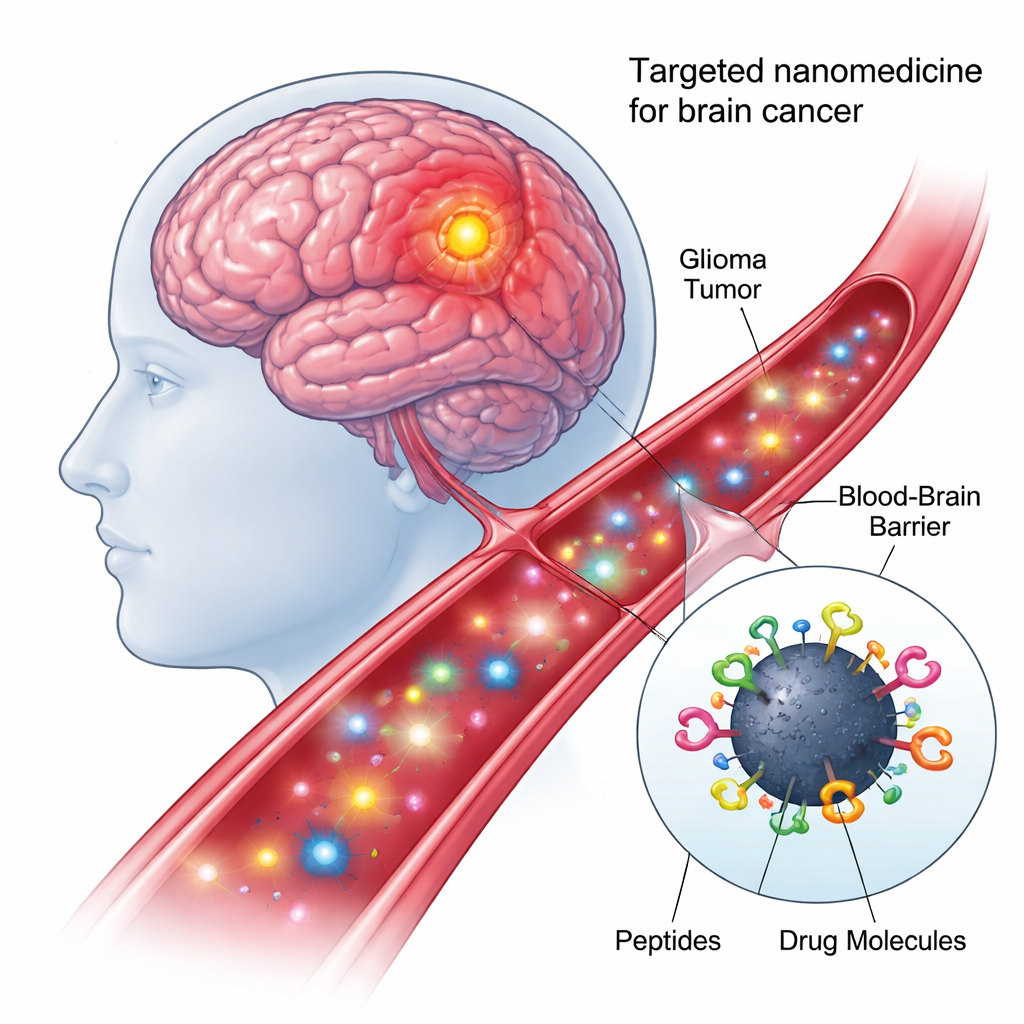
Trovare ed entrare nelle cellule cerebrali giuste
Il primo peptide sulla nanoparticella, chiamato shPep-1, è progettato per riconoscere un recettore denominato IL13Rα2. Questo recettore è espresso a livelli elevati in molti tumori cerebrali aggressivi—compresi il glioblastoma adulto e pediatrico e il glioma pontino intrinseco diffuso—ma è presente solo debolmente nelle cellule cerebrali normali. Legandosi a IL13Rα2, shPep-1 aiuta i punti di carbonio a localizzarsi sulle cellule tumorali ed entrarvi tramite captazione mediata da recettore. Il secondo peptide, più lungo, lnPep-1, contiene un segnale di localizzazione nucleare: una breve sequenza che facilita il passaggio del carico attraverso la membrana nucleare fino al centro di controllo della cellula, dove è conservato il DNA. Insieme, questi due peptidi conferiscono alla nanoparticella sia preferenza per il tumore sia la capacità di raggiungere il nucleo una volta all’interno.
Consegna di un attacco farmacologico coordinato
Il carico terapeutico è composto da due piccole molecole. La prima è l’epirubicina, un noto chemioterapico che uccide le cellule cancerose inserendosi nel DNA e bloccando gli enzimi necessari alla riparazione delle rotture a doppio filamento. La seconda è un metabolita chiamato 5-amminoimidazolo-4-carbossamide (AIC), prodotto a pH fisiologico dal farmaco per tumori cerebrali temozolomide. In lavori precedenti lo stesso gruppo ha mostrato che combinare epirubicina e AIC su un punto di carbonio aumentava l’uccisione delle cellule tumorali rispetto ai singoli farmaci. Nel nuovo design, entrambi sono co-consegnati sulla nanoparticella a doppio peptide, mirando a un effetto sinergico proprio nel nucleo delle cellule tumorali.
Potente nelle cellule tumorali, più mite per quelle normali
Per valutare l’efficacia del nanomodello, il team ha esposto diverse linee cellulari di glioma ad alto grado—glioblastoma adulto, glioblastoma pediatrico e un modello di glioma pontino intrinseco diffuso—ai punti di carbonio a quadrupla coniugazione. Anche a concentrazioni molto basse (fino a 50 nanomolari), la vitalità delle cellule tumorali scendeva a circa la metà rispetto ai controlli non trattati, e a dosi più elevate tutti i coniugati testati uccidevano la maggior parte delle cellule tumorali. È significativo che il nanomodello quadruplo abbia superato le versioni più semplici “a peptide singolo”, nonostante contenesse complessivamente meno epirubicina. Testato su cellule muscolari lisce vascolari non cancerose, è risultato molto meno tossico: queste cellule richiedevano circa 25–40 volte più nanoparticella per osservare una perdita di vitalità simile, suggerendo una finestra di sicurezza utile guidata dal targeting del tumore anziché da dosaggi massicci.
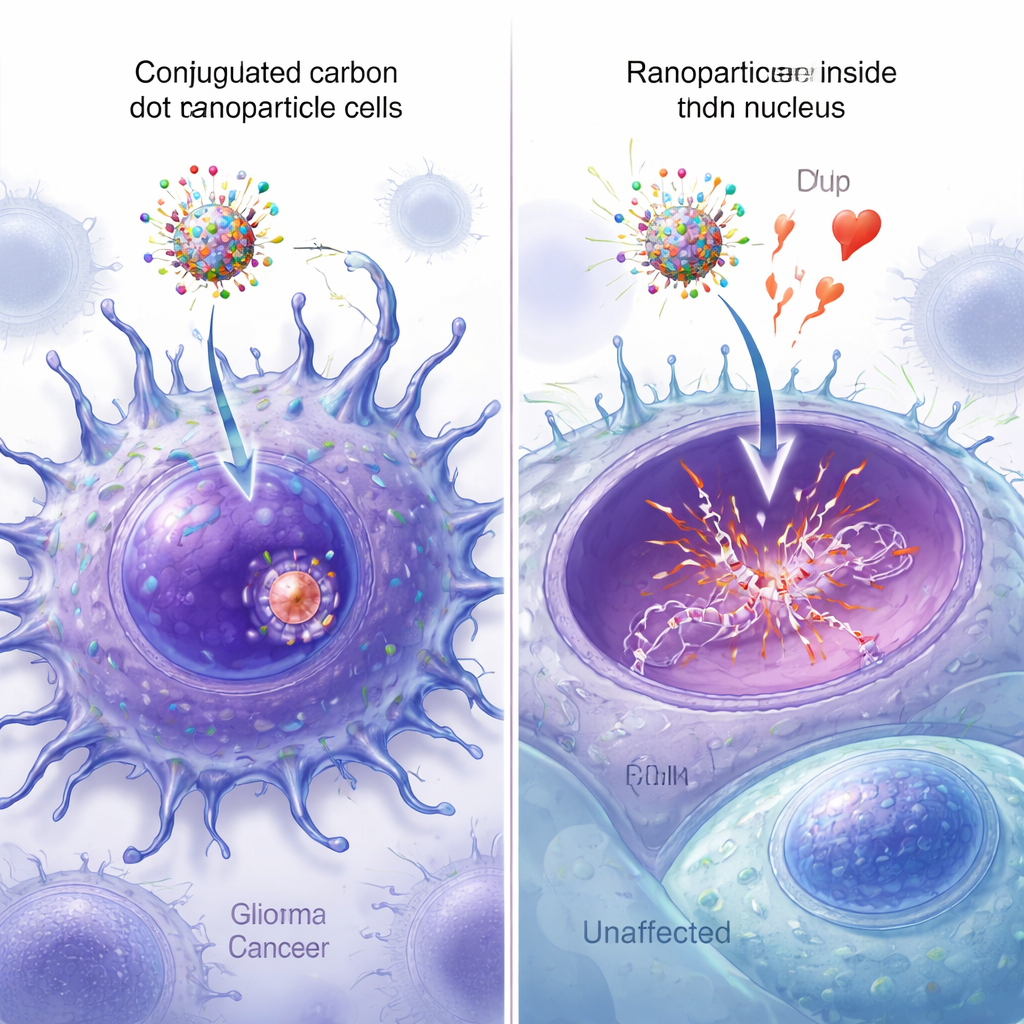
Osservare le nanoparticelle raggiungere il nucleo
Versioni fluorescenti delle nanoparticelle hanno consentito ai ricercatori di monitorare quanto bene ogni design entrasse nelle cellule e raggiungesse il nucleo. Al microscopio, i punti di carbonio dotati di entrambi i peptidi mostravano il segnale più brillante distribuito nelle cellule tumorali, con forte sovrapposizione tra la fluorescenza verde della nanoparticella e la colorazione nucleare blu. L’analisi quantitativa delle immagini ha confermato che le particelle a doppio peptide avevano la più alta colocalizzazione nucleare, superando significativamente quella delle particelle con un solo peptide o senza. Ulteriori misure con spettroscopia, spettrometria di massa e microscopia a forza atomica hanno verificato che tutti e quattro i componenti erano stati effettivamente attaccati ai punti di carbonio e ne avevano aumentato modestamente le dimensioni, senza compromettere la funzione chiave di legame al DNA dell’epirubicina.
Cosa potrebbe significare per la cura futura dei tumori cerebrali
Per i pazienti, questi risultati sono ancora una dimostrazione in fase iniziale su colture cellulari e non una terapia pronta per l’uso clinico. Tuttavia mettono in luce un concetto promettente: una nanoparticella a base di carbonio, piccola, stabile e relativamente facile da produrre, che può essere rapidamente personalizzata con peptidi di targeting e combinazioni farmacologiche. Orientando i farmaci specificamente verso le cellule tumorali che sovraesprimono IL13Rα2 e concentrandoli nel nucleo, tali nanomedicine potrebbero un giorno consentire dosi più basse, meno effetti collaterali e strategie terapeutiche più personalizzate per tumori cerebrali altamente letali come il glioblastoma e il glioma pontino intrinseco diffuso.
Citazione: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Parole chiave: glioblastoma, nanomedicina, punti di carbonio, consegna mirata di farmaci, tumori cerebrali