Clear Sky Science · it
Un saggio generalizzabile per l’accumulo intracellulare per profilare la somministrazione citosolica di farmaci in cellule di mammifero
Perché è importante far entrare i farmaci nelle cellule
Molti dei farmaci più promettenti oggi—piccole molecole, brevi frammenti proteici chiamati peptidi e proteine a grandezza naturale—sono progettati per agire su bersagli all’interno delle nostre cellule. Ma la membrana cellulare è una barriera difficile da superare. Un farmaco può aderire alla superficie della cellula o rimanere intrappolato in sacche interne chiamate endosomi e comunque non raggiungere il fluido interno, il citosol, dove risiedono molti bersagli. Questo articolo descrive un nuovo test di laboratorio, chiamato saggio CHAMP, che indica ai ricercatori non solo se una molecola entra nella cellula, ma se arriva effettivamente nel citosol, dove può svolgere la sua funzione.
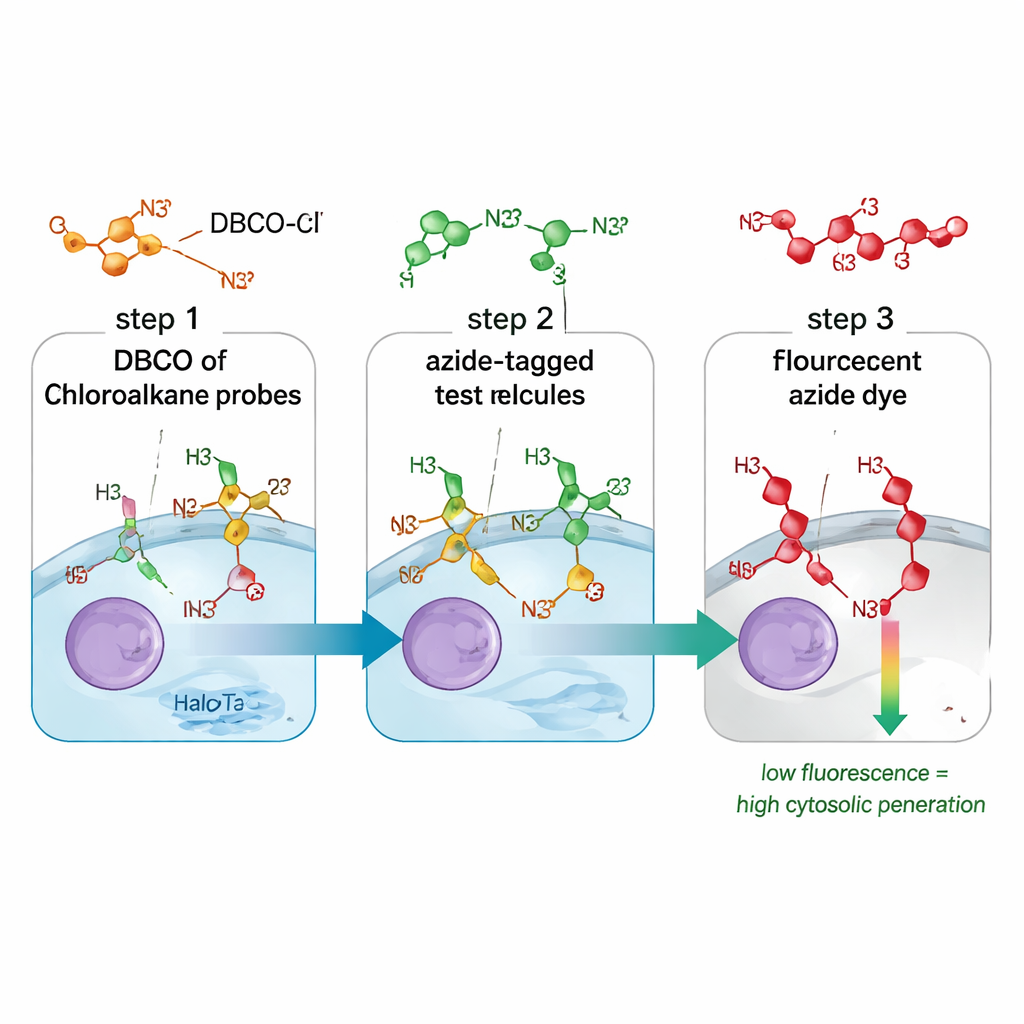
Un nuovo modo di tracciare l’ingresso dei farmaci
I metodi tradizionali per misurare l’assorbimento dei farmaci spesso confondono molecole che solo toccano la superficie cellulare, si trovano negli endosomi o raggiungono con successo il citosol. Possono anche dipendere da marcatori fluorescenti ingombranti che modificano il comportamento della molecola. Il saggio CHAMP risolve entrambi i problemi combinando una piccola “maniglia” chimica chiamata azide con un marcatore proteico chiamato HaloTag, progettato per essere libero nel citosol di cellule umane coltivate. Prima, le cellule vengono trattate con una molecola linker che attacca DBCO, una forma tesa di alchino, a HaloTag. Successivamente, gli scienziati aggiungono il composto in prova, che porta la piccola etichetta azide. Solo se quel composto attraversa la membrana cellulare e raggiunge il citosol l’azide e il DBCO possono reagire insieme in una reazione chimica altamente selettiva. Un colorante azidico fluorescent finale rivela quanti siti DBCO restano: cellule deboli indicano che il composto di prova è entrato e ha occupato la maggior parte dei siti; cellule luminose indicano scarso accesso citosolico.
Dal concetto al saggio operativo
Gli autori hanno innanzitutto confermato che HaloTag veniva espresso correttamente e localizzato nel citosol di cellule HeLa umane usando un colorante cloroalchile standard e imaging. Hanno quindi ottimizzato ogni fase di CHAMP: la quantità di linker DBCO da aggiungere, i tempi di incubazione e quale colorante azide fluorescente offrisse un segnale forte e specifico senza danneggiare le cellule. La citometria a flusso—uno strumento che misura la fluorescenza in migliaia di singole cellule—ha mostrato che il saggio era rapido, robusto e regolabile. Fondamentale, il team ha dimostrato che la fluorescenza derivava davvero da reazioni specifiche sui siti HaloTag piuttosto che da coloranti che si attaccano in modo non specifico ai componenti cellulari, e che la piccola etichetta azide non perturbava in modo apprezzabile il modo in cui le molecole entravano nelle cellule.
Ciò che il saggio rivela su piccole molecole e peptidi
Con CHAMP a disposizione, i ricercatori lo hanno messo alla prova con centinaia di piccole molecole etichettate con azide e hanno variato sistematicamente caratteristiche come carica, dimensione e flessibilità. Hanno osservato, per esempio, che trasformare un acido carbossilico carico negativamente in un’ammide neutra aumentava l’accumulo citosolico, e che il grado e la posizione della metilazione dell’azoto cambiavano l’efficacia con cui i composti penetravano. Confrontando le reazioni su perline libere rispetto a cellule vive, sono riusciti a separare la reattività chimica intrinseca dalla barriera imposta dalla membrana stessa. Il team ha anche applicato CHAMP a un pannello di antibiotici comuni, mostrando che alcuni raggiungevano il citosol molto meglio di altri—informazione importante quando si trattano batteri che si nascondono all’interno delle cellule dell’ospite.
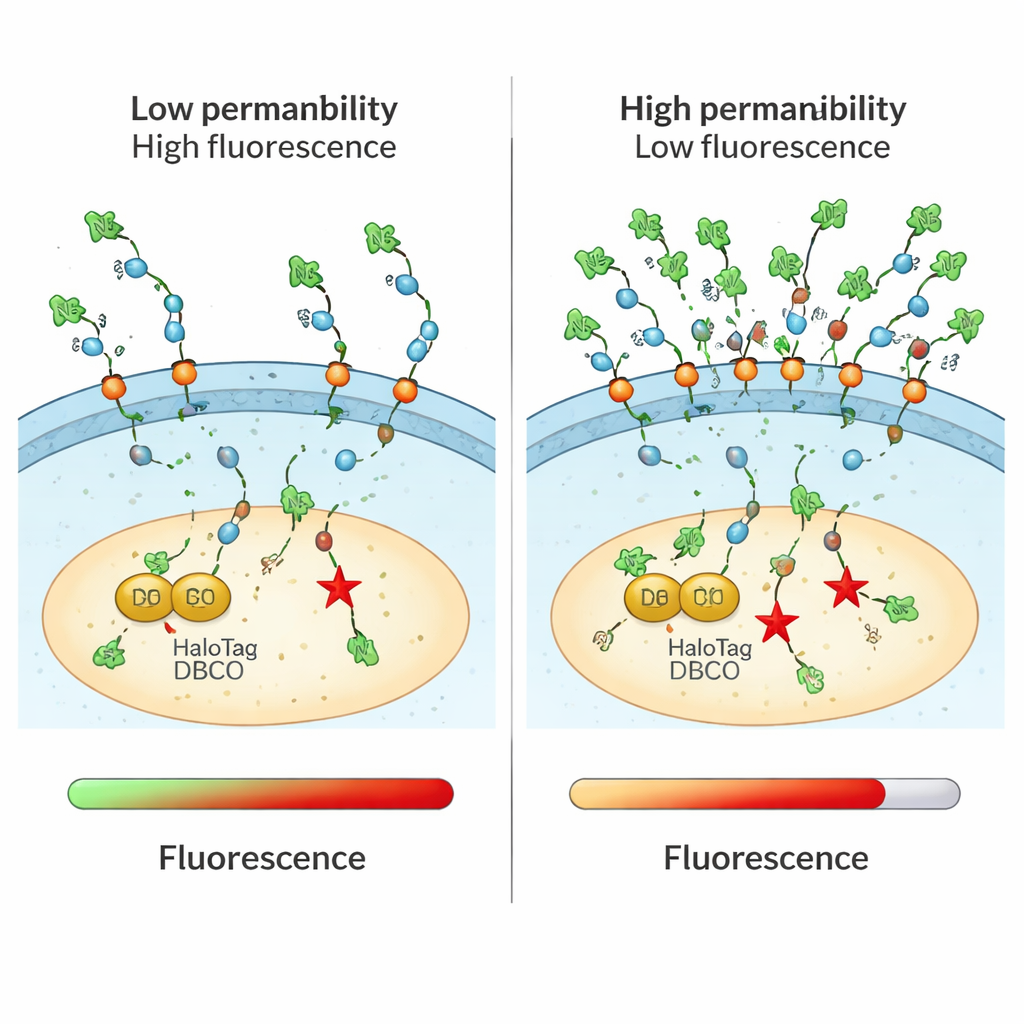
Peptidi e proteine supercariche che attraversano la barriera
Il saggio è stato particolarmente potente per studiare molecole più grandi e fortemente cariche che sono difficili da tracciare con altri metodi. Gli autori hanno esaminato peptidi penetranti la cellula costituiti da molte unità di arginina e hanno confermato una tendenza chiara: catene più lunghe e più positive trasportavano più materiale nel citosol, fino a un certo punto. Hanno studiato come invertire la chiralità (stereochimica) di alcuni amminoacidi alterasse l’ingresso, trovando che versioni speculari a volte si accumulavano meglio, suggerendo interazioni chirali sottili con la membrana. CHAMP ha inoltre mostrato che proteine “supercariche”—ingegnerizzate per portare molte cariche positive—potevano raggiungere il citosol più efficacemente rispetto ai corrispondenti naturali, supportando il loro potenziale come vettori per carichi terapeutici di grandi dimensioni.
Regole di progettazione per i futuri farmaci intracellulari
Testando in modo sistematico piccole molecole, peptidi, peptidi macrocilici e scheletri modificati, lo studio ha messo in luce principi generali di progettazione. I peptidi macrocilici, i cui scheletri sono chiusi ad anello, tendevano a raggiungere il citosol più facilmente rispetto alle versioni lineari e flessibili. Gruppi N-metil ben posizionati sui backbone peptidici miglioravano moderatamente l’ingresso, ma un eccesso poteva risultare controproducente. Queste relazioni struttura–permeazione, rivelate con un unico saggio standardizzato, offrono indicazioni pratiche per i chimici che cercano di progettare molecole che non solo si leghino ai loro bersagli ma possano effettivamente raggiungerli all’interno delle cellule.
Come questo aiuta lo sviluppo dei farmaci
In termini semplici, il saggio CHAMP è un contatore del traffico finemente tarato alla porta d’ingresso e nei corridoi interni della cellula. Indica agli scienziati quali farmaci sperimentali riescono veramente a superare la membrana e a entrare nel citosol, senza essere ingannati da molecole bloccate sulla superficie o in compartimenti interni. Poiché funziona con una vasta gamma di forme e dimensioni molecolari e usa solo una piccola etichetta azide, CHAMP può essere integrato nelle pipeline di scoperta ad alto rendimento. Col tempo, questo dovrebbe accelerare la progettazione di terapie più efficaci per le malattie i cui bersagli più importanti sono rinchiusi all’interno delle nostre cellule.
Citazione: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Parole chiave: consegna intracellulare di farmaci, permeabilità della membrana cellulare, accumulo citosolico, peptidi penetranti la cellula, chimica click bioortogonale