Clear Sky Science · it
Deidroclorurazione assistita da idrogeno del 1,1,1,2-tetrafluoro-2-cloropropano a 2,3,3,3-tetrafluoropropene su Pd-Ag/nano-MgF2 con siti Pd isolati ottimizzati
Refrigeranti più puliti per un mondo che si riscalda
Condizionatori e frigoriferi ci mantengono comodi, ma molte delle sostanze che li fanno funzionare sono potenti gas serra. Questo studio affronta una sfida cruciale: come produrre uno dei refrigeranti di nuova generazione più importanti, l’HFO‑1234yf, in modo più efficiente e con un’impronta di carbonio inferiore. Progettando un catalizzatore più intelligente — in sostanza una piccola macchina chimica microscopica — gli autori mostrano un modo per ottenere questo refrigerante a basso potenziale di riscaldamento a temperature più basse e con molti meno sottoprodotti indesiderati.
Perché serve una chimica dei refrigeranti migliore
I tradizionali idrofluorocarburi (HFC), come l’HFC‑134a usato nei condizionatori d’auto, intrappolano il calore nell’atmosfera migliaia di volte più intensamente dell’anidride carbonica. Accordi internazionali come l’emendamento di Kigali ne stanno riducendo l’uso, spingendo l’industria verso le idrofluoroolefine (HFO), che mantengono prestazioni simili ma con un potenziale di riscaldamento globale molto più basso (spesso sotto 10). L’HFO‑1234yf è il principale candidato a sostituirli, tuttavia i metodi industriali attuali per produrlo si basano su passaggi ad alta temperatura, energivori, che riducono anche la durata dei catalizzatori e aumentano gli scarti. Una via più fredda e più selettiva per ottenere HFO‑1234yf potrebbe quindi ridurre sia le emissioni sia i costi operativi.
Una via più gentile verso una molecola chiave
Gli autori si concentrano sulla conversione di un composto correlato, l’HCFC‑244bb, in HFO‑1234yf rimuovendo cloruro di idrogeno (HCl) con l’aiuto di idrogeno gassoso. Questa “deidroclorurazione assistita da idrogeno” permette alla reazione di procedere a temperature relativamente moderate di 270 °C — ben al di sotto dei 600–800 °C spesso richiesti dai metodi puramente termici. Al centro del processo c’è un catalizzatore solido su misura: piccole particelle cave di fluoruro di magnesio (nano‑MgF2) decorate con palladio (Pd) e argento (Ag). Variando l’ordine di aggiunta di Pd e Ag durante la preparazione, il gruppo può controllare quanto i due metalli si mescolano — formando leghe di carattere diverso — e come i siti attivi di Pd compaiono infine sulla superficie durante la reazione.
Trasformare grappoli metallici in atomi singoli
Durante le prime ore di attività, i catalizzatori mostrano un “periodo di induzione”: la conversione dell’HCFC‑244bb diminuisce lentamente, mentre la selettività verso l’HFO‑1234yf desiderato aumenta costantemente. Microscopia, spettroscopia e misure di superficie attente rivelano il perché. Con il procedere della reazione, l’acido cloridrico formato in situ clorura le particelle metalliche, rompendo i cluster di Pd più grandi e rimodellandoli in atomi di Pd isolati ancorati sulla superficie del nano‑MgF2. I catalizzatori che partono con un grado maggiore di legame Pd–Ag — ottenuto quando Pd viene aggiunto per primo e poi Ag — subiscono la ristrutturazione più estesa e finiscono con la densità maggiore di siti Pd monoatomici. Questo materiale ottimizzato converte circa il 60% dell’HCFC‑244bb e indirizza approssimativamente l’82% del prodotto verso HFO‑1234yf, sopprimendo fortemente la idrogenazione profonda verso un composto saturo indesiderato, l’HFC‑254eb.
Come il comportamento dell’idrogeno controlla il risultato
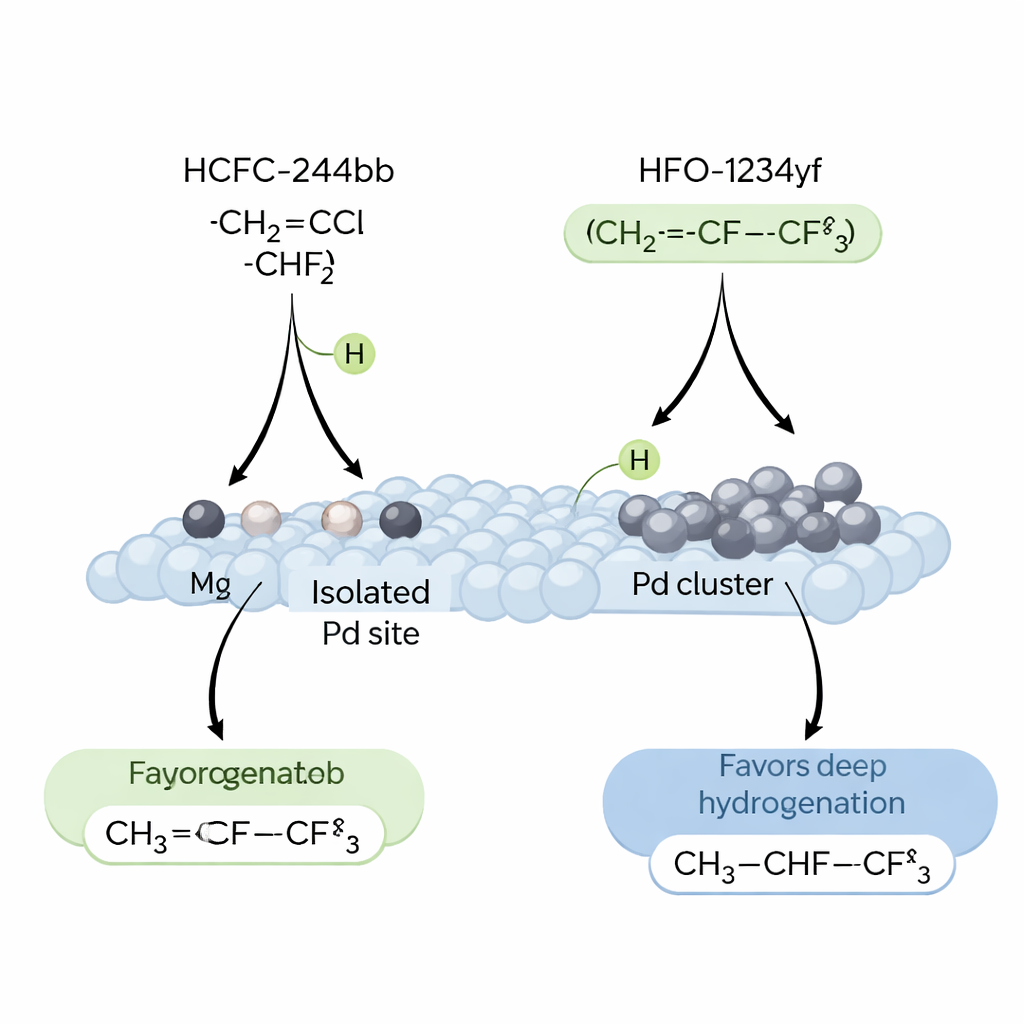
Per capire perché gli atomi di Pd isolati funzionano così bene, i ricercatori hanno studiato come l’idrogeno, la molecola reagente e il prodotto interagiscono con diverse superfici catalitiche. Hanno trovato che sia l’HCFC‑244bb sia l’idrogeno preferiscono adsorbirsi sul Pd, non sull’Ag, ma che la forza e la natura del legame con l’idrogeno sono critiche. I grandi aggregati di Pd tendono a creare un idrogeno in “spillover” che rimane fortemente legato a temperature elevate e favorisce l’iper‑idrogenazione, trasformando l’apprezzato HFO‑1234yf in prodotti saturi meno utili. Al contrario, i siti Pd monoatomici trattengono l’idrogeno in una forma più reattiva ma meno persistente, ideale per rimuovere pulitamente l’HCl e formare il doppio legame carbonio‑carbonio desiderato. Simulazioni al calcolatore basate sulla teoria del funzionale di densità confermano questo quadro, mostrando che questi ambienti Pd–fluoruro isolati facilitano la rimozione dell’idrogeno dagli intermedi chiave nel percorso verso l’HFO‑1234yf, rendendo invece meno favorevoli dal punto di vista energetico i passaggi di idrogenazione secondaria.
Dall’intuizione di laboratorio a un raffreddamento più verde
In termini pratici, il miglior catalizzatore Pd–Ag/nano‑MgF2 fornisce tassi di formazione di HFO‑1234yf decine di volte superiori rispetto ai precedenti catalizzatori solidi che si basavano su deidroclorurazioni dure e ad alta temperatura. Il lavoro dimostra che controllare gli atomi metallici uno per uno — non solo come nanoparticelle — può orientare drasticamente i percorsi di reazione, migliorando sia l’efficienza sia la selettività. Per i non specialisti, il messaggio chiave è che un design migliore dei catalizzatori può tradursi direttamente in una produzione più pulita dei refrigeranti moderni. Questo, a sua volta, aiuta il mondo a raggiungere gli obiettivi climatici mantenendo freschi edifici, veicoli e scorte alimentari.
Citazione: Yang, C., Mao, W., Dong, X. et al. Hydrogen-assisted dehydrochlorination of 1,1,1,2-tetrafluoro-2-chloropropane to 2,3,3,3-tetrafluoropropene over Pd-Ag/nano-MgF2 with optimized Pd isolated sites. Commun Chem 9, 93 (2026). https://doi.org/10.1038/s42004-026-01896-w
Parole chiave: refrigeranti, catalisi, palladio-argento, gas serra, idrofluoroolefine