Clear Sky Science · it
La catalisi dei DNAzimi innescata da superfici metalliche per un’efficiente scissione del DNA
Metalli che fanno tagliare il DNA
La maggior parte di noi pensa al metallo come a qualcosa di solido e inerte—buono per monete, pentole e fili, ma non per compiere reazioni chimiche in un bicchiere d’acqua. Questo studio ribalta quell’intuizione mostrando che pezzi di metallo nudo possono attivare piccoli catalizzatori a base di DNA, chiamati DNAzimi, usando soltanto acqua pura e aria. Il lavoro rivela un modo inatteso in cui materiali comuni come il rame e altri metalli possono guidare reazioni di tipo biologico sulle loro superfici, suggerendo nuovi strumenti per sensori, medicina e persino chimica delle origini della vita. 
Cosa sono le forbici del DNA?
I DNAzimi sono brevi filamenti di DNA che si ripiegano in strutture capaci di accelerare reazioni chimiche specifiche, in modo analogo agli enzimi proteici. Molti DNAzimi conosciuti agiscono come forbici molecolari che tagliano altri filamenti di DNA o RNA, ma quasi sempre hanno bisogno di ioni metallici disciolti—come rame, zinco o magnesio—in soluzione per funzionare. Uno di questi DNAzimi, chiamato PL, è un filamento che si auto-taglia e normalmente dipende da ioni rame e da certi cofattori come la vitamina C o il perossido di idrogeno. Questi ausili partecipano a reazioni redox (di trasferimento di elettroni) che generano specie reattive dell’ossigeno molto aggressive, le quali attaccano e rompono lo scheletro del DNA in posizioni precise.
Quando un filo di rame diventa un cofattore
Esplorando un apparato elettrochimico per controllare l’attività di PL, i ricercatori notarono qualcosa di sorprendente: immergere semplicemente un filo di rame nudo in una soluzione contenente PL e acqua bidistillata portava a una scissione efficiente del DNA, anche senza aggiunta di ioni rame, tamponi o sali. La sola superficie di rame eguagliava o superava le prestazioni delle miscele tradizionali di ioni rame più vitamina C o perossido, tagliando il DNA esattamente nello stesso sito. Test successivi mostrarono che molti oggetti di rame—lastre, imbuti, pentole e persino monete di diverse valute—potevano innescare la scissione di PL, con l’entità della reazione che dipendeva dall’area di superficie metallica a contatto con la gocciolina. Il rame lucidato di fresco funzionava leggermente meno bene rispetto al rame invecchiato e ossidato, suggerendo che uno strato sottile formato dall’esposizione all’aria potrebbe effettivamente favorire la reazione.
Quali superfici funzionano—e perché
Per verificare se si trattasse di una curiosità del solo rame, il gruppo ha testato 24 metalli e 10 materiali non metallici. Hanno scoperto che solo certi metalli, come rame, tantalio e vanadio, attivavano fortemente PL, mentre vetro, plastica, legno e altri non metalli non avevano effetto. Le misure mostrarono che piccole quantità di ioni metallici si staccano nell’acqua dalle superfici attive, ma questi ioni da soli erano troppo deboli per spiegare la forte scissione del DNA. L’ingrediente mancante risultò essere ossigeno reattivo derivato dall’aria disciolta. Usando sequestranti chimici ed enzimi, gli autori dimostrarono che il superossido—una forma energetica di ossigeno con un elettrone in più—è essenziale. Quando l’ossigeno disciolto veniva rimosso facendo scorrere azoto, l’attività di PL quasi scompariva; reinserire ossigeno ripristinava il taglio. Nel loro complesso i dati supportano un ciclo in cui la superficie metallica e gli ioni che essa rilascia convertono l’ossigeno disciolto in superossido e perossido d’idrogeno proprio all’interfaccia solido-liquido, e queste specie poi guidano la scissione del DNA. 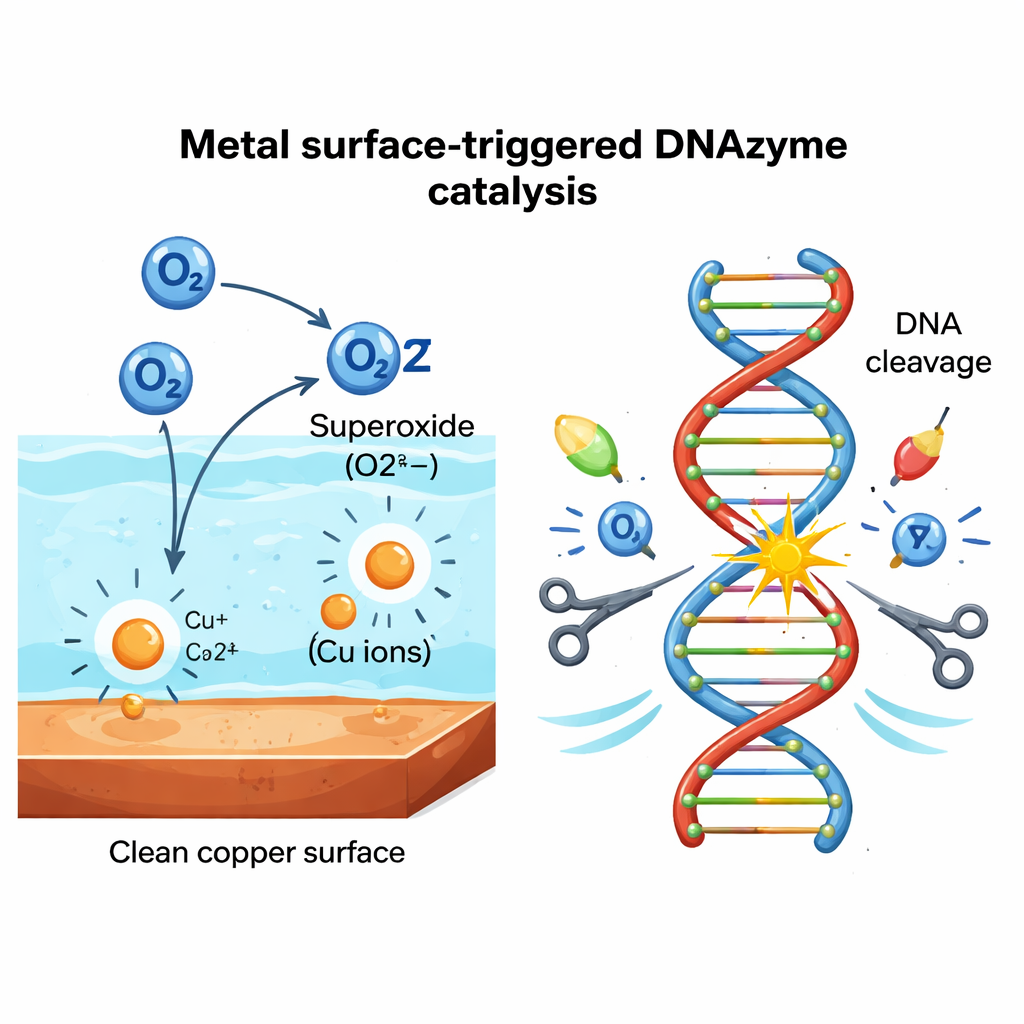
Aiutanti, bloccanti e altri DNAzimi
La chimica innescata dalla superficie poteva essere modulata usando molecole note. Chelanti come l’EDTA, che catturano gli ioni metallici, rallentavano la reazione. La catalasi, un enzima che degrada il perossido d’idrogeno, e coloranti che assorbono il superossido riducevano anch’essi il taglio del DNA, confermando il ruolo di queste specie reattive dell’ossigeno. Al contrario, piccole molecole come la vitamina C, il glutatione e la catecol aumentavano l’attività nutrendo il ciclo redox che genera superossido vicino alla superficie metallica. Sorprendentemente, l’effetto non era unico per PL: altri DNAzimi che tagliano DNA o RNA, inclusi F-8, Ag10c e I-R3, venivano anch’essi attivati dai corrispondenti metalli bulk (per esempio, argento metallico per un DNAzima dipendente dall’argento e zinco metallico per uno dipendente dallo zinco). Ciò suggerisce che la catalisi del DNA “attivata da superficie metallica” potrebbe essere un fenomeno ampio piuttosto che una singola stranezza.
Perché questo conta oltre il laboratorio
Per i lettori non specialisti, il messaggio centrale è che le superfici metalliche solide possono agire come partner chimici invisibili per catalizzatori a base di DNA, usando solo aria e acqua per generare le specie reattive necessarie a tagliare il DNA. Invece di dover dissolvere quantità precise di ioni metallici, si può semplicemente mettere a contatto una superficie metallica adatta con una soluzione di DNA e lasciare che l’interfaccia faccia il lavoro. Questo apre possibilità per sensori a basso costo che rilevino oggetti metallici, strumenti per monitorare o eliminare radicali ossigeno dannosi nelle cellule e nuovi modi per studiare come reazioni simili alla vita possano avvenire su superfici minerali o metalliche. In breve, la tua moneta di rame non è solo spicciolo—può essere anche una piccola fabbrica chimica per forbici del DNA.
Citazione: Jiang, F., Dong, Y., Yu, W. et al. Metal surface-triggered DNAzyme catalysis for efficient DNA cleavage. Commun Chem 9, 91 (2026). https://doi.org/10.1038/s42004-026-01893-z
Parole chiave: DNAzima, catalisi su superfici metalliche, specie reattive dell’ossigeno, chimica dell’interfaccia del rame, scissione del DNA