Clear Sky Science · it
Crescita controllata di cristalli sferulitici da miscele saline
Perché i cristalli di sale possono somigliare a fiori
La maggior parte di noi pensa ai cristalli come a forme nette e sfaccettate, ma in natura spesso crescono in sfere spettacolari che ricordano fiori o palle di neve. Queste “sferuliti” compaiono nelle rocce vulcaniche, nei calcoli renali e persino in alcune malattie legate a proteine mal ripiegate. Questo articolo esplora come un minerale di uso comune, il solfato di sodio—lo stesso sale presente in detersivi e in alcuni materiali da costruzione—possa essere indotto a formare cristalli sferici così intricati e cosa questo rivela sul modo in cui strutture complesse si autoassemblano a partire da ingredienti semplici.
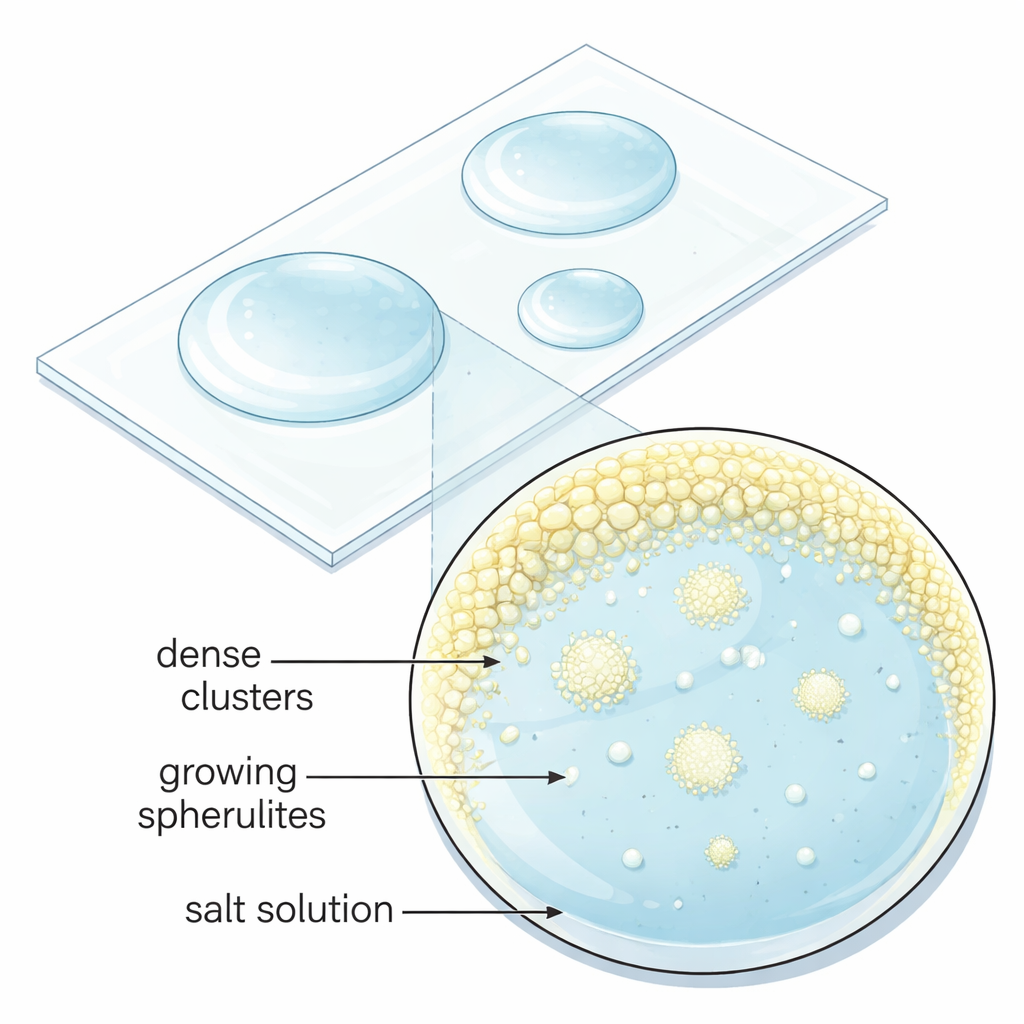
Da sali semplici a sfere scolpite
I ricercatori hanno cercato di capire quando e come il solfato di sodio cresce in sferuliti invece che in cristalli angolari ordinari. Hanno preparato goccioline microscopiche d’acqua contenenti miscele di solfato di sodio e altri solfati i cui ioni metallici hanno carica doppia positiva, come magnesio o ferro. Mentre queste goccioline, da picolitri a microlitri, evaporavano lentamente su vetrini a temperatura ambiente, i sali disciolti si concentravano sempre di più fino all’inizio della cristallizzazione. Variando sistematicamente il rapporto di miscelazione, hanno individuato precisi “punti ottimali” di composizione nei quali il solfato di sodio produceva coerentemente cristalli sferici a texture radiali. Al di fuori di questi intervalli, la stessa soluzione generava o grani sfaccettati regolari o un solido gelatinoso senza caratteristiche, dimostrando che le forme sferiche richiedono condizioni accuratamente regolate.
Piccole tasche liquide che innescano sfere cristalline
Al microscopio il gruppo ha osservato che le sferuliti non comparivano direttamente da una soluzione limpida. L’evaporazione generava prima piccoli agglomerati liquidi densi, arricchiti in ioni disciolti, vicino al bordo della goccia. Queste tasche di dimensioni microniche persistono per minuti prima di far germinare improvvisamente molte sferuliti contemporaneamente. Immagini ad alta risoluzione al microscopio elettronico delle strutture essiccate hanno rivelato che ogni sferulite è composta da innumerevoli cristalli di solfato di sodio di dimensioni nanometriche orientati approssimativamente verso l’esterno, che poi si fondono insieme. Questo comportamento contraddice l’immagine scolastica della crescita cristallina, in cui un singolo nucleo stabile cresce omogeneamente, e indica invece un percorso multi-step “non classico” in cui goccioline dense e nanoparticelle si assemblano e si riorganizzano fino a raggiungere la forma solida finale.
Quando l’acqua salata diventa densa come il burro di arachidi
Una parte cruciale della storia è quanto densa, o viscosa, diventi la soluzione man mano che l’acqua evapora. Monitorando la velocità di espansione delle sferuliti e misurando direttamente le proprietà di flusso di soluzioni saline correlate, gli autori hanno mostrato che le soluzioni miste sodio–magnesio o sodio–ferro diventano straordinariamente viscose—fino a circa 100 volte più dense del miele—proprio nel momento in cui le sferuliti cominciano a formarsi. Questa consistenza prossima al “burro di arachidi” rallenta così tanto il moto degli ioni che è la diffusione, non la chimica di superficie, a limitare la velocità di crescita dei cristalli. In questo ambiente pigro, si formano innumerevoli piccoli agglomerati e nanocristalli che hanno il tempo di aderire fra loro in aggregati sferici anziché crescere in pochi grandi cristalli ben modellati. Gli ioni metallici bivalenti sono la chiave: legano l’acqua in modo stretto e si collegano in catene o reti corte, aumentando la viscosità e favorendo la formazione di uno sfondo amorfo, simile a un gel, intorno alle sferuliti in crescita.
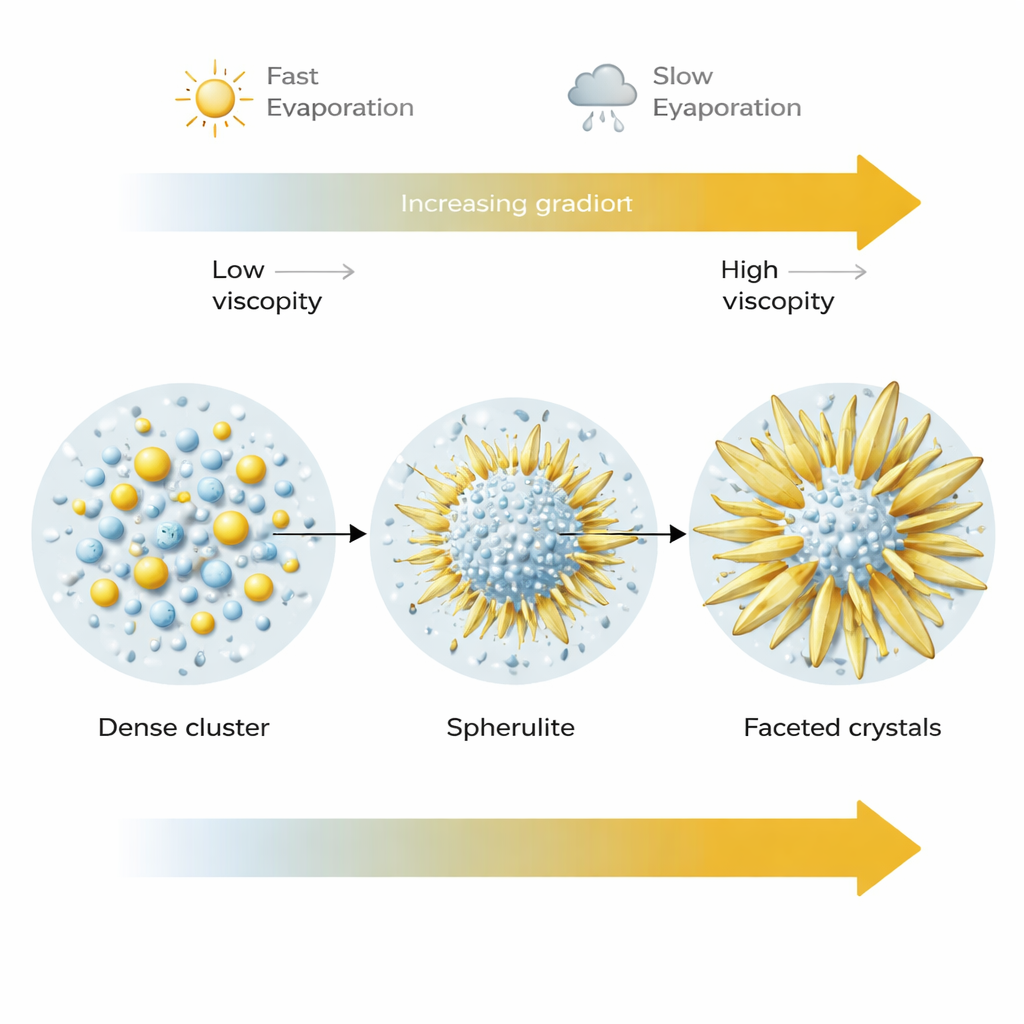
Come la velocità di essiccazione rimodella i cristalli finali
La velocità di evaporazione si è rivelata un altro potente parametro di controllo. Con un’essiccazione più rapida (minore umidità) molte sferuliti si nucleavano ma restavano relativamente piccole, bloccate nella loro forma sferica metastabile mentre il fluido circostante si addensava rapidamente. Con un’essiccazione più lenta (umidità più alta), le stesse sfere iniziali avevano più tempo e accesso agli ioni disciolti. I loro piccoli blocchi costitutivi potevano riorganizzarsi e fondersi in cristalli più grandi, più lisci e più sfaccettati, spesso con escrescenze a lama che alla fine si convertivano nella forma di solfato di sodio termodinamicamente stabile. In altre parole, le strutture sferiche fungono da stadio transitorio in un percorso di crescita che può terminare con forme molto diverse, a seconda della rapidità con cui la soluzione si asciuga e della facilità con cui la materia può ancora muoversi al suo interno.
Perché questo ha importanza oltre i cristalli belli da vedere
In termini semplici, lo studio mostra che sfere saline belle e simili a fiori sorgono quando miscele concentrate di sali semplici diventano sufficientemente dense da rallentare tutto, ma non così tanto da fermare completamente la crescita. In queste condizioni “giuste”, tasche liquide dense e sciami di piccoli cristalli si autoassemblano in aggregati sferici che possono poi evolvere in grani più stabili e sfaccettati. Capire e controllare questo delicato equilibrio tra composizione, viscosità ed evaporazione apre la strada a progettare texture cristalline su misura per applicazioni che vanno da materiali da costruzione più resistenti e farmaci migliorati a modelli migliori di formazione cristallina in contesti geologici e biologici.
Citazione: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Parole chiave: sferuliti, solfato di sodio, <keyword>nucleazione non classica, soluzioni saline