Clear Sky Science · it
Prima struttura cristallina di un addotto formato dalla reazione di un composto del vanadio con la transferrina sierica umana
Perché una proteina del sangue e un farmaco metallico contano
Molti farmaci sperimentali contengono atomi metallici che possono contribuire a curare malattie che vanno dal diabete al cancro. Ma una volta che questi medicinali a base di metalli entrano nel flusso sanguigno, devono agganciarsi alle proteine di trasporto naturali del corpo. Questo studio esamina come una di queste proteine, la transferrina sierica umana — il principale vettore del ferro nel nostro sangue — interagisca con un promettente composto di vanadio, facendo luce su come i farmaci metallici vengono trasportati nell’organismo e su come potrebbero essere perfezionati per terapie più sicure ed efficaci.
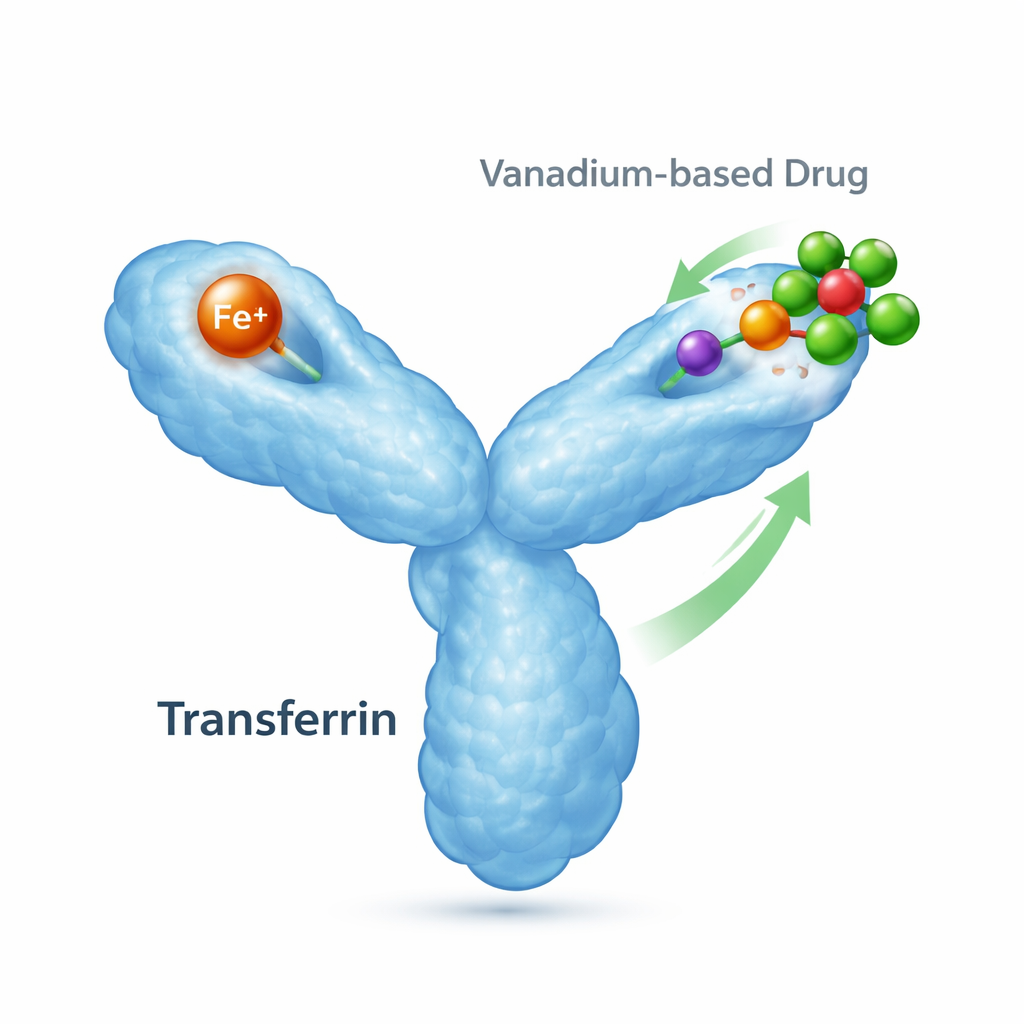
Il corriere del ferro dell’organismo e i suoi ruoli secondari
La transferrina è una proteina di circa 80 kilodalton il cui compito principale è catturare il ferro e consegnarlo alle cellule che ne hanno bisogno. Presenta due “lobi”, ciascuno in grado di legare un ione di ferro, e cambia conformazione a seconda della presenza del ferro. Quando il ferro si lega, un lobo si chiude; senza ferro rimane aperto. Recettori specializzati sulla superficie cellulare riconoscono queste forme cariche di ferro e le internalizzano, rendendo la transferrina centrale per l’equilibrio del ferro e la salute cellulare. Tuttavia, la transferrina può anche legare altri metalli, compresi quelli utilizzati in trattamenti medici, il che significa che può influenzare dove i farmaci metallici si spostano e come agiscono.
Un’istantanea conformazionale del vanadio sulla transferrina
I ricercatori si sono concentrati su un candidato farmaco al vanadio ben studiato chiamato bis(acetilacetonato)oxovanadio(IV), spesso indicato come [VIVO(acac)₂]. Studi precedenti avevano mostrato che questo composto, o specie derivate da esso in acqua, possono legarsi alla transferrina, ma nessuno aveva osservato esattamente come. Usando la cristallografia a raggi X, il gruppo ha ottenuto strutture ad alta risoluzione della transferrina che porta ferro solo nel lobo C‑terminale (la forma “FeC”), sia prima sia dopo l’esposizione al composto di vanadio. Nei cristalli trattati con vanadio non hanno osservato il farmaco originale, ma un frammento trasformato contenente vanadio e ossigeno legato al lobo N privo di ferro. Questo ha fornito la prima immagine strutturale diretta di un frammento di vanadio attaccato alla transferrina umana.
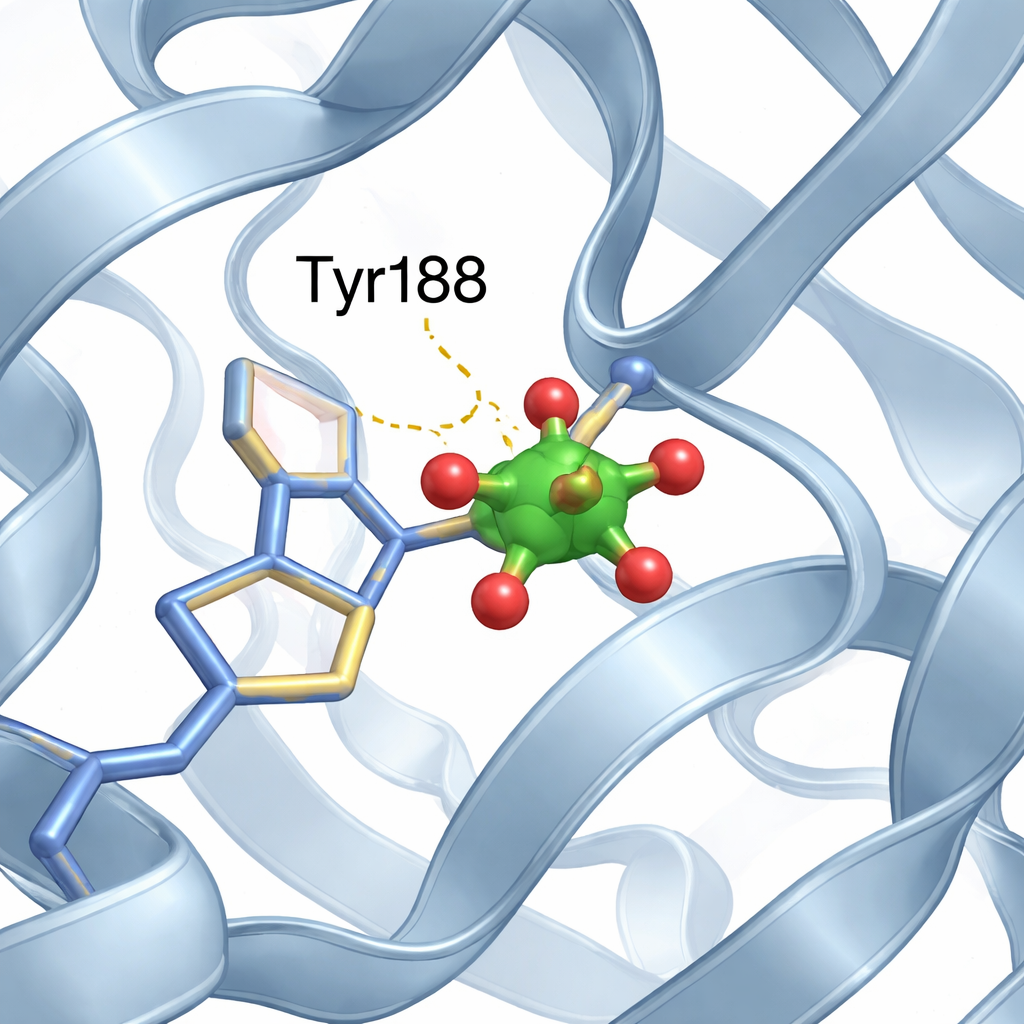
Un minuscolo cluster di vanadio trova il suo spazio
All’interno del sito del ferro del lobo N, il team ha identificato un piccolo cluster composto da due atomi di vanadio e atomi di ossigeno, descritto al meglio come un’unità modificata di “divanadato”. Una delle posizioni di ossigeno del cluster è occupata dall’ossigeno di un amminoacido specifico, la tirosina 188 (Tyr188), formando un legame diretto tra proteina e cluster metallico. Interazioni complementari più deboli, come legami a idrogeno da segmenti proteici vicini, stabilizzano ulteriormente il cluster in sede. È importante sottolineare che, nonostante questo nuovo ospite metallico occupi una tasca di legame del ferro, la proteina mantiene la sua abituale conformazione con il lobo N aperto e il lobo C chiuso, quasi identica alla struttura priva di vanadio.
Come la transferrina rimodella la chimica del vanadio
In soluzione, al pH e alle concentrazioni usate per la cristallizzazione, la specifica specie a due vanadi osservata nel cristallo è normalmente solo un attore di minoranza; tendono a predominare cluster di vanadio‑ossigeno più grandi. Misure spettroscopiche e calcoli teorici di speciazione suggeriscono che il farmaco originale a base di vanadio si ossida lentamente e si decompone in acqua, producendo ioni vanadato semplici che poi si assemblano in una varietà di cluster. La struttura cristallina indica che la transferrina stabilizza selettivamente questo piccolo frammento simile al divanadato rispetto ai cluster più grandi, scegliendo essenzialmente una forma chimica da una miscela complessa in soluzione fornendo un sito di legame accogliente su Tyr188 e una rete di legami a idrogeno di supporto.
Conservare la stretta di mano con il recettore cellulare
Poiché la transferrina deve legare un recettore sulla superficie cellulare per consegnare il ferro, i ricercatori si sono chiesti se l’attacco di questo cluster di vanadio potesse compromettere quella stretta di mano cruciale. Usando elettroforesi su gel non denaturante e una tecnica sensibile chiamata interferometria a biostratificazione, hanno misurato quanto bene la transferrina trattata con vanadio legasse il recettore della transferrina rispetto alla forma trattata solo con ferro. Entrambe si comportavano quasi in modo identico, con un legame molto forte nell’ordine dei nanomolari bassi. Questo conferma che il cluster di vanadio, pur annidandosi nel lobo N, non altera in modo significativo la conformazione della transferrina nelle aree di interazione con il recettore e quindi non dovrebbe impedire al protein di essere riconosciuta dalle cellule.
Cosa significa per i farmaci a base di metalli
Per i non specialisti, il messaggio è che questo studio fornisce un’istantanea molecolare di come un derivato di un farmaco al vanadio si attacca al principale corriere del ferro dell’organismo senza mettere fuori uso la sua funzione normale. La transferrina può catturare un particolare piccolo cluster vanadio‑ossigeno in un sito di legame del ferro, eppure la forma complessiva della proteina e la sua capacità di legare il recettore restano sostanzialmente invariate. Ciò aiuta a spiegare come i farmaci a base di vanadio potrebbero circolare legati alla transferrina e mette in evidenza che proteine diverse possono favorire dimensioni diverse di cluster di vanadio. Questi approfondimenti sono fondamentali per progettare terapie metalliche più intelligenti il cui comportamento nel sangue — quali forme assumono, dove vanno e quanto durano — possa essere previsto e controllato.
Citazione: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Parole chiave: farmaci a base di vanadio, transferrina sierica umana, terapie metalliche, legame metallo‑proteina, biologia strutturale