Clear Sky Science · it
Il lattame abilita riarrangiamenti boronati remoti verso legami C═N
Una nuova scorciatoia per costruire molecole tipo farmaco
I chimici sono sempre alla ricerca di modi più rapidi e puliti per assemblare le molecole complesse presenti nei medicinali e nei materiali avanzati. Questo studio presenta una trovata intelligente che consente a una struttura ad anello comune, chiamata lattame, di guidare temporaneamente una reazione per poi ritirarsi silenziosamente—rendendo possibile trasformare ingredienti semplici e facilmente reperibili in preziosi mattoni per la sintesi farmaceutica senza l’uso di metalli costosi o passaggi di preparazione elaborati.
Trasformare un aiutante discreto in una guida temporanea
Molti farmaci moderni e materiali funzionali si basano su reazioni degli acidi boronici, una famiglia di composti contenenti boro apprezzata per la loro affidabilità e comportamento mite. Tradizionalmente, per indurre gli acidi boronici a formare nuovi legami con doppi legami carbonio–azoto (C=N), i chimici devono preinstallare speciali «gruppi direzionali» sui materiali di partenza. Questi gruppi fungono da maniglie che orientano la reazione, ma richiedono tempo, denaro e passaggi aggiuntivi—e spesso funzionano solo con partner molto reattivi. Gli autori hanno capito che i lattami, parenti ad anello del familiare legame ammidico presente nelle proteine, possono funzionare come guide integrate e temporanee. Coordinandosi all’atomo di boro, l’ossigeno del lattame aiuta a formare un centro di boro altamente organizzato e tetracoordinato che può trasferire un frammento legato a una posizione distante lungo la molecola, predisponendo la formazione di nuovi legami carbonio–azoto senza alcun gruppo direzionale permanente.
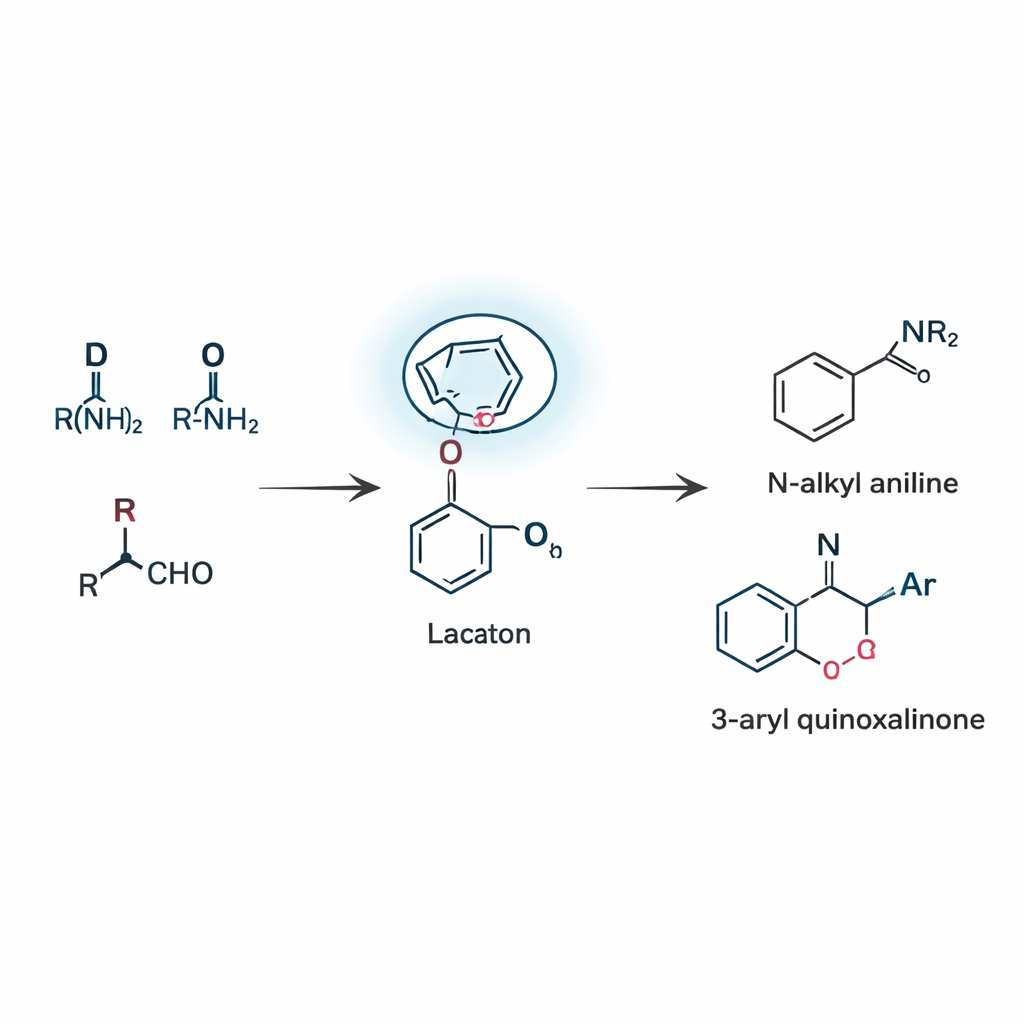
Costruire due famiglie di prodotti utili con un’unica strategia
Partendo da questo concetto, il gruppo ha sviluppato due reazioni correlate che si basano entrambe su questo riassestamento guidato dal lattame, noto come riarrangiamento boronato remoto. Nella prima, tre pezzi semplici—un aldeide, un ammina e un acido boronico—si uniscono per formare aniline N‑alchilate, un motivo chiave che compare in innumerevoli candidati farmaci e coloranti. La reazione procede attraverso un raro spostamento 1,5, in cui un gruppo arilico legato al boro salta sopra cinque atomi per raggiungere il legame C=N. Regolando con cura il catalizzatore, il solvente e la temperatura, i ricercatori hanno ottenuto rese ragionevoli e mostrato che sono tollerati molti sostituenti diversi, inclusi alogeni, gruppi alchilici e eterocicli. Nella seconda modalità di reazione, la stessa idea direttiva viene applicata ai chinoxalinoni, una classe di anelli ricchi di azoto comune nella chimica medicinale. Qui la reazione non impiega alcun catalizzatore metallico aggiunto e fornisce comunque in modo efficiente chinoxalinoni 3‑arilici, grazie alla capacità del lattame di coinvolgere il boro e stabilizzare l’intermedio chiave.
Condizioni verdi e modifica in fase avanzata di farmaci
Oltre a dimostrare un ampio campo di applicazione, gli autori mostrano che questa strategia è pratica per molecole del mondo reale. Poiché il riarrangiamento 1,4 sui chinoxalinoni avviene in condizioni prive di metalli in un solvente alcolico specializzato, si evita l’uso di metalli di transizione costosi o tossici. Il team ha applicato il metodo a frammenti complessi derivati da farmaci commercializzati come l’ibuprofene e altri principi terapeutici che contengono lo scheletro del chinoxalinone. In ogni caso, la reazione ha installato nuovi gruppi arilici in una posizione specifica senza alterare altre funzionalità sensibili. Questo tipo di «funzionalizzazione in fase avanzata» permette ai chimici di decorare rapidamente nuclei farmacologici esistenti con nuove catene laterali, accelerando la ricerca di miglioramenti in potenza, sicurezza o proprietà fisiche.
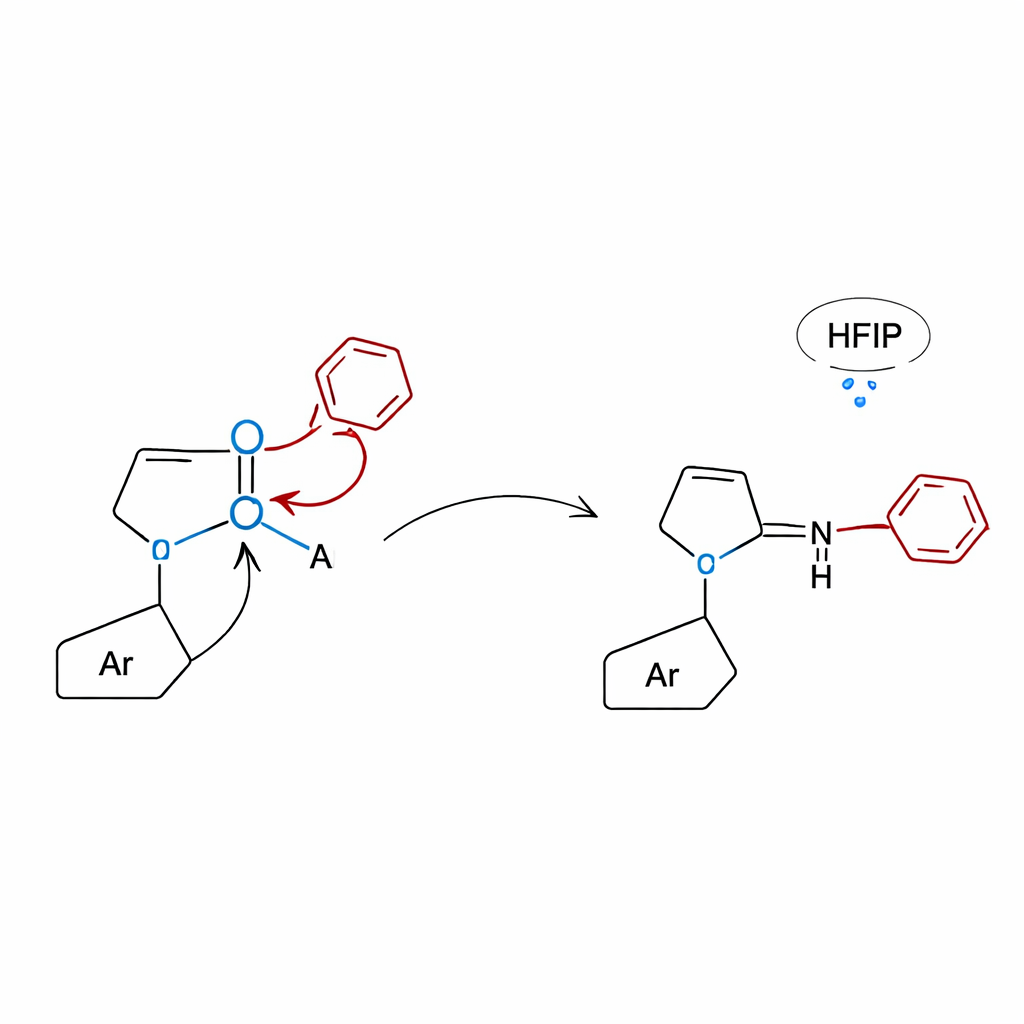
Dare un’occhiata sotto il cofano con teoria e test di controllo
Per capire perché l’approccio del lattame funziona così bene, i ricercatori hanno combinato esperimenti di controllo progettati con cura e simulazioni al computer. Quando sono state testate molecole prive della porzione di lattame, le reazioni si sono praticamente spente, confermando che l’anello del lattame è essenziale per attivare l’acido boronico e dirigere il riarrangiamento. Calcoli di chimica quantistica hanno rivelato che l’ossigeno del lattame si lega al boro formando una struttura compatta tetracoordinata dalla quale il gruppo arilico può migrare o su cinque atomi (spostamento 1,5) per dare aniline N‑alchiliche o su quattro atomi (spostamento 1,4) per dare chinoxalinoni 3‑arilici. Nel caso dei chinoxalinoni, la rete di legami a idrogeno fornita dal solvente HFIP abbassa ulteriormente la barriera energetica, aiutando la reazione a procedere in condizioni termiche relativamente miti senza alcun catalizzatore aggiunto.
Perché questo conta per i farmaci del futuro
Nel complesso, il lavoro mostra che un semplice anello di lattame può agire come una guida dinamica e riciclabile che sblocca schemi di formazione di legami precedentemente inaccessibili nella chimica degli acidi boronici. Per i non specialisti, il messaggio chiave è che i chimici dispongono ora di un modo più diretto ed efficiente per trasformare mattoni di base in due classi importanti di molecole contenenti azoto che stanno alla base di molti farmaci. Poiché il metodo evita metalli preziosi, tollera un’ampia gamma di gruppi funzionali e funziona su strutture avanzate simili a quelle farmaceutiche, è destinato a semplificare la progettazione e l’ottimizzazione dei futuri prodotti farmaceutici e, potenzialmente, anche di nuovi agrochimici.
Citazione: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Parole chiave: acidi boronici, chimica dei lattami, formazione di legami C–N, chinoxalinoni, chimica medicinale