Clear Sky Science · it
La mutazione della sindrome PACS1 interrompe il trasporto mediato da dineina tramite HDAC6 e BICD2
Perché è importante per lo sviluppo cerebrale
La sindrome PACS1 è una rara patologia genetica che provoca disabilità intellettiva, crisi epilettiche e tratti facciali distintivi. Famiglie e clinici conoscono i sintomi, ma fino a poco tempo fa non era chiaro cosa andasse realmente storto all’interno delle cellule dei pazienti. Questo studio scioglie il mistero, mostrando come una singola sostituzione nella sequenza del gene PACS1 scombussoli il sistema di trasporto interno della cellula, in particolare nei neuroni, e come ciò colleghi la sindrome PACS1 a una più ampia famiglia di malattie da “traffico” del sistema nervoso. 
Le autostrade di consegna della cellula
Ogni cellula si affida a autostrade microscopiche fatte di tubi proteici chiamati microtubuli. Motori molecolari corrono lungo questi binari, trasportando carichi come enzimi e compartimenti di membrana verso i punti in cui servono. Un motore, la dineina, è responsabile dei "viaggi di ritorno" a lunga distanza, tirando il carico dalla periferia della cellula verso il centro, dove si trova una stazione di smistamento importante chiamata apparato di Golgi. Gli autori si concentrano su PACS1, una proteina che aiuta a selezionare quali carichi vengono affidati alla dineina e che regola anche lo stato dei binari tramite un’altra proteina, HDAC6, che controlla un marcatore chimico (acetilazione) sui microtubuli. I neuroni, con le loro estensioni molto lunghe, sono particolarmente sensibili anche a piccoli difetti di questo sistema.
Un coordinatore mutato che si aggrappa troppo
La sindrome PACS1 è causata dalla ricorrente mutazione R203W in PACS1. Il gruppo ha scoperto che sia la forma normale sia quella mutata di PACS1 si legano fisicamente alla catena pesante della dineina, ma la versione mutata si attacca con maggiore forza. Utilizzando cellule cutanee di pazienti e linee cellulari ingegnerizzate, hanno dimostrato che questo iper‑coinvolgimento produce lo stesso risultato della perdita parziale della funzione della dineina: il Golgi si disgrega in mini‑stack disseminati e un enzima importante chiamato furina, normalmente localizzato sul lato trans del Golgi, viene deviato verso altri compartimenti. Analizzando la struttura di PACS1, hanno individuato una breve "toppa" a foglietto beta che contatta specificamente la dineina. Quando hanno alterato questa patch senza disturbare le altre funzioni di PACS1, la furina ha nuovamente perso la sua corretta localizzazione, confermando che la stretta di mano dineina–PACS1 è cruciale per il posizionamento corretto dei carichi. 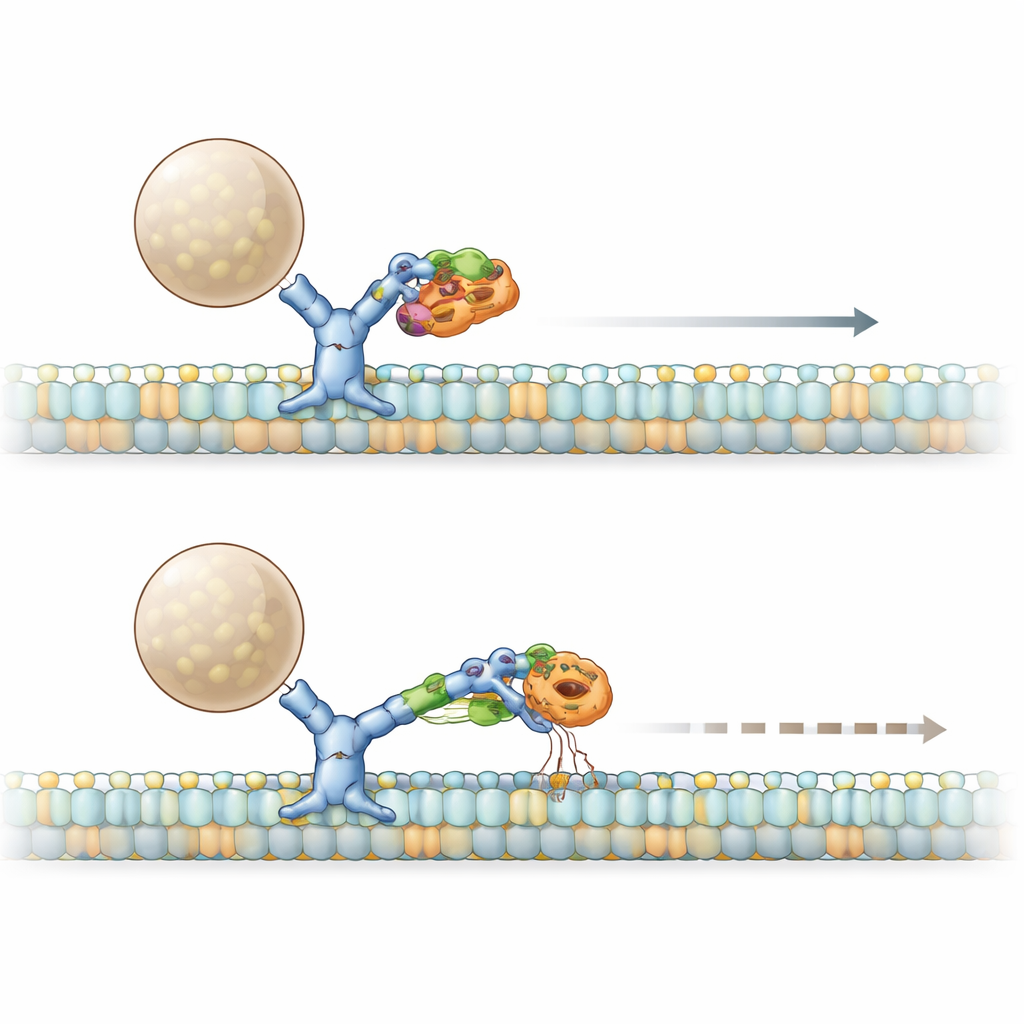
Come un’alleanza di tre proteine inceppa il motore
La storia si complica con due attori aggiuntivi: HDAC6 e un adattatore chiamato BICD2, che aiuta ad assemblare complessi dineinici attivi. La PACS1 mutata non solo aumenta l’attività di HDAC6, riducendo l’acetilazione sui microtubuli, ma forma anche un complesso ingrandito con HDAC6 e BICD2. Test biochimici hanno rivelato che, insieme, la PACS1 mutata e HDAC6 sottraggono BICD2 dalla dineina lasciando intatta la sua associazione con un motore diretto in avanti (chinesina). Nelle cellule vive, un cargo artificiale che normalmente scorre velocemente grazie alla dineina rallentava e meno carichi si muovevano quando era presente la PACS1 mutata. Bloccare l’attività di HDAC6 ha ripristinato sia la velocità sia il numero di particelle in movimento, mostrando che l’assemblaggio PACS1 mutata–HDAC6–BICD2 agisce come un freno sulla capacità della dineina di avviare e sostenere il trasporto.
Ripristinare il traffico con un aiuto naturale della dineina
I ricercatori hanno poi testato se la dineina potesse essere "riattivata" nonostante il complesso mutato. Si sono rivolti a Lis1, un noto fattore che aiuta la dineina stabilizzando gli assemblaggi motori attivi. Nelle cellule dei pazienti, i livelli di Lis1 erano leggermente ridotti. Quando il gruppo ha aggiunto Lis1 in eccesso, due aspetti sono migliorati: il Golgi si è ricompattato vicino al centro cellulare e i lisosomi, un’altra classe di organelli che si erano spostati verso l’esterno, sono tornati al loro posto. Nel medesimo saggio di motilità, Lis1 ha aumentato sia la frequenza sia la velocità del movimento dei carichi guidati dalla dineina in presenza della PACS1 mutata. Questi risultati mostrano che il problema non è l’assenza di dineina, ma il suo intrappolamento in uno stato poco attivo — uno stato che può essere parzialmente corretto sia attenuando HDAC6 sia rafforzando l’attivazione della dineina.
Collegare una sindrome rara a un insieme più ampio di disturbi
Combinando analisi strutturale, biologia cellulare e imaging in vivo, gli autori propongono un modello chiaro: PACS1 normalmente collega carichi selezionati alla dineina e affina le prestazioni del motore tramite HDAC6 e l’acetilazione dei microtubuli. La mutazione R203W apre la superficie di interazione di PACS1, reclutando eccessivamente HDAC6 e BICD2 in un complesso che compromette la capacità della dineina di agganciare i microtubuli e muoversi con efficienza. Il risultato è un ampio malposizionamento di Golgi, lisosomi e altri carichi, in particolare nei neuroni dove il trasporto a lunga distanza è vitale. Questo meccanismo aiuta a spiegare perché abbassare PACS1 o HDAC6 con terapie antisenso corregge i difetti cerebrali nei modelli murini ed è ora in fase di esplorazione nei pazienti. Più in generale, colloca la sindrome PACS1 nello spettro crescente dei disturbi del traffico sui microtubuli, insieme a condizioni causate da mutazioni in dineina, BICD2 e fattori di trasporto correlati.
Citazione: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Parole chiave: Sindrome PACS1, trasporto della dineina, traffico sui microtubuli, organizzazione del Golgi, sviluppo neuronale