Clear Sky Science · it
La proteina secretoria, CLCF1, migliora la colestasi epatica inibendo la sintesi epatica degli acidi biliari e favorendone l’escrezione
Perché questa ricerca è importante per la salute del fegato
Le malattie epatiche colestatiche sono condizioni in cui la bile, un fluido digestivo prodotto dal fegato, non fluisce correttamente e si accumula, avvelenando progressivamente il fegato dall’interno. I farmaci attuali aiutano solo una parte dei pazienti e molti finiscono per necessitare un trapianto di fegato. Questo studio identifica una proteina prodotta naturalmente, chiamata CLCF1, che l’organismo sembra attivare come sistema di difesa durante la colestasi. Capire come funziona questa proteina potrebbe indicare nuove terapie che proteggono il fegato riducendo la produzione di componenti biliari dannosi e facilitandone l’eliminazione.
Un aiuto nascosto nei fegati malati
I ricercatori hanno iniziato esaminando tessuto epatico di pazienti con colangite biliare primitiva e colangite sclerosante primitiva, due forme principali di malattia epatica colestatica cronica. Hanno confrontato persone con malattia in fase iniziale e con colestasi più avanzata, e hanno anche analizzato dataset genici pubblici esistenti. Tra queste fonti umane indipendenti, una proteina secreta è emersa in modo consistente: CLCF1 risultava tra i geni maggiormente aumentati nei fegati colestatici. Livelli più elevati di CLCF1 correlavano con peggiori marker ematici di gravità della malattia, suggerendo che il fegato aumenta la produzione di questa proteina man mano che lo stress e l’accumulo di bile peggiorano. Nei pazienti in fase iniziale trattati con il farmaco standard acido ursodesossicolico, chi rispondeva bene tendeva ad avere più CLCF1 nel fegato, insinuando che questa proteina possa identificare un fegato più adattabile e sensibile al trattamento.
Testare CLCF1 in modelli animali
Per andare oltre le correlazioni umane, il gruppo ha usato topi e ha impiegato sia strategie genetiche sia dietetiche per imitare la colestasi epatica. In due diversi modelli murini, la colestasi aumentava fortemente la produzione epatica di Clcf1, rispecchiando i risultati umani. Quando gli scienziati hanno rimosso specificamente il recettore di CLCF1 dalle cellule epatiche, il danno colestatico è peggiorato notevolmente: i dotti biliari crescevano eccessivamente, il tessuto epatico andava in necrosi, l’infiammazione aumentava, si accumulava tessuto cicatriziale e gli acidi biliari tossici si accumulavano. L’esperimento inverso ha dato risultati più incoraggianti. Quando il team ha usato un virus innocuo per aumentare i livelli di Clcf1 solo nel fegato, i topi sono stati protetti. I loro fegati apparivano più sani, gli esami del sangue miglioravano, la fibrosi si riduceva e la quantità di acidi biliari intrappolati nel fegato calava in modo marcato.
Chiudere il rubinetto e aprire lo scarico
Come fa CLCF1 a ridurre così efficacemente la sovraccarica di acidi biliari? I ricercatori hanno individuato due azioni complementari. Primo, CLCF1 ha calmato direttamente la macchina epatica di produzione della bile. In più modelli murini e in cellule epatiche in coltura, CLCF1 in eccesso ha spento in modo consistente enzimi chiave che convertono il colesterolo in acidi biliari, riducendo la produzione di nuova bile. Questo avveniva senza attivare il solito regolatore nucleare epatico della bile, il recettore FXR, il che suggerisce che CLCF1 utilizza una via alternativa all’interno delle cellule epatiche per rallentare la sintesi degli acidi biliari. Secondo, CLCF1 ha influenzato la gestione della bile più a valle nell’organismo. Ha rimodellato la comunità microbica intestinale verso batteri particolarmente abili nella trasformazione degli acidi biliari e ha aumentato la quantità di acidi biliari eliminati con le feci, funzionando come uno scarico più efficiente.
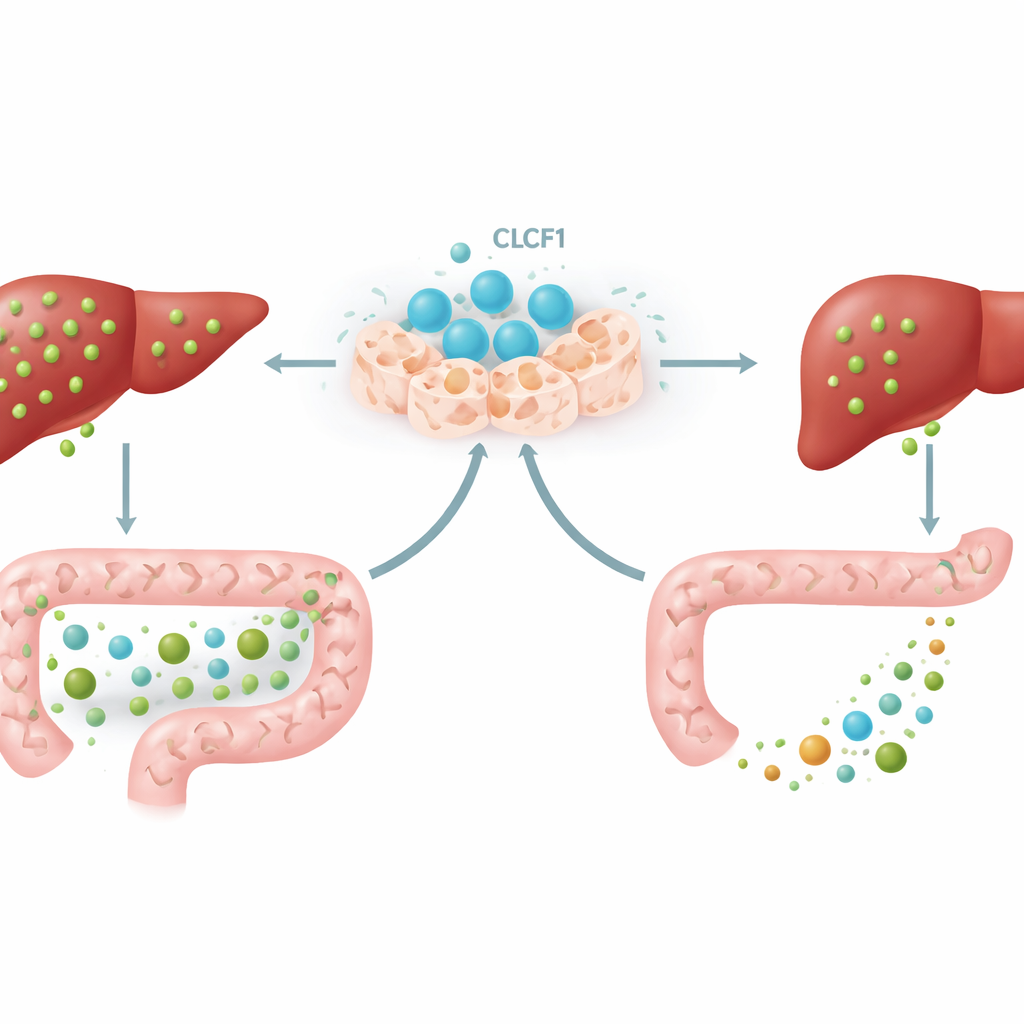
La conversazione intestino–fegato
Un pezzo chiave del puzzle coinvolgeva un circuito di segnalazione tra intestino e fegato. Alcuni acidi biliari nell’intestino attivano un sensore chiamato FXR nelle cellule intestinali, che poi rilasciano un ormone messaggero noto come FGF15 nei topi. Questo ormone viaggia nel sangue fino al fegato e gli comunica di rallentare la produzione di acidi biliari. Con CLCF1 in eccesso, i topi accumulavano specifici tipi di acidi biliari nell’intestino—in particolare forme note per essere forti attivatori di FXR. Di conseguenza, l’FXR intestinale si accendeva, i livelli di FGF15 aumentavano sia nell’intestino sia nel fegato e il fegato riduceva ulteriormente la produzione di acidi biliari. Quando gli scienziati bloccarono l’FXR intestinale con un farmaco limitato all’intestino, gran parte dell’effetto protettivo di CLCF1 svanì, dimostrando che questa conversazione intestino–fegato è una componente essenziale dell’azione della proteina.
Cosa potrebbe significare per terapie future
Nel complesso, questi risultati dipingono CLCF1 come una valvola di sicurezza integrata per la malattia epatica colestatica. La proteina riduce i livelli di acidi biliari da entrambi i lati: rallenta la loro produzione all’interno del fegato e ne favorisce l’eliminazione attraverso l’intestino, aiutata da microbi intestinali benefici e da un segnale ormonale di feedback. A differenza dei farmaci esistenti che attivano l’FXR in tutto l’organismo e possono causare effetti collaterali come prurito e alterazioni dei lipidi nel sangue, CLCF1 sembra modulare il controllo della bile in modo più delicato e selettivo, specialmente attraverso l’intestino. Pur essendo ancora lavoro su modelli animali e campioni di laboratorio, lo studio suggerisce che potenziare CLCF1 o imitare le sue vie potrebbe costituire la base di nuove terapie—e che misurare questa proteina, o gli acidi biliari che favorisce nell’intestino, potrebbe aiutare a identificare i pazienti che ne trarrebbero maggior beneficio.
Citazione: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Parole chiave: malattia epatica colestatica, acidi biliari, asse intestino–fegato, CLCF1, microbiota intestinale