Clear Sky Science · it
Il sistema di secrezione di tipo VI di Acinetobacter: meccanismi, biologia e potenziale terapeutico
Armi nascoste nei germi ospedalieri
Molti sanno che alcuni germi ospedalieri possono resistere agli antibiotici, ma in pochi si rendono conto che questi microrganismi combattono anche battaglie feroci tra loro. Questa rassegna esamina una sorta di “lancia a molla” microscopica all’interno di Acinetobacter, un gruppo di batteri che comprende il temuto patogeno ospedaliero Acinetobacter baumannii. Capire come funziona quest’arma incorporata, quando viene attivata e come favorisce l’insediamento delle infezioni potrebbe aprire nuove strade per diagnosticare e disinnescare infezioni letali e resistenti ai farmaci.
Una macchina per sopravvivere, non solo un dardo velenoso
Le specie di Acinetobacter vivono nel suolo, nell’acqua e sulla nostra pelle, ma alcune sono diventate patogeni ospedalieri di grande successo. Uno strumento chiave del loro arsenale è il sistema di secrezione di tipo VI, o T6SS, una minuscola macchina contrattilе ancorata all’involucro cellulare. Quando viene attivata, spara un picco simile a un ago carico di proteine tossiche nelle cellule vicine, uccidendo spesso i batteri concorrenti al contatto. A differenza di altri germi che possono avere diverse versioni di questo sistema, gli Acinetobacter patogeni di solito possiedono un solo T6SS, eppure hanno riconfigurato questa piattaforma unica per servire a molti scopi, dal respingere rivali al modellare le infezioni.
Hardware ricostruito: una piattaforma di lancio insolita
La maggior parte dei batteri costruisce il proprio T6SS attorno a un set standard di componenti, ma Acinetobacter ha rimodellato diverse parti chiave. Gli manca un comune ancoraggio della membrana esterna chiamato TssJ e invece si affida a un trio di helper specializzati: TsmK forma una base nella membrana interna, TslA stabilizza una lunga proteina “tunnel” (TssM) mentre attraversa la parete cellulare, e TagX taglia localmente la parete per fare spazio all’arma. Inoltre, una particolare proteina della punta, VgrG1, deve avere una forma quasi perfetta perché il sistema possa sparare — singole sostituzioni di aminoacidi possono disattivarla. Insieme, questi adattamenti mostrano come l’evoluzione possa sostituire parti mancanti con nuove soluzioni pur preservando il principio di funzionamento di base.
Controlli intelligenti: quando ha senso la modalità attacco
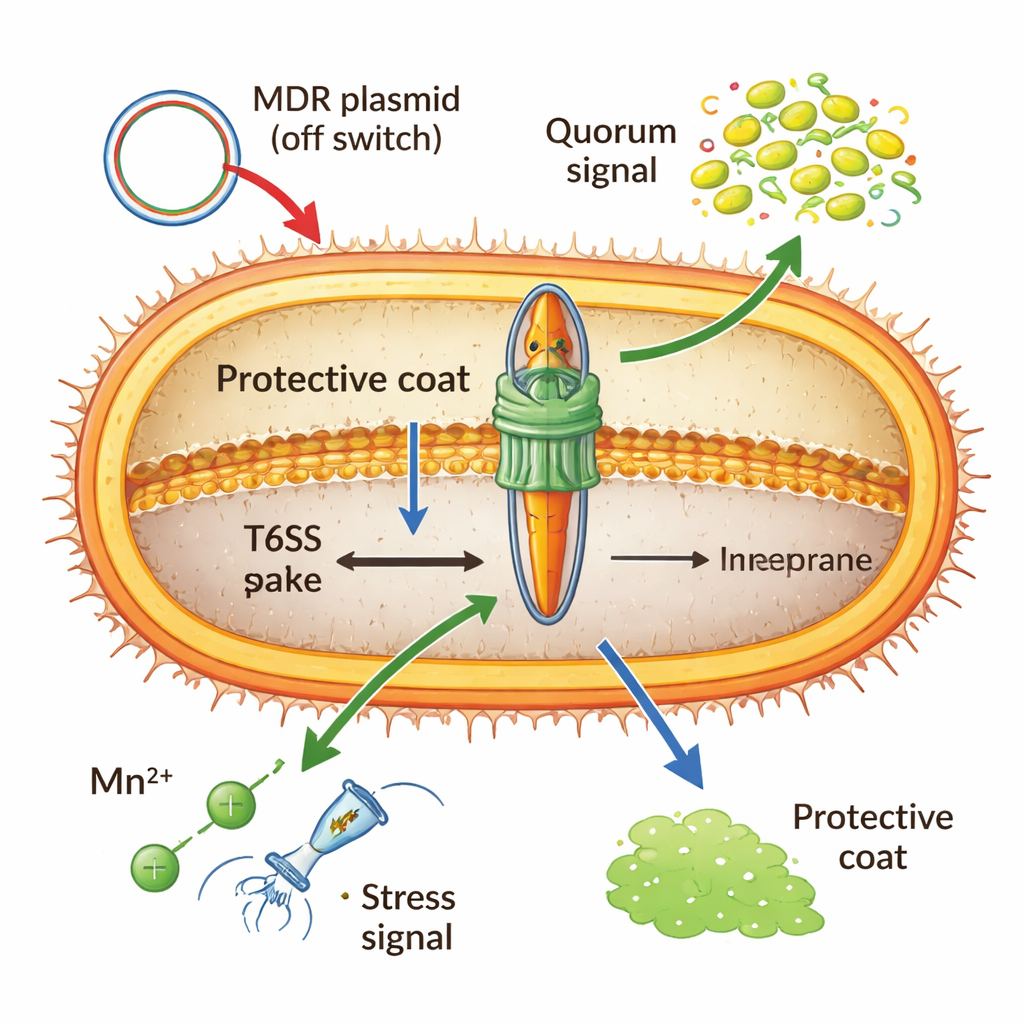
Costruire e azionare questa nanomacchina è dispendioso, quindi Acinetobacter la mantiene sotto stretto controllo. Una proteina globale legante il DNA (H‑NS) e repressori speciali portati su plasmidi multiresistenti possono bloccare il sistema in posizione “spenta”, soprattutto quando i geni della resistenza vengono condivisi tra cellule. A densità cellulare elevata, segnali chimici di “quorum” possono attivarlo, preparando i batteri alla competizione a distanza ravvicinata. Anche gli ioni metallici giocano un ruolo: sotto stress ossidativo, il manganese importato attiva un piccolo RNA che provoca la distruzione di messaggi chiave del T6SS, attenuando l’arma per favorire la sopravvivenza all’interno dell’ospite. Perfino la capsula — un rivestimento esterno zuccherino — agisce sia da scudo sia da freno, bloccando attacchi in arrivo ma anche smorzando fisicamente il lancio dell’Acinetobacter stesso.
Un kit diversificato di colpi microscopici
Quando Acinetobacter preme il grilletto, può erogare una vasta gamma di tossine. Alcuni enzimi degradano la robusta parete cellulare dei rivali; altri erodono silenziosamente le membrane cellulari, e altri ancora tagliano il DNA all’interno delle cellule bersaglio. Ogni tossina è accoppiata con una proteina di “immunità” corrispondente che protegge l’attaccante dal fuoco amico. Una tossina che taglia il DNA, ora chiamata TafE, può persino uccidere funghi, suggerendo schermaglie interregnali in ambienti come intestino o polmoni. Studi genomici indicano che Acinetobacter codifica molte altre tossine ancora non caratterizzate, spesso inglobate in grandi proteine Rhs che agiscono come vettori modulari. Piuttosto che affidarsi a un singolo colpo, questi batteri sembrano usare attacchi stratificati che danneggiano contemporaneamente diverse strutture essenziali.
Modellare infezioni, geni e trattamenti futuri
Prove da isolati clinici e modelli animali suggeriscono che un T6SS attivo spesso è associato a malattie più gravi, infiammazione più intensa e migliore sopravvivenza dei batteri all’interno dell’ospite. Uccidendo i microrganismi vicini, il sistema rilascia anche DNA che le cellule di Acinetobacter naturalmente competenti possono assorbire, accelerando la diffusione di caratteristiche come la resistenza agli antibiotici. Tuttavia mantenere l’arma costantemente attiva è oneroso, quindi molti ceppi ospedalieri di successo portano plasmidi o mutazioni che la silenziano una volta assicurata la resistenza. Nel complesso, gli autori sostengono che questo sistema di secrezione non debba essere visto come un semplice fattore di virulenza ma come un “modulo di fitness” flessibile che Acinetobacter regola per bilanciare aggressività, persistenza e consumo energetico. Questa nuova prospettiva indica applicazioni pratiche, da vaccini che mirano a parti conservate del T6SS a farmaci che inceppano selettivamente il meccanismo di sparo, aiutando i medici a battere un nemico ospedaliero pericoloso e adattabile.
Citazione: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Parole chiave: Acinetobacter, sistema di secrezione di tipo VI, resistenza agli antibiotici, competizione batterica, infezioni ospedaliere