Clear Sky Science · it
Ottimizzare la precisione del CRISPR negli embrioni di topo tramite targeting dominante mediato da microomologie
Perché è importante ottenere topi geneticamente modificati più precisi
Strumenti di editing genetico come il CRISPR hanno reso sorprendentemente semplice creare topi che riproducono malattie umane, ma esiste un problema nascosto: le variazioni genetiche nella primissima generazione di animali sono spesso disordinate e miste. Ciò rallenta gli esperimenti, riduce l’affidabilità e richiede più animali. Questo studio presenta un metodo per indirizzare i tagli del CRISPR negli embrioni di topo verso esiti altamente prevedibili, così che la maggior parte dei topi fondatori nasca con la stessa mutazione ben definita—portando una biologia più pulita e una maggiore eticità nella ricerca sull’editing genetico.
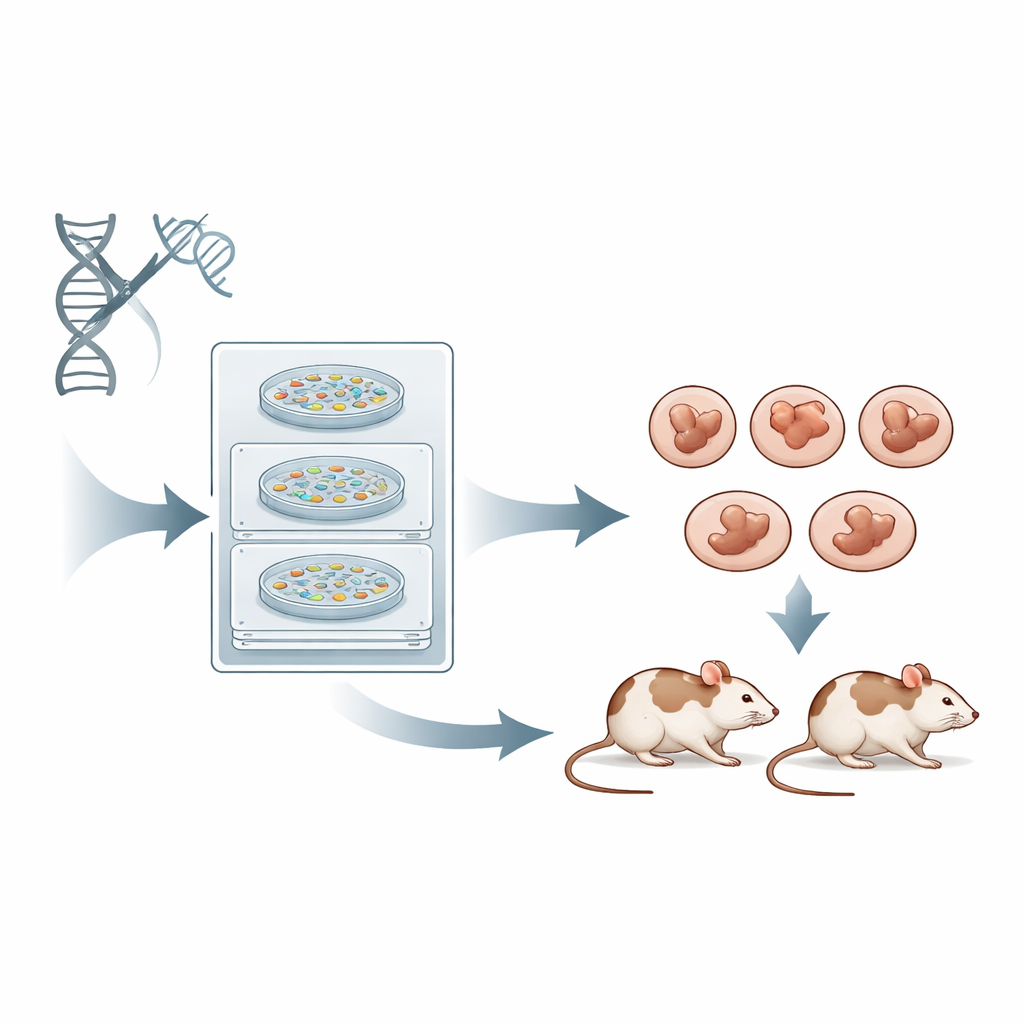
La sfida delle riparazioni del DNA disordinate
Quando il CRISPR taglia il DNA, la cellula deve riparare la rottura utilizzando i propri sistemi di riparazione. La via più comune, detta non-homologous end joining, è rapida ma imprecisa, producendo un insieme confuso di piccole inserzioni e delezioni nel sito di taglio. Un’altra via, la microhomology-mediated end joining, tende a rimuovere porzioni di DNA in modi stereotipati usando brevi sequenze corrispondenti come guida. Entrambe sono molto più efficienti della via precisa ma lenta chiamata homology-directed repair. Negli esperimenti CRISPR standard, gli scienziati si concentrano soprattutto su quanto efficacemente una guida taglia e su quanti siti off-target colpisce, prestando molta meno attenzione a quale via di riparazione sarà favorita o quale mutazione esatta risulterà. Il risultato è che molti topi fondatori portano un mosaico di mutazioni diverse in cellule differenti, costringendo i ricercatori ad allevare la generazione successiva prima di poter lavorare con un genotipo pulito e uniforme.
Un modo più intelligente di scegliere le guide CRISPR
Gli autori hanno cercato di ribaltare questa situazione progettando guide non solo per efficacia e sicurezza, ma anche per prevedibilità. Hanno iniziato con inDelphi, uno strumento di machine learning addestrato su ampi dataset di mutazioni indotte da CRISPR in cellule in coltura. inDelphi non si limita a indicare con quale frequenza un sito verrà editato; predice l’intero menu di possibili inserzioni e delezioni e la frequenza con cui ciascuna comparirà, con attenzione particolare agli eventi guidati da microomologie. Il gruppo ha scandagliato il gene della tirosinasi (Tyr) nel topo, la cui perdita di funzione rende gli animali albini, e ha selezionato guide RNA previste favorire delezioni mediate da microomologie forti e ripetibili mantenendo basso il rischio off-target. Hanno quindi editato embrioni di topo e misurato le mutazioni risultanti con sequenziamento profondo. In generale, il genotipo preferito da inDelphi per ciascuna guida è apparso in frequenze simili negli embrioni come previsto, e le guide con caratteristiche di microomologia più forti hanno effettivamente prodotto pattern di mutazione più uniformi.
Usare le cellule staminali come fase di prova
Tuttavia la previsione da sola non è stata sufficiente. Quando il team ha confrontato le previsioni di inDelphi con i pattern reali di editing, ha trovato solo un accordo moderato. Per colmare questo divario, hanno introdotto un passaggio intermedio pratico: testare ciascuna guida in cellule staminali embrionali di topo che condividono molte caratteristiche con gli embrioni molto precoci. Dopo aver trasfettato queste cellule con componenti CRISPR, hanno isolato le cellule editate e sequenziato i siti bersaglio. I pattern di mutazione nelle cellule staminali corrispondevano a quelli negli embrioni molto più da vicino rispetto al modello computazionale. Le guide che producevano una singola delezione dominante nelle cellule staminali tipicamente facevano lo stesso nei blastocisti e negli embrioni in stadio più avanzato. Combinando il ranking di inDelphi con questa “prova generale” sulle cellule staminali, i ricercatori sono stati in grado di scegliere in modo affidabile guide che promuovono la riparazione mediata da microomologie e minimizzano la diversità degli alleli mutanti.
Dalla colorazione degli occhi agli arti mancanti
Gli autori hanno messo alla prova la loro pipeline su animali viventi. Per il gene Tyr hanno scelto tre guide che rappresentavano precisione prevista alta, media e bassa e hanno trasferito embrioni editati in madri affidatarie. All’undicesimo giorno e mezzo di sviluppo hanno esaminato la pigmentazione degli occhi e sequenziato ogni embrione singolarmente. La guida che favoriva fortemente le microomologie ha prodotto embrioni per lo più albini e portatori di una delezione dominante di piccole dimensioni, spesso in entrambe le copie del gene, con pochissima variabilità. Una guida meno ottimizzata ha prodotto un mix di perdita di pigmentazione e pigmentazione parziale legata a un set più complesso di mutazioni. Hanno quindi applicato lo stesso approccio al gene Fgf10, la cui perdita di funzione dà embrioni privi di arti. Selezionando una guida prevista—e confermata nelle cellule staminali—per generare una specifica delezione di quattro basi con alta probabilità di interrompere il gene, hanno ottenuto embrioni al giorno 15.5 uniformemente senza arti e portatori di un set fortemente arricchito delle delezioni attese. Per entrambi i geni, gli stessi pochi tipi di mutazione hanno dominato nelle previsioni di inDelphi, nelle cellule staminali, negli embrioni precoci e negli embrioni in stadi successivi.
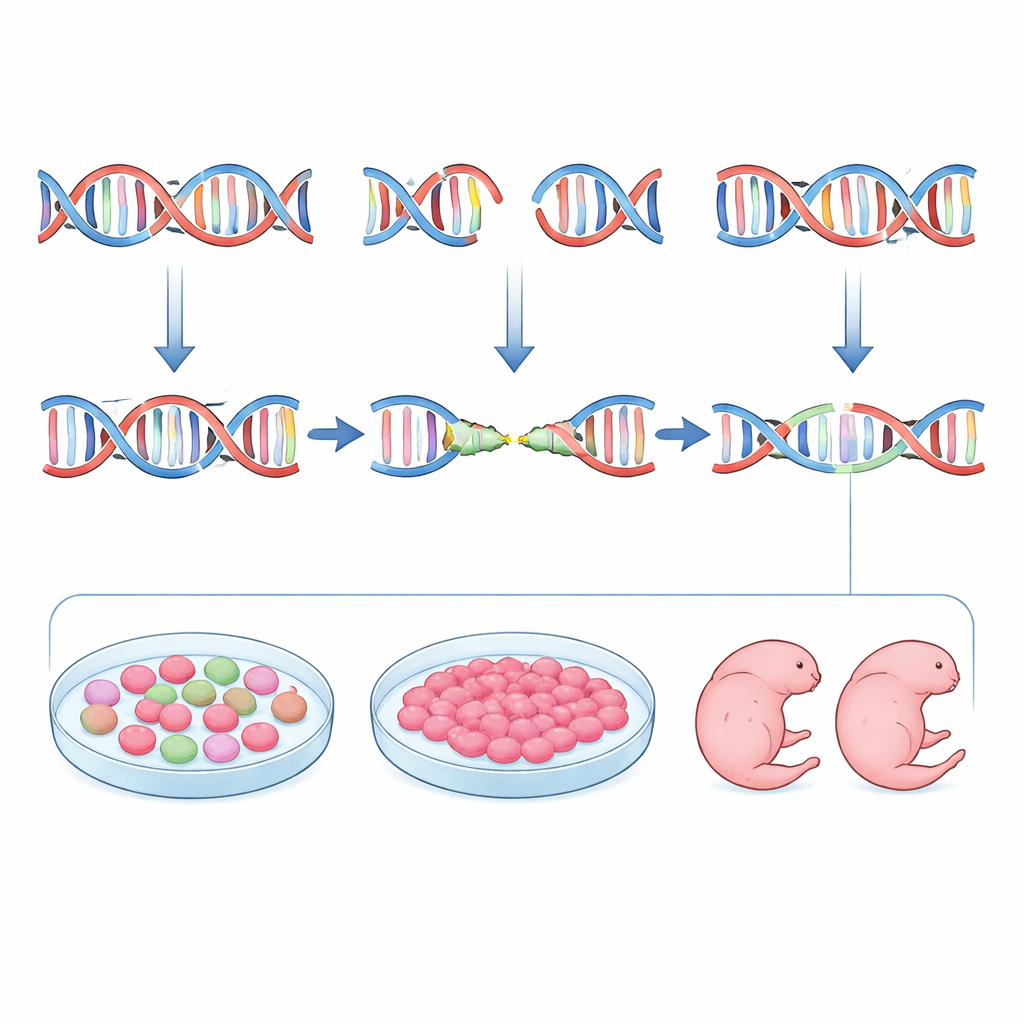
Genetica più pulita con meno animali
In termini pratici, lo studio offre un nuovo modello per progettare esperimenti CRISPR nei topi. Invece di passare frettolosamente da una guida progettata al computer all’editing degli embrioni, gli autori propongono una pipeline integrata: usare inDelphi e strumenti per gli off-target per scegliere guide che probabilmente favoriscono delezioni mediate da microomologie e frameshift, testare queste guide in cellule staminali embrionali per confermare sia l’efficienza sia l’uniformità delle mutazioni, e avanzare in embrioni solo le migliori. Questa strategia produce topi fondatori le cui cellule condividono in modo schiacciante la stessa mutazione ben caratterizzata, rendendoli immediatamente utili per modellare malattie umane—soprattutto quelle causate da mutazioni ricorrenti di tipo delezione—riducendo al contempo il numero di animali da allevare e analizzare. Il risultato è una genetica più precisa e riproducibile e un percorso più etico verso potenti modelli di malattia.
Citazione: Lkhagvadorj, K., Okamura, E., Taki, T. et al. Optimizing CRISPR precision in mouse embryos via microhomology-mediated end joining-dominant targeting. Commun Biol 9, 371 (2026). https://doi.org/10.1038/s42003-026-09771-z
Parole chiave: CRISPR, modelli murini, editing del genoma, riparazione del DNA, modellizzazione delle malattie