Clear Sky Science · it
Glicosilazione come regolatore dinamico delle vie di segnalazione immunitaria innata RLR e cGAS-STING
Come i marcatori zuccherini aiutano le cellule a percepire i virus
Le nostre cellule sono costantemente in guardia contro i virus invasori e gran parte di questa difesa dipende da piccoli marcatori zuccherini attaccati alle proteine. Questa recensione spiega come questi marcatori, noti come glicosilazione, funzionino più come dimmer che come semplici interruttori on/off per vie antivirali chiave. Comprendere questo fine-tuning basato sugli zuccheri potrebbe aprire nuove strade per potenziare i vaccini, trattare le infezioni virali e persino sfruttare il sistema immunitario contro il cancro.
Il primo allarme della cellula
Quando i virus entrano in una cellula, lasciano dietro di sé filamenti di RNA o DNA riconoscibili. Sistemi specializzati di “allarme” pattugliano l’interno della cellula in cerca di questi detriti genetici. Un sistema, chiamato via dei recettori RIG-I-like (RLR), rileva l’RNA virale. Un altro, noto come via cGAS–STING, percepisce il DNA che compare nel posto sbagliato all’interno della cellula. Una volta attivate, entrambe le vie avviano cascate chimiche che si concludono con il rilascio di interferoni di tipo I e molecole infiammatorie—segnali potenti che avvertono le cellule vicine e mobilitano le difese immunitarie. Poiché una risposta eccessiva o insufficiente può essere pericolosa, la cellula deve sintonizzare con cura questi allarmi, e la glicosilazione è uno dei modi principali per farlo. 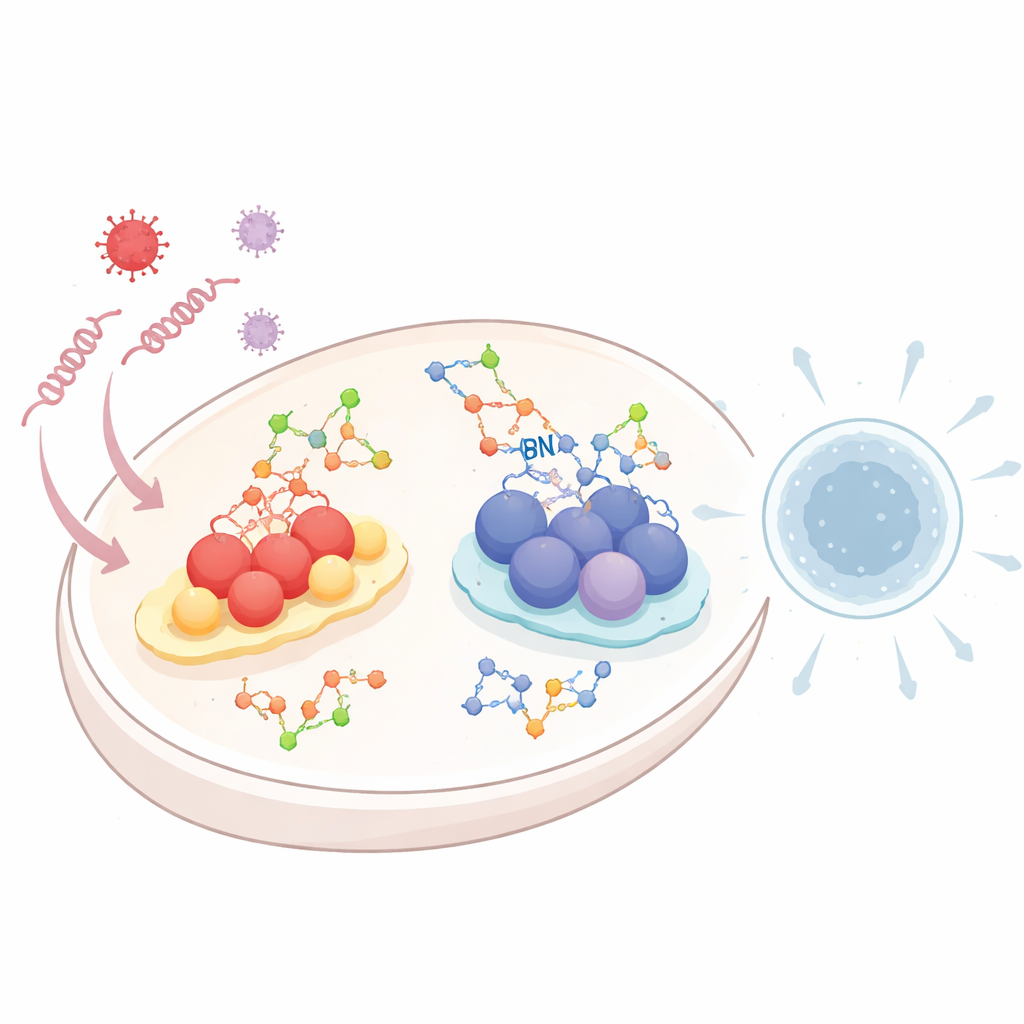
I rivestimenti zuccherini come controlli di precisione
La glicosilazione aggiunge piccole unità zuccherine alle proteine in diverse localizzazioni cellulari. Nella rete di trasporto interna della cellula, il reticolo endoplasmatico e il Golgi, catene zuccherine N-legate ingombranti aiutano le proteine a ripiegarsi correttamente, a restare stabili e a raggiungere la membrana giusta. Al contrario, una forma più snella chiamata O-GlcNAcylation pone un singolo zucchero sulle proteine nel citoplasma e nel nucleo. Questo marcatore minimalista è altamente dinamico, con un rapido turnover controllato da due enzimi che lo aggiungono o lo rimuovono in risposta ai livelli di nutrienti e allo stress. La recensione descrive come questi diversi tipi di zuccheri non si limitino ad accendere o spegnere i sensori immunitari; piuttosto, ne modulano la facilità con cui si aggregano, la loro durata e l’intensità del segnale. In questo modo, la glicosilazione collega lo stato metabolico della cellula alla sua prontezza a combattere le infezioni.
Regolazione della via sensoriale dell’RNA
Nell’ambito del sistema RLR che riconosce l’RNA, una proteina di relay centrale chiamata MAVS si trova sui mitocondri e funge da hub chiave. La recensione mostra che l’O-GlcNAcylation di MAVS può sia accelerare sia frenare la segnalazione antivirale, a seconda del sito di attacco dello zucchero. I marcatori zuccherini in particolari posizioni favoriscono ulteriori decorazioni proteiche, come un tipo specifico di catena di ubiquitina, che aiutano MAVS a formare grandi aggregati di segnalazione e a promuovere una forte produzione di interferoni contro i virus a RNA. Altri siti zuccherini mantengono MAVS disperso e inattivo in condizioni normali, prevenendo infiammazioni inutili. L’infezione virale e i cambiamenti nel percorso metabolico di produzione degli zuccheri della cellula possono spostare l’equilibrio tra questi marcatori attivanti e inibitori. Modifiche correlate su un altro fattore, IRF5, possono spingere il sistema immunitario verso pericolose “tempeste di citochine”, evidenziando che più zuccheri non sono sempre meglio. Parallelamente, i virus possono sfruttare gli zuccheri N-legati sulle proteine di superficie cellulare, come il recettore del fattore di crescita EGFR, per marcare sensori a monte come RIG-I per la degradazione, attenuando le difese antivirali.
Regolazione della via sensoriale del DNA
Anche la via cGAS–STING che riconosce il DNA è fortemente plasmata dalla glicosilazione. STING, una proteina di membrana nel reticolo endoplasmatico, necessita di catene zuccherine N-legate per ripiegarsi correttamente, restare stabile e assemblarsi in aggregati di segnalazione una volta attivata da messaggeri derivati dal DNA. Senza questi zuccheri, STING non riesce a formare le strutture di ordine superiore e a trafficarе attraverso i compartimenti cellulari necessari per un robusto rilascio di interferoni. Allo stesso tempo, l’O-GlcNAcylation di STING in un sito particolare potenzia un diverso insieme di marcatori chimici che ne favoriscono l’aggregazione e il movimento, amplificando i segnali antivirali contro i virus a DNA. Catene zuccherine chiamate glicosaminoglicani solfati, costruite nel Golgi, assistono ulteriormente aiutando STING attivato a polimerizzare in lunghe strutture che reclutano enzimi a valle. I virus controbatttono alterando le proprie glicoproteine o attivando vie di degradazione che prendono di mira STING, spesso negli stessi spazi cellulari in cui queste decorazioni zuccherine vengono aggiunte o elaborate. 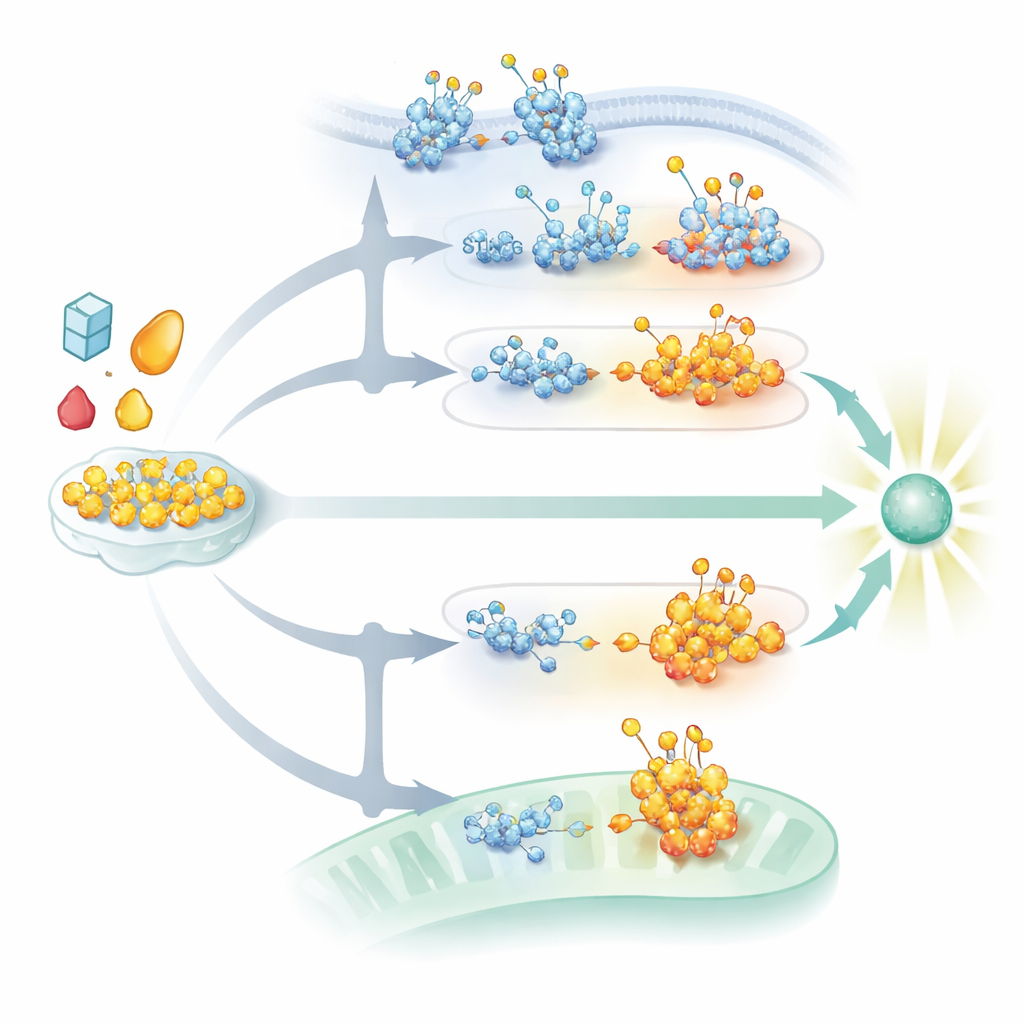
Metabolismo, malattie e terapie future
Poiché il principale donatore di zucchero per l’O-GlcNAcylation è prodotto da una via metabolica nota come percorso biosintetico delle esosoamine, i cambiamenti nell’uso dei nutrienti modellano direttamente la segnalazione antivirale. Molti virus pilotano questa via a loro vantaggio, mentre l’aumento sperimentale o il blocco del flusso delle esosoamine può rafforzare o indebolire le risposte antivirali nei modelli animali. La recensione collega questi meccanismi alle malattie umane: i tumori riscrivono frequentemente la glicosilazione per attenuare la segnalazione degli interferoni ed eludere l’attacco immunitario, mentre lo stress metabolico cronico o difetti ereditari nell’elaborazione dei glicani possono spostare l’equilibrio verso autoimmunità dannosa. Gli autori sostengono che gli enzimi che controllano la glicosilazione—soprattutto quelli che aggiungono o rimuovono O-GlcNAc o costruiscono strutture N-legati chiave—sono bersagli farmacologici promettenti ma sfidanti. Le terapie future probabilmente dovranno agire in modo sito-specifico e contestuale, spingendo il “glico-codice” verso una migliore protezione contro infezioni, cancro e disturbi infiammatori senza innescare nuove forme di squilibrio immunitario.
Il quadro generale per la salute quotidiana
In termini quotidiani, questo articolo rivela che gli allarmi antivirali di prima linea del corpo non operano in isolamento—sono collegati all’uso di energia della cellula e alla sua chimica degli zuccheri. Piccoli marcatori zuccherini su una manciata di proteine critiche decidono se un genoma virale vagante scateni un avvertimento misurato, una difesa totale o una reazione eccessiva pericolosa. Decodificando e imparando infine a regolare questo sistema di controllo basato sugli zuccheri, i ricercatori sperano di progettare trattamenti che rendano i vaccini più efficaci, aiutino a eliminare infezioni ostinate, rendano i tumori visibili al sistema immunitario e calmino l’infiammazione incontrollata nelle malattie autoimmuni.
Citazione: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Parole chiave: immunità innata, glicosilazione, via RLR, cGAS-STING, O-GlcNAcylation