Clear Sky Science · it
Approfondimenti strutturali sulla macchina dei pili di tipo IV di Thermus thermophilus che assembla due pili distinti
Piccoli peli batterici con grandi compiti
I batteri possono essere microscopici, ma molti sono dotati di notevoli “peli” di superficie che permettono loro di muoversi, aderire a superfici e perfino catturare DNA disperso nell’ambiente. In questo studio, i ricercatori esaminano come un batterio amante del calore, Thermus thermophilus, costruisca e faccia funzionare una sofisticata nanomacchina che spinge questi peli — chiamati pili — attraverso l’involucro cellulare. Capire questa macchina non solo rivela come i microrganismi si adattano ed evolvono, ma offre anche ispirazione per future tecnologie a scala nanometrica e nuovi modi per neutralizzare batteri dannosi.
Due peli diversi da un’unica macchina
Thermus thermophilus produce due tipi distinti di pili: un filamento più largo e spesso e un altro più stretto e sottile. Lavori precedenti hanno mostrato che questi filamenti sono composti da mattoni diversi e verosimilmente svolgono funzioni differenti, come il movimento sulla superficie o la cattura del DNA. Tuttavia entrambi vengono costruiti dalla stessa macchina multipartita che attraversa dalla membrana interna fino a quella esterna della cellula. La domanda centrale di questo studio è come un singolo sistema possa assemblare due filamenti diversi e spingerli attraverso gli strati protettivi della cellula verso l’esterno.
Mappare l’hardware nascosto
Per scoprire come è composta la macchina, i ricercatori hanno usato la crio-tomografia elettronica, una tecnica che congela rapidamente le cellule e le fotografa in 3D a temperature molto basse. Hanno combinato questi scatti con modifiche genetiche mirate che rimuovevano o alteravano parti specifiche della macchina. Confrontando cellule normali con mutanti privi di certi componenti, hanno potuto associare le forme sfocate nelle loro mappe 3D alle proteine corrispondenti. Strumenti avanzati di predizione strutturale sono poi stati usati come progetti molecolari, aiutando a inserire questi modelli proteici nelle densità osservate e a costruire un modello ipotetico completo della macchina.
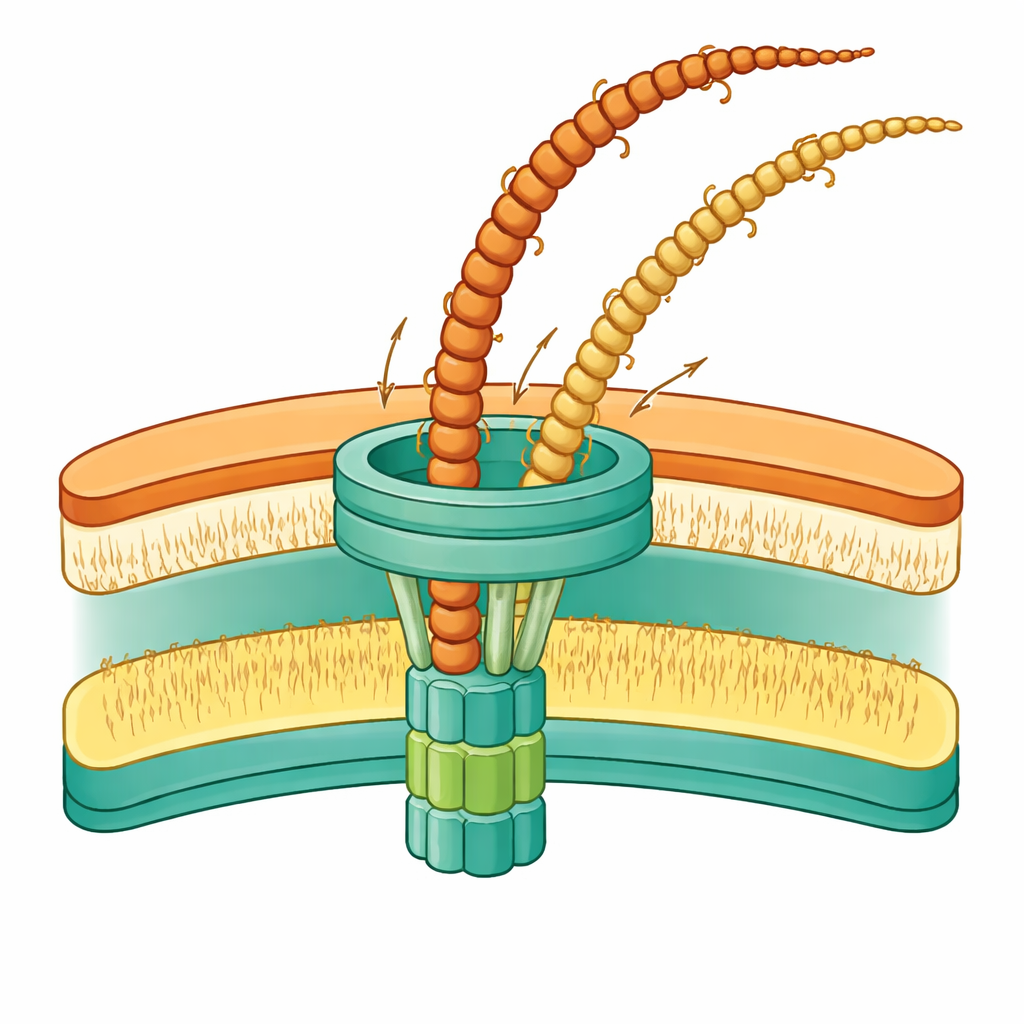
Un collegamento flessibile che tiene tutto insieme
Un risultato di rilievo riguarda una proteina chiamata PilW. Questo componente si trova tra una porta nella membrana esterna e una piattaforma interna ancorata nella membrana citoplasmatica. Quando PilW manca completamente, i pili non riescono a raggiungere l’esterno e si accumulano nello spazio tra le membrane. Quando invece viene rimosso solo un tratto di PilW, la macchina funziona ancora, ma i suoi componenti interni si spostano di posizione e le membrane circostanti si incurvano verso l’interno. Queste osservazioni suggeriscono che PilW si comporti come un tenditore flessibile che collega la porta esterna alla piattaforma interna, adattando lunghezza e forma mentre la macchina cicla tra stati di riposo e attivi. I modelli del gruppo indicano che questa flessibilità permette al sistema di affrontare il gap insolitamente ampio tra le due membrane in Thermus, pur allineando le parti a sufficienza per assemblare ed espellere i pili.
Osservare i filamenti e i loro rivestimenti zuccherini
Parallelamente all’imaging in-cellula, i ricercatori hanno anche isolato i due tipi di pilus e li hanno esaminati in maggiore dettaglio usando la crio-microscopia elettronica a particelle singole. Questo approccio a risoluzione più elevata ha rivelato l’esatta disposizione dei mattoni costitutivi e, fatto cruciale, ha permesso al team di modellare le molecole di zucchero che decorano la superficie dei filamenti. Il pilus più largo porta tre siti di attacco degli zuccheri per unità costitutiva, producendo un alone denso di carboidrati. Il pilus più stretto presenta soltanto un sito di questo tipo, ma la sua catena zuccherina si protende più lontano, facendo apparire il filamento complessivamente più grande rispetto al suo nucleo proteico. Simulazioni al computer hanno poi esplorato come questi zuccheri si pieghino e oscillino mentre il filamento attraversa la porta nella membrana esterna.
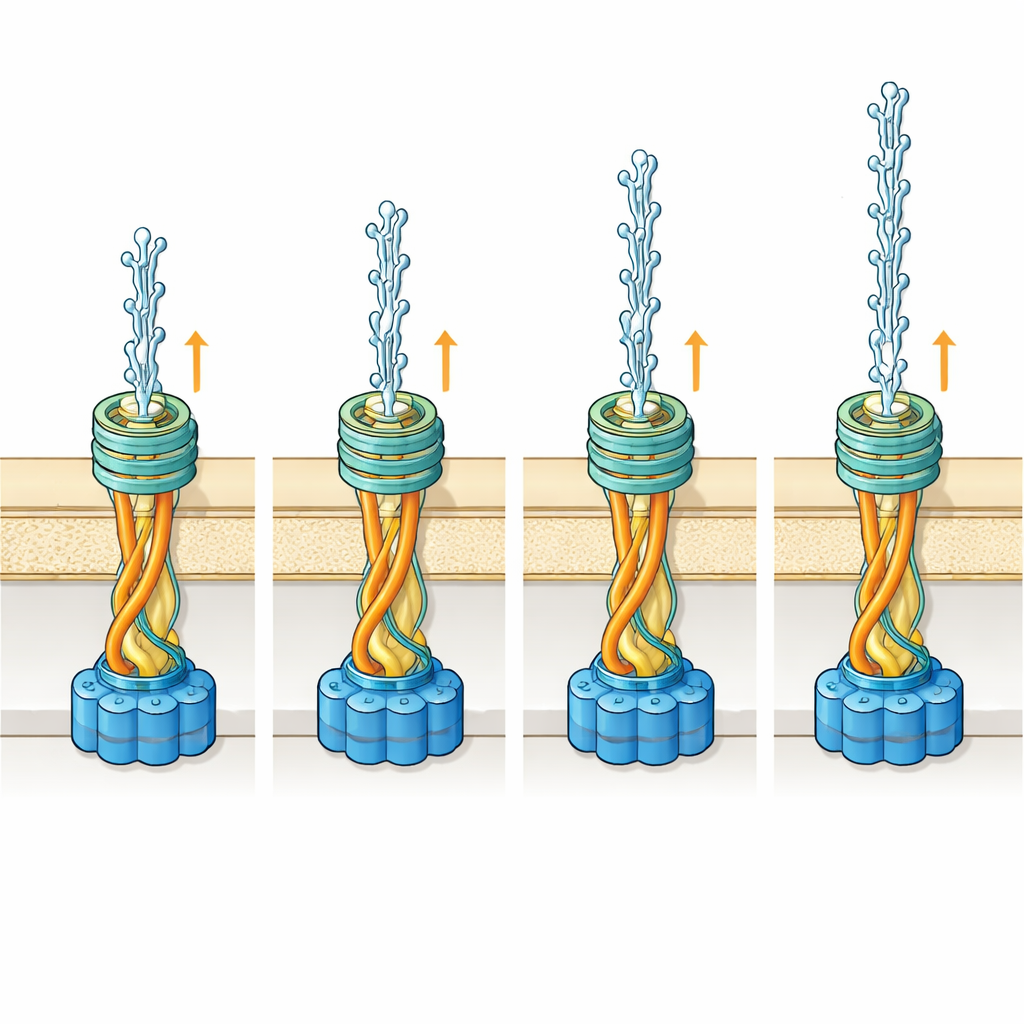
Una porta condivisa per due cavi molto diversi
Incastonando le strutture dettagliate dei pili in un modello della porta della membrana esterna, chiamata PilQ, il gruppo ha scoperto che entrambi i tipi di filamento possono, in linea di principio, scorrere attraverso la stessa apertura. Per il filamento più largo, i suoi zuccheri multipli hanno spazio sufficiente per assumere molte conformazioni mentre attraversano la porta. Per il filamento più sottile, lo spazio diventa ristretto in un punto del canale, perciò alcune conformazioni della catena zuccherina andrebbero in conflitto con le pareti. Le simulazioni suggeriscono che in questo caso la catena zuccherina probabilmente rimanga più aderente al filamento mentre è dentro la porta e si apre solo una volta all’esterno della cellula. Piuttosto che evolvere una porta più ampia e costosa per ospitare comodamente entrambi i filamenti, il batterio sembra fare affidamento sulla naturale flessibilità di queste catene zuccherine per far funzionare il sistema in modo efficiente.
Cosa significa per la vita microbica
Nel complesso, lo studio dipinge un quadro coerente di come una singola macchina adattabile costruisca ed esporti due pili molto diversi in un batterio delle sorgenti termali. Una proteina collegante flessibile sembra mantenere allineate le parti interne ed esterne mentre il motore cicla e la struttura si accorcia leggermente durante la crescita attiva del filamento. Allo stesso tempo, i rivestimenti zuccherini sui pili conferiscono protezione ed estensione, restando però sufficientemente flessibili da flettersi attraverso un canale d’uscita relativamente stretto. Per i non specialisti, il messaggio chiave è che anche microrganismi apparentemente semplici si affidano a assemblaggi mobili altamente coordinati per sopravvivere ed evolvere — dispositivi molecolari la cui eleganza ed efficienza competono, e talvolta superano, le macchine umane su scala nanometrica.
Citazione: Neuhaus, A., McLaren, M., Isupov, M.N. et al. Structural insights into the Thermus thermophilus type IV pilus machinery assembling two distinct pili. Commun Biol 9, 474 (2026). https://doi.org/10.1038/s42003-026-09762-0
Parole chiave: pili di tipo IV, nanomacchine batteriche, crio-microscopia elettronica, glicosilazione delle proteine, Thermus thermophilus