Clear Sky Science · it
Modellizzazione guidata dal tasso di crescita suggerisce che l’adattamento fenotipico guida la resistenza ai farmaci nel melanoma con mutazione BRAFV600E
Cellule tumorali che imparano a vivere con i farmaci
I farmaci mirati hanno trasformato il trattamento per molte persone affette da melanoma, un grave tumore della pelle. Eppure questi farmaci quasi sempre smettono di funzionare: i tumori che prima si riducevano ricominciano a crescere. Questo studio pone una domanda semplice ma potente: invece di fare affidamento solo sulle mutazioni genetiche, le cellule del melanoma possono “imparare” a sopravvivere al trattamento cambiando il loro comportamento—e questo apprendimento potrebbe spiegare perché alcuni modi di somministrare i farmaci funzionano meglio di altri?
Dalle cellule sensibili ai sopravvissuti
I ricercatori si sono concentrati sulle cellule di melanoma che portano una variazione comune nel gene BRAF, che le rende particolarmente sensibili a un tipo di farmaco noto come inibitore di BRAF. In esperimenti di laboratorio riportati in lavori precedenti, queste cellule sono state esposte al farmaco encorafenib a dosi diverse e per periodi di tempo differenti. Misurando con cura la velocità con cui le cellule crescevano o morivano in ciascuna condizione, gli autori hanno suddiviso le cellule in due categorie ampie: cellule naive al farmaco che non lo avevano mai incontrato e cellule adattate al farmaco che avevano vissuto in presenza del farmaco per almeno una settimana. Le cellule naive crescevano bene in assenza di trattamento ma venivano fortemente rallentate o uccise dal farmaco. Le cellule adattate, al contrario, crescevano meglio in presenza del farmaco ma perdevano quel vantaggio quando il farmaco veniva rimosso—suggerendo che la loro sopravvivenza fosse legata a un cambiamento di stato flessibile e reversibile piuttosto che a danni genetici permanenti.
Una mappa dei comportamenti cellulari nascosti
Per comprendere questi cambiamenti, il gruppo ha costruito un modello matematico in cui a ogni cellula cancerosa viene assegnato un “stato fenotipico”—una posizione astratta su una scala che va da molto sensibile al farmaco a molto resistente. Invece di assumere solo due tipi di cellule, hanno permesso molti stati intermedi, riflettendo spostamenti graduali nel comportamento osservati in marcatori biologici della resistenza. Per ogni combinazione di stato e dose del farmaco, hanno stimato un tasso di crescita netto, che poteva essere positivo (più divisioni che morti) o negativo (più morti che divisioni). Tutti questi tassi sono stati disposti in una griglia, o “matrice di fitness”, che funziona come un paesaggio: alcuni stati a certe dosi sono buoni posti in cui le cellule prosperano, altri sono letali. Le cellule nel modello possono muoversi passo a passo attraverso questo paesaggio mentre il trattamento viene acceso o spento.
Le cellule deragliano o scalano verso il vantaggio?
L’incognita chiave era come le cellule si muovono attraverso questo paesaggio. Gli autori hanno testato quattro possibili strategie. In una, le cellule non cambiano mai stato, quindi eventuali cellule resistenti devono essere presenti fin dall’inizio. In un’altra, le cellule vagano casualmente tra stati vicini, come una camminata ubriaca, indipendentemente dal fatto che la loro situazione migliori. Nelle due strategie restanti, le cellule tendono a spostarsi verso stati dove il loro tasso di crescita è più alto—o in modo rumoroso, con alcuni errori, o in modo deciso, sempre scalando verso una sopravvivenza migliore. Quando il team ha eseguito simulazioni al computer e le ha confrontate con dati di laboratorio reali, in particolare esperimenti in cui il farmaco veniva somministrato in modo continuo o a intermittenza (una settimana on, una settimana off), solo le strategie in cui le cellule scalano verso una fitness più alta hanno potuto riprodurre quanto osservato: il trattamento intermittente ad alta dose sopprimeva meglio il numero di cellule rispetto al trattamento continuo con lo stesso tempo totale e una quantità complessiva maggiore di farmaco.
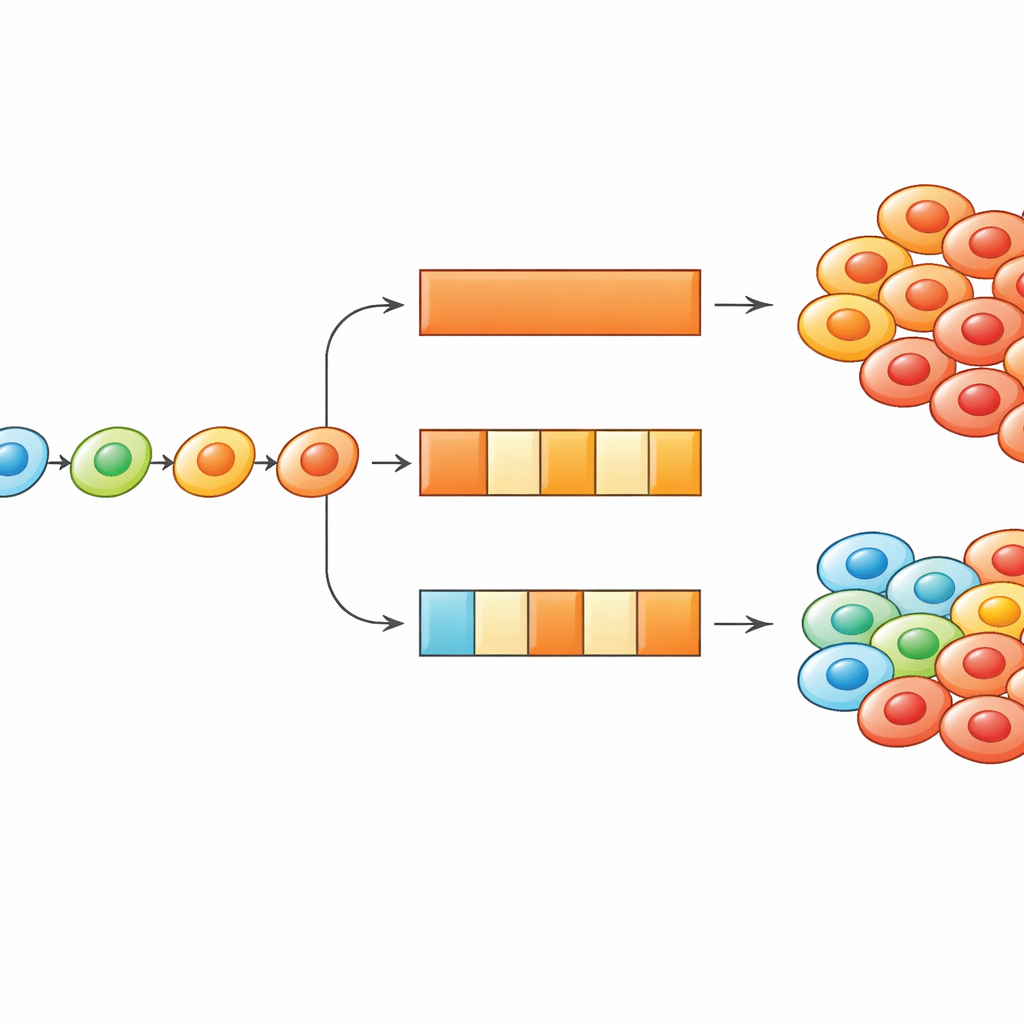
Usare la somministrazione on–off per trasformare l’adattamento contro il cancro
Approfondendo, i ricercatori hanno usato sia simulazioni sia equazioni più semplici per esplorare quanto spesso le cellule possono cambiare stato e quanto durano i periodi di farmaco-on e farmaco-off. Hanno scoperto che quando le cellule si adattano in modo diretto, i programmi di trattamento possono essere sintonizzati per rallentare o sfruttare questo adattamento. Accorciare la frequenza con cui le cellule possono aggiornare il loro stato—concettualmente, rallentare i meccanismi biologici che consentono il cambiamento fenotipico—tende a rendere i trattamenti intermittenti più potenti, perché le cellule non possono così rapidamente salire verso stati altamente resistenti. Al contrario, se le cellule iniziano in uno stato fortemente resistente, le pause dal farmaco possono dare loro il tempo di scivolare indietro verso stati più sensibili, in modo che la reintroduzione del farmaco inneschi un’ondata di morte cellulare. Lo studio mostra come il timing della somministrazione e la velocità dell’adattamento cellulare insieme plasmino quale schema funziona meglio.
Cosa significa questo per la cura del cancro in futuro
Per un non esperto, il messaggio centrale è che le cellule tumorali non sono nemici fissi; sono cambiacolore. In questo sistema di melanoma, le cellule sembrano muoversi attivamente verso comportamenti che le aiutano a crescere nelle condizioni che affrontano. Il modello degli autori suggerisce che questo adattamento diretto da solo—senza invocare cloni permanenti diversi—può spiegare perché gli schemi di somministrazione on–off a volte superano il dosaggio costante, anche quando usano meno farmaco nel complesso. Pur essendo risultati ottenuti su cellule coltivate in laboratorio e richiedendo ulteriore lavoro prima di orientare la cura dei pazienti, l’approccio offre un quadro pratico: misurando quanto velocemente e in quale direzione le cellule tumorali si adattano, i medici potrebbero riuscire in futuro a progettare schemi terapeutici che non solo attaccano i tumori ma anche indirizzano il loro “apprendimento” fenotipico verso vicoli ciechi anziché rotte di fuga.
Citazione: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Parole chiave: melanoma, resistenza ai farmaci, plasticità cellulare, terapia intermittente, modellizzazione matematica