Clear Sky Science · it
Base strutturale dell’attivazione per dimerizzazione della nitric oxide reductase dipendente da chinoli di Neisseria meningitidis
Come i batteri eludono la nostra difesa immunitaria
Quando batteri nocivi invadono l’organismo, le nostre cellule immunitarie rilasciano molecole tossiche come il monossido di azoto per ucciderli. Alcuni patogeni, tuttavia, hanno sviluppato stratagemmi molecolari per neutralizzare questo attacco e sopravvivere. Questo studio rivela, a livello atomico, come un enzima batterico chiave si riorganizzi in coppie per diventare molto più efficiente nella detossificazione del monossido di azoto, e perché comprendere questo comportamento metamorfico potrebbe aprire nuove strade per la progettazione di antibiotici.
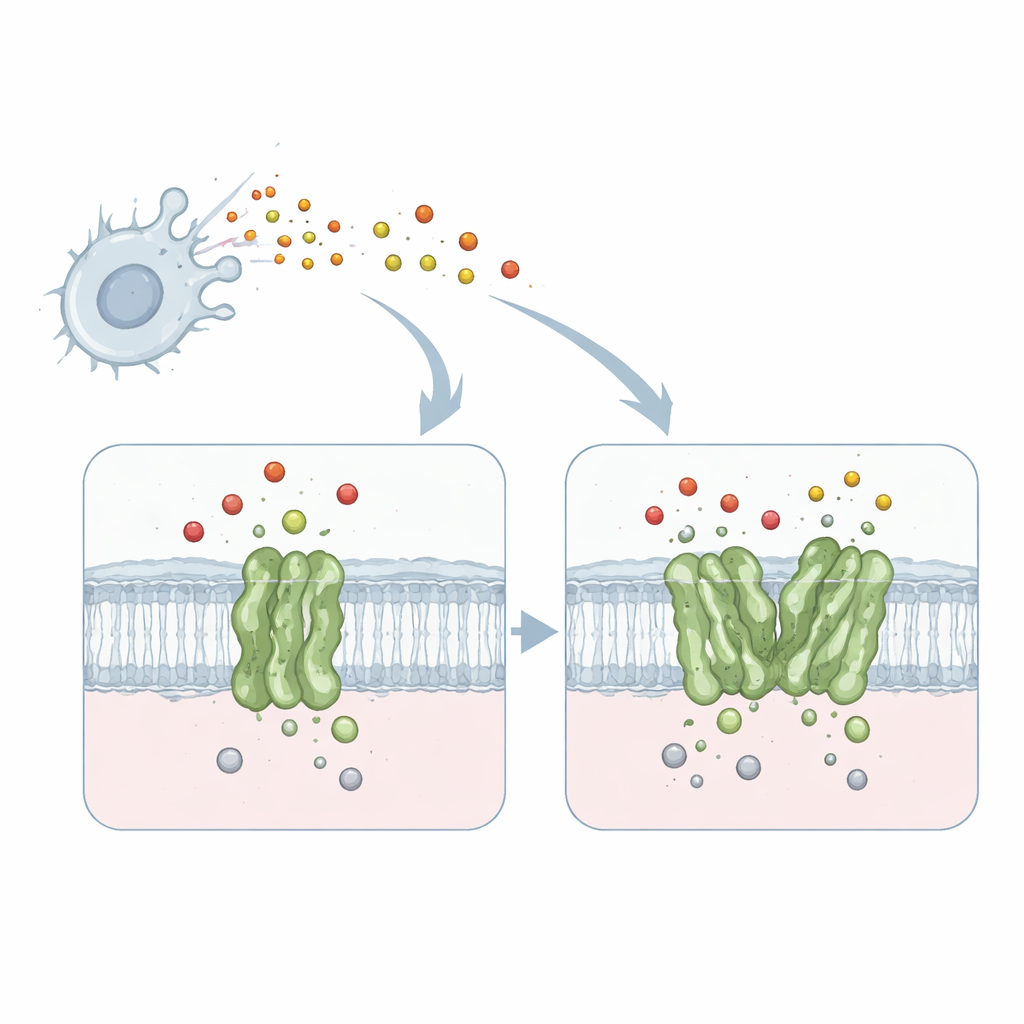
Una piccola macchina che disarma un gas tossico
Il lavoro si concentra su una proteina di membrana chiamata nitric oxide reductase dipendente da chinoli, o qNOR, del batterio che causa la meningite Neisseria meningitidis. qNOR è inserita nella membrana cellulare batterica e trasforma il monossido di azoto — un gas tossico prodotto dal nostro sistema immunitario — in prodotti meno dannosi. Questa detossificazione permette al microrganismo di continuare a respirare e crescere anche in ambienti ostili come i macrofagi umani. Poiché la respirazione e la rimozione del monossido di azoto sono vitali per la sopravvivenza del patogeno, qNOR rappresenta un bersaglio interessante per nuovi farmaci antimicrobici.
Quando uno è buono ma due sono meglio
Studi biochimici precedenti avevano mostrato che qNOR può esistere sia come unità singola (monomero) sia come coppia (dimero), e che il dimero è da due a quattro volte più veloce nel neutralizzare il monossido di azoto. Fino a oggi non era chiaro perché il semplice accoppiamento di due copie dello stesso enzima avesse un effetto così marcato sulle prestazioni. Per rispondere a questo, i ricercatori hanno usato la crio–microscopia elettronica single-particle ad alta risoluzione per catturare strutture tridimensionali dettagliate sia del qNOR monomerico sia di quello dimerico provenienti dalla stessa ceppa batterica. Hanno ottenuto viste a risoluzione quasi atomica — 1,89 angstroms per il dimero e 2,25 angstroms per il monomero — sufficientemente nitide da localizzare singole catene laterali di aminoacidi, ioni metallici e molte molecole d’acqua.
Un’elica flessibile diventa una staffa stabilizzante
Sorprendentemente, il cuore catalitico dell’enzima — il centro metallico dove il monossido di azoto viene convertito — appariva quasi identico in entrambe le forme. Le differenze chiave, invece, si manifestavano a distanza, in un’elica transmembrana chiamata TM10 e nel suo contatto con un’altra elica (TM2) quando due molecole di qNOR si accoppiano. Nel monomero, TM10 è ancorata debolmente e può oscillare e piegarsi in modo consistente, come rivelato dall’analisi computazionale dei dati cryo-EM. Nel dimero, TM10 di ciascun partner si blocca contro il vicino formando un fascio di quattro eliche, limitandone fortemente il movimento. Questa stabilizzazione riposiziona sottilmente un amminoacido cruciale, un glutammato denominato Glu563, portandolo vicino a un altro glutammato (Glu494) vicino al sito attivo e definendo un percorso più mirato per i protone in ingresso necessari alla reazione.
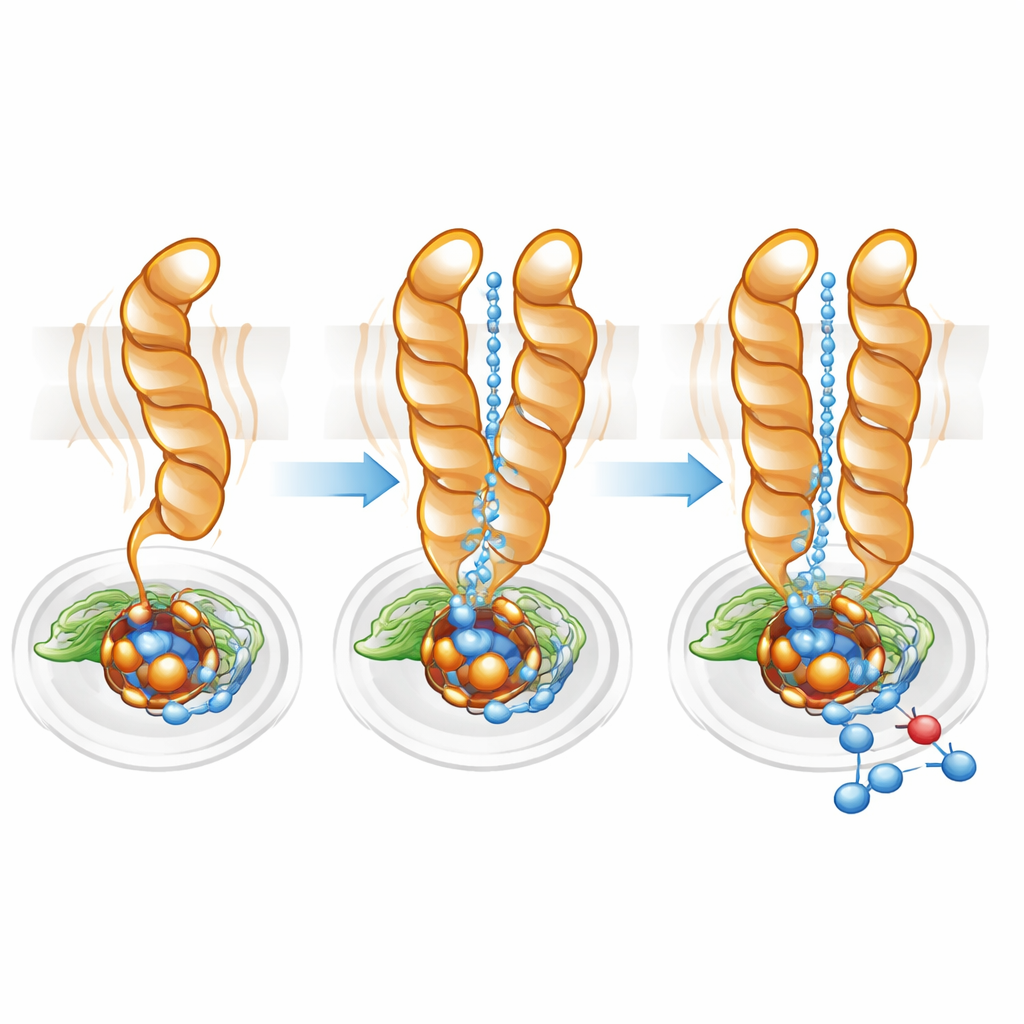
Affinare l’autostrada dei protoni
I protoni — ioni di idrogeno carichi positivamente — devono essere trasportati in modo efficiente dall’interno della cellula al sito attivo sepolto perché la riduzione del monossido di azoto proceda. Utilizzando software di mappatura dei percorsi, il team ha trovato una cavità idrofila che collega il citoplasma al sito attivo sia nel monomero sia nel dimero. Tuttavia, nel monomero questo canale era più ampio e più diffuso, coerente con la maggiore mobilità di TM10. Nel dimero, la posizione bloccata di TM10 e l’orientamento favorevole di Glu563 hanno contribuito a definire un percorso più diretto e meglio organizzato. La mutazione di Glu563 in amminoacidi incapaci di formare le stesse interazioni ha ridotto l’attività dell’enzima a meno del 10% del normale e ha anche destabilizzato il dimero, mentre mutazioni in posizioni correlate hanno ridotto la quantità del ferro non-eme essenziale nel sito attivo. Nel complesso, questi risultati mostrano che la formazione del dimero e il posizionamento preciso di Glu563 e Glu494 sono strettamente collegati sia all’integrità strutturale sia all’efficienza catalitica.
Trasformare le intuizioni strutturali in nuovi trattamenti
I risultati rivelano una linea chiara dall’accoppiamento delle proteine sulla superficie della membrana a sottili aggiustamenti in profondità nel sito attivo che controllano quanto efficacemente qNOR rimuove il monossido di azoto. In termini semplici, quando due copie dell’enzima si uniscono, raddrizzano e irrigidiscono un segmento flessibile che aiuta a indirizzare i protoni nel centro della reazione, aumentando la resa dell’enzima. Per lo sviluppo di farmaci, questo suggerisce una strategia non convenzionale: invece di bloccare direttamente il sito attivo, si potrebbero progettare molecole che forzino la separazione del dimero o che interrompano l’interazione Glu563–Glu494, costringendo l’enzima nel suo lento stato monomerico. Poiché qNOR e enzimi affini sono cruciali per la sopravvivenza di diversi patogeni pericolosi e resistenti ai farmaci, approcci guidati dalla struttura potrebbero contribuire alla prossima generazione di antimicrobici mirati.
Citazione: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Parole chiave: detossificazione del monossido di azoto, respirazione batterica, enzimi di membrana, crio microscopía elettronica, bersagli per farmaci antimicrobici