Clear Sky Science · it
La multiomica spaziale rivela caratteristiche immuno-metaboliche indotte da elettroporazione irreversibile al margine infiammatorio nel cancro del fegato
Perché un nuovo trattamento per il cancro del fegato richiede uno sguardo più attento
L’elettroporazione irreversibile (IRE) è una tecnica più recente per distruggere i tumori epatici utilizzando brevi impulsi elettrici ad alta tensione invece del calore. Poiché può risparmiare vasi sanguigni e dotti biliari vicini, è particolarmente utile per tumori in sedi delicate. Tuttavia, fino a un terzo dei pazienti vede comunque la comparsa di recidive proprio accanto all’area trattata. Questo studio indaga cosa accade in quella sottile regione di confine dopo l’IRE e se cambiamenti nascosti nelle cellule immunitarie e nel metabolismo cellulare lì potrebbero silenziosamente creare le condizioni per la ricomparsa del cancro.
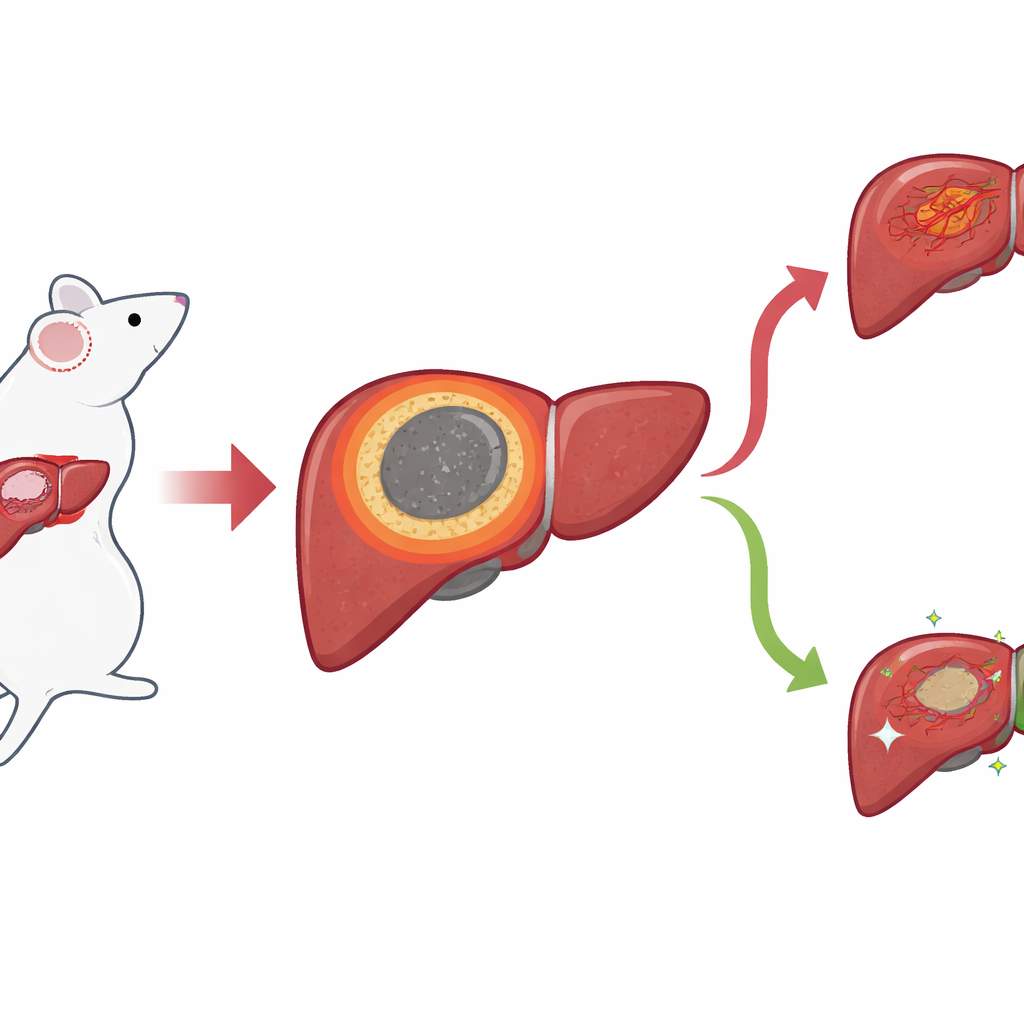
Un sottile margine con grandi conseguenze
Usando un modello murino di cancro al fegato, i ricercatori si sono concentrati sull’anello sottile di tessuto che si forma tra il nucleo necrotico ablated e il fegato sano circostante dopo l’IRE. Lo chiamano margine infiammatorio, o IM. Le immagini al microscopio standard mostravano che questa zona si trova esattamente dove di solito appaiono le recidive locali, ma i suoi confini risultavano difficili da tracciare a occhio nudo. Per ottenere un quadro più nitido, il team ha applicato metodi “spaziali” che rilevano quali geni e piccole molecole sono presenti preservando la loro posizione nel tessuto. Con la trascrittomica spaziale hanno mappato l’attività genica spot per spot e scoperto un cluster distinto di spot che si allineava precisamente con l’IM, separando il centro necrotico dalle aree di fegato normale e dal tumore.
Cellule immunitarie si radunano—ma molte frenano l’attacco
Gli scienziati hanno poi utilizzato il sequenziamento dell’RNA a singola cellula e a singolo nucleo, insieme a un potente metodo di profilazione chiamato CyTOF, per catalogare i tipi cellulari individuali attraverso il fegato. Hanno scoperto che l’IM è dominato da un tipo di cellula immunitaria chiamata macrofago. In particolare, una sotto-popolazione simile ai “macrofagi associati ai lipidi” (LAM) è affluita nell’IM nei giorni successivi all’IRE. Queste cellule presentano marcatori di superficie e profili genici legati all’immunosoppressione, compresi alti livelli di PD-L1, una molecola nota per attenuare le risposte delle cellule T. Le analisi dell’espressione genica suggeriscono che questi macrofagi sono abili nel fagocitare materiale, rispondere a attrattori chimici e inviare segnali che possono reprimere le stesse cellule T necessarie per uccidere le cellule tumorali. L’imaging ha confermato che i macrofagi PD-L1-positivi erano molto più abbondanti nell’IM rispetto al tessuto normale vicino.
Un punto caldo di chimica lipidica alterata
Successivamente, il team ha sovrapposto questo paesaggio immunitario con la metabolomica spaziale, un approccio di imaging con spettrometria di massa che mappa la distribuzione di centinaia di piccole molecole. Hanno mostrato che l’IM possiede un’impronta metabolica diversa sia rispetto al nucleo necrotico sia rispetto al fegato circostante. In questa stretta fascia diverse vie lipidiche (legate ai grassi) erano fortemente potenziate, inclusa la produzione di acidi grassi insaturi, derivati dell’acido arachidonico e sfingolipidi. Lipidi segnalatori chiave come prostaglandine e leucotrieni, derivati dall’acido arachidonico, erano arricchiti nell’IM, mentre altre vie enzimatiche per processare la stessa molecola risultavano relativamente attenuate. Un’altra famiglia lipidica, gli sfingolipidi—comprendenti ceramidi e sfingomieline—si accumulava anch’essa, supportata da un’aumentata espressione degli enzimi che li sintetizzano e rimodellano.
Uno spostamento graduale dal danno a una nicchia ricca di carburante
Suddividendo il margine infiammatorio in tre sottili strati dal nucleo necrotico verso l’esterno, i ricercatori hanno osservato un graduale cambiamento nella chimica. Più vicino alla zona morta, lipidi complessi e molecole correlate al colesterolo erano più abbondanti, mentre più esternamente aumentavano piccole molecole legate all’energia come il glucosio e certi amminoacidi. Questo schema suggerisce che, su una breve distanza, il tessuto passa da un ambiente carico di lipidi e ricco di segnali a uno orientato a fornire carburante per la sopravvivenza e la crescita cellulare. Gli autori propongono che questo riprogrammarsi passo dopo passo contribuisca a sostenere i macrofagi immunosoppressivi, affamati di lipidi, che dominano l’IM e potrebbe silenziosamente preparare il terreno per la ricolonizzazione da parte delle cellule tumorali.
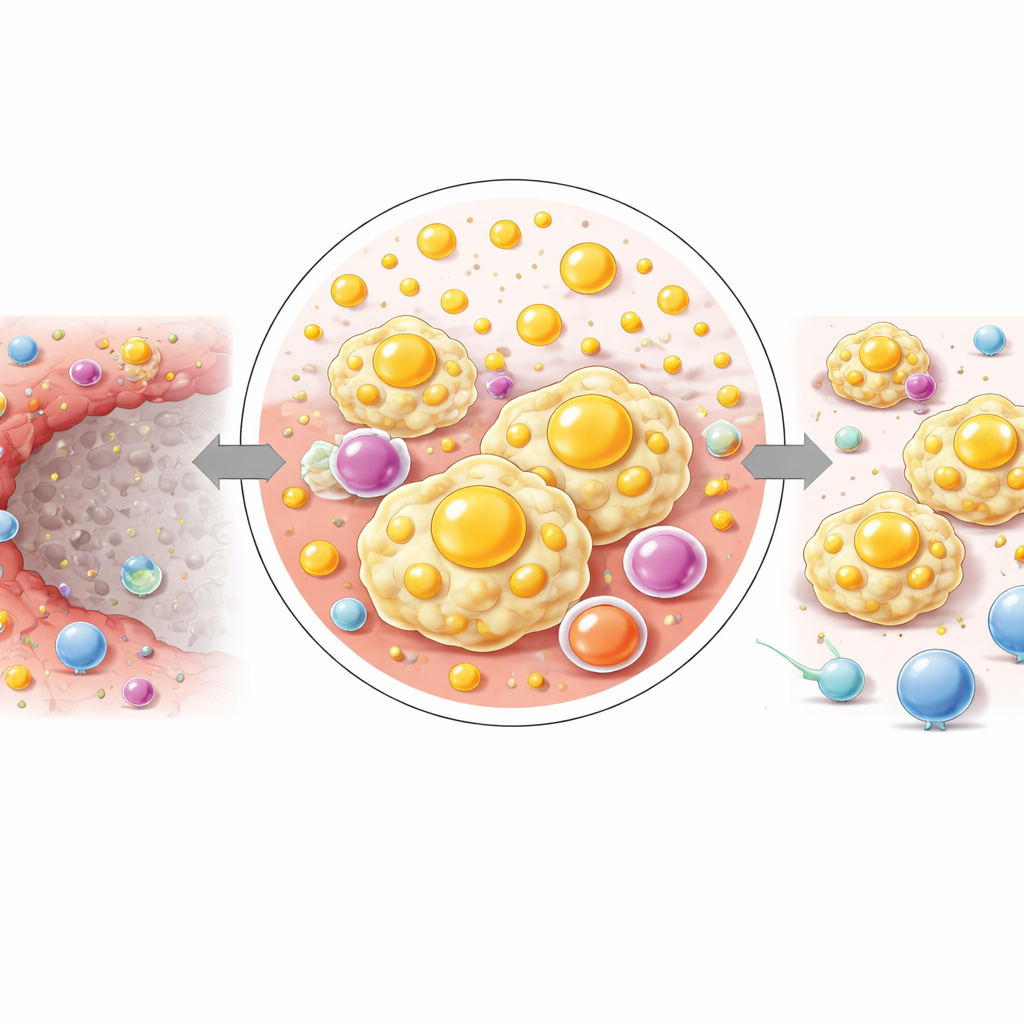
Cosa significa per la cura futura del cancro del fegato
In termini semplici, questo lavoro mostra che l’IRE fa più che uccidere le cellule tumorali: crea anche un anello sottile di tessuto dove cellule immunitarie e chimica lipidica insieme costruiscono un quartiere schermato e favorevole al tumore. I macrofagi in questa zona sono abbondanti, carichi di lipidi e orientati più a spegnere le cellule T che ad aiutarle. Poiché questi cambiamenti sono strettamente legati a specifiche vie metaboliche, indicano nuove possibilità terapeutiche. Combinare l’IRE con farmaci che mirano al metabolismo lipidico o che bloccano PD-L1 in questo margine potrebbe, in teoria, trasformare un bordo soggetto a recidive in una zona che porta realmente al completamento dell’eliminazione del cancro del fegato.
Citazione: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Parole chiave: cancro del fegato, ablazione tumorale, microambiente immune, macrofagi, metabolismo lipidico