Clear Sky Science · it
Attivatori di NRF2 e l’inibitore dell’esportazione nucleare, selinexor, limitano i coronavirus colpendo una rete che coinvolge ACE2, TMPRSS2 e XPO1 tramite un meccanismo indipendente da NRF2
Farmaci che aiutano le cellule a dire “no” ai coronavirus
La maggior parte dei trattamenti antivirali attuali mira al virus stesso. Ma i virus sono maestri del cambiamento e le nuove varianti possono rapidamente ridurre l’efficacia di tali farmaci. Questo studio esplora una strategia diversa: rendere le nostre cellule meno ospitali sia per coronavirus pericolosi come SARS-CoV-2 sia per ceppi stagionali più miti. Modificando il modo in cui le cellule gestiscono alcuni proteine chiave di controllo, i ricercatori mostrano che piccole molecole già esistenti possono ridurre nettamente l’infezione nei modelli di laboratorio, e lo fanno con un meccanismo che non dipende dalla via antivirale per cui erano originalmente conosciute.
Un nuovo angolo per la difesa contro i coronavirus
Il team si è concentrato su composti noti per attivare un programma di protezione cellulare controllato da una proteina chiamata NRF2. Questi composti — 4-octyl itaconate (4OI), bardoxolone (BARD) e sulforafano (SFN) — sono stati testati insieme a selinexor (SEL), un farmaco che blocca una proteina di trasporto chiamata XPO1, che aiuta a spostare altre proteine fuori dal nucleo cellulare. In modelli di cellule polmonari e renali, tutti e quattro i farmaci hanno ridotto i livelli di SARS-CoV-2 senza danneggiare le cellule. Hanno inoltre funzionato contro diverse varianti preoccupanti. Sorprendentemente, quando NRF2 è stato eliminato geneticamente, i virus si sono in realtà replicati meglio, dimostrando che NRF2 è naturalmente protettivo — ma i farmaci hanno comunque mantenuto una forte attività antivirale, mostrando che il loro potere antivirale proviene da una via diversa. 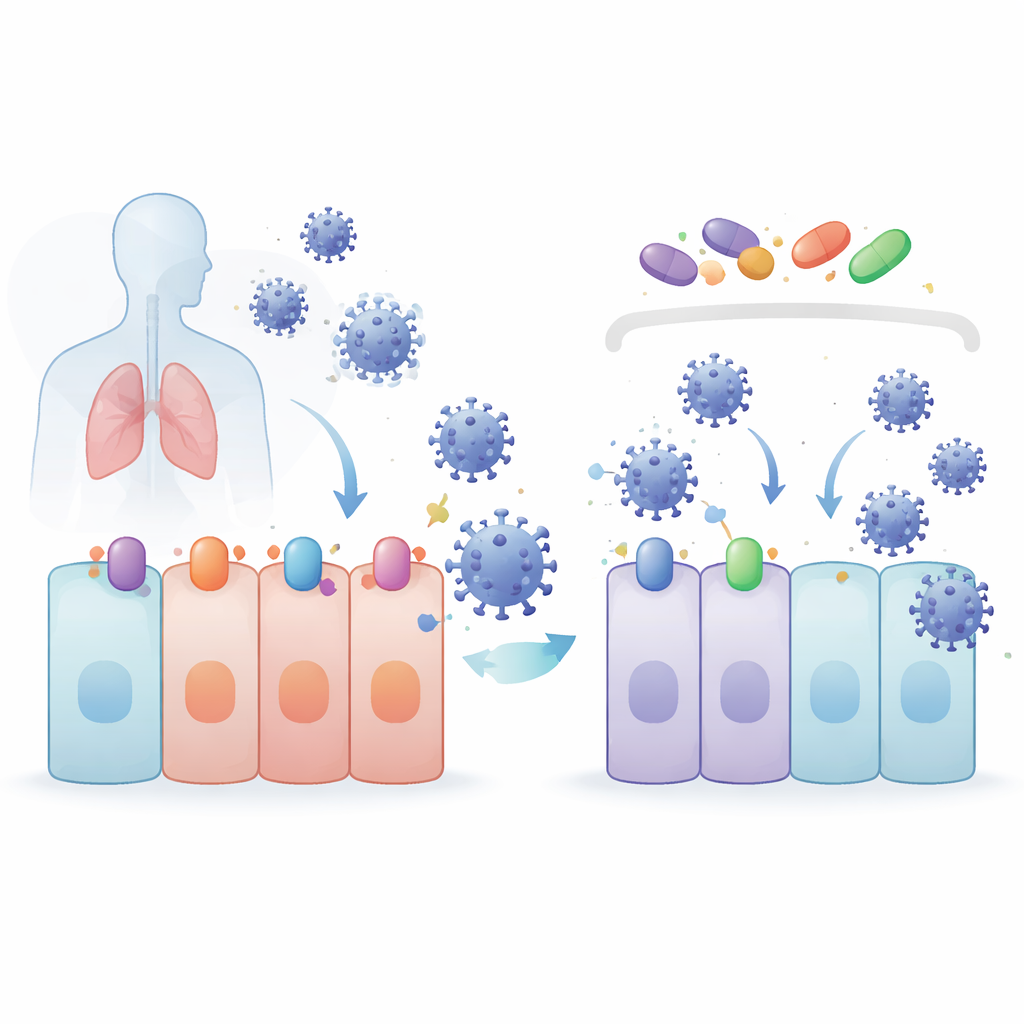
Chiudere la porta d’ingresso virale
I coronavirus iniziano l’infezione agganciandosi a proteine recettoriali sulla superficie cellulare. Per SARS-CoV-2 e parenti stretti, la porta principale è ACE2, con l’aiuto di un enzima che taglia chiamato TMPRSS2. Anche la proteina di esportazione XPO1 sembra favorire l’infezione. I ricercatori hanno rilevato che 4OI, BARD, SFN e SEL hanno tutti ridotto le quantità di ACE2, TMPRSS2 e XPO1 nelle cellule polmonari umane. 4OI e SEL sono risultati particolarmente potenti se presenti prima dell’infezione, e hanno bloccato l’ingresso di particelle simili al virus rivestite dalla proteina spike del coronavirus. In altre parole, questi farmaci non si limitano a rallentare il virus una volta entrato — aiutano a rimuovere le serrature e le maniglie di cui il virus ha bisogno per aprire la porta in primo luogo.
Come le cellule smontano gli aiuti chiave al virus
Approfondendo, il team ha mostrato che 4OI accelera la degradazione della proteina ACE2. In condizioni normali, ACE2 persiste per molte ore; con 4OI, scompariva dalla superficie cellulare in una frazione di quel tempo. Questa distruzione richiedeva due marcatrici cellulari, NEDD4L e MDM2, che attaccano alle proteine segnali molecolari di “smaltiscimi”. Bloccare questi marcatori indeboliva la capacità di 4OI di eliminare ACE2. Sorprendentemente, il macchinario usuale di triturazione delle proteine, il proteasoma, non era la via principale. Invece, ACE2 veniva instradato nel sistema di riciclo e smaltimento della cellula, il lisosoma. I farmaci riducevano anche l’attività genica di ACE2 e XPO1, in parte diminuendo l’attivazione di STAT3, una proteina che normalmente aumenta la trascrizione del gene ACE2. 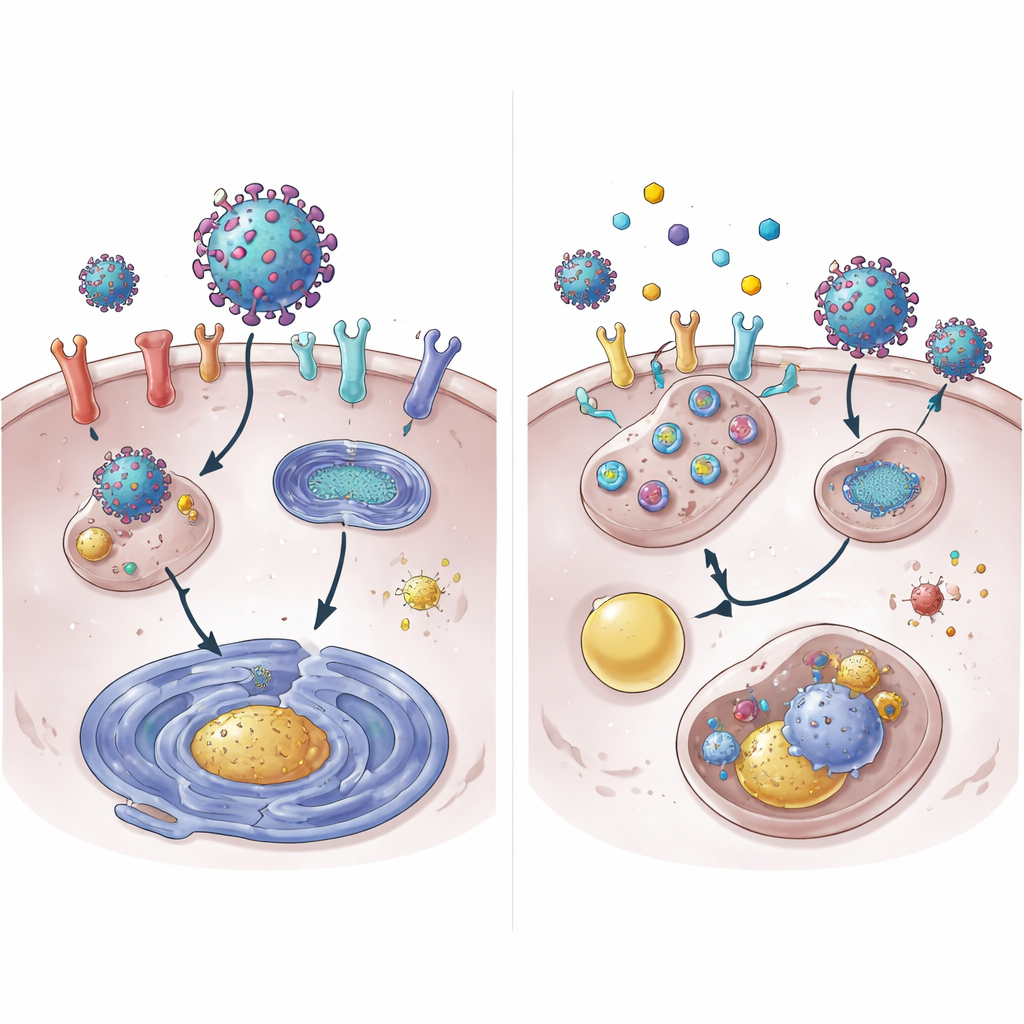
Coronavirus stagionali e la connessione con XPO1
I ricercatori si sono poi rivolti a hCoV-229E, un coronavirus stagionale che di solito causa raffreddori lievi ma può essere pericoloso in persone con sistema immunitario indebolito. Utilizzando virus ingegnerizzati che brillano quando si replicano, hanno mostrato che tutti e quattro i composti sopprimevano fortemente 229E nelle cellule polmonari e vascolari, anche in assenza di NRF2. Diversamente da SARS-CoV-2, questo virus usa un recettore diverso, ANPEP, che i farmaci non alteravano. Il loro effetto però seguiva da vicino quanto riducevano XPO1. L’abbassamento di XPO1 stesso riduceva nettamente la replicazione di 229E, e l’effetto di selinexor quasi scompariva in queste cellule povere di XPO1. Questa gerarchia — SEL più dipendente da XPO1, BARD meno — suggerisce che ogni composto ha un mix leggermente diverso di bersagli, con XPO1 come snodo centrale per molte delle loro azioni antivirali.
Cosa potrebbe significare per i trattamenti futuri
Per i non specialisti, il messaggio chiave è che è possibile combattere i coronavirus non solo attaccando il virus, ma rimodellando delicatamente le nostre cellule in modo che siano più difficili da infettare. In cellule umane coltivate in laboratorio, i composti studiati hanno rimosso siti di aggancio e vie di supporto cruciali su cui SARS-CoV-2 e un comune coronavirus del raffreddore fanno affidamento, e l’hanno fatto in larga parte senza la via NRF2 che inizialmente li aveva resi interessanti. Sebbene questi risultati siano ancora preclinici e non si traducano direttamente in terapie per il momento, evidenziano una strada promettente: farmaci che contemporaneamente riducono l’ingresso virale, attenuano l’infiammazione dannosa e proteggono i tessuti colpendo una rete condivisa di proteine dell’ospite come ACE2, TMPRSS2 e XPO1.
Citazione: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Parole chiave: antivirali indirizzati all’ospite, ingresso dei coronavirus, ACE2 e TMPRSS2, attivatori di NRF2, inibizione di XPO1