Clear Sky Science · it
Quantificazione ultrarapida e specifica di miRNA tramite cinetica di spegnimento della fluorescenza a singola molecola
Perché i test rapidi per le malattie sono importanti
La diagnosi di malattie come il cancro o le infezioni virali spesso si riduce a individuare tracce minime di materiale genetico nel sangue o in altri fluidi corporei. I test considerati standard oggi possono essere molto accurati, ma talvolta sono lenti, costosi o faticano a rilevare segnali molto rari. Questo studio presenta un nuovo metodo basato sul microscopio, chiamato Q‑FISH, in grado di leggere questi indizi genetici in meno di un secondo. Se tradotto in strumenti clinici, tale rapidità e precisione potrebbe facilitare la diagnosi precoce, il monitoraggio della risposta ai trattamenti e la personalizzazione delle cure per ogni paziente.
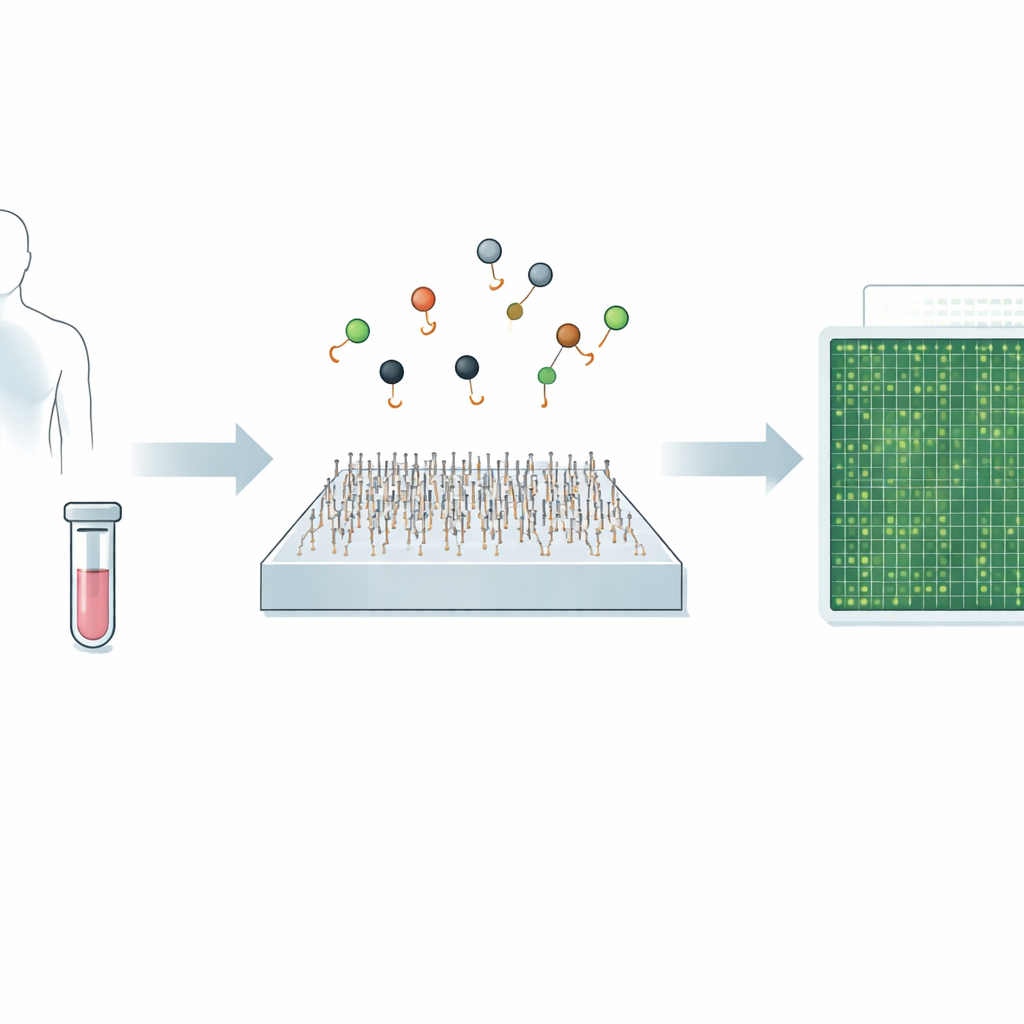
Un nuovo modo di vedere i minuscoli messaggi genetici
Il lavoro si concentra sui microRNA—brevi frammenti di RNA che regolano l’espressione genica e sono fortemente legati a molti tumori, malattie cardiache, infezioni e disturbi cerebrali. Poiché i microRNA sono molto piccoli e spesso differiscono solo per uno o due nucleotidi, metodi standard come la PCR e il sequenziamento di nuova generazione possono avere difficoltà a distinguere tipi molto simili, soprattutto quando sono presenti a livelli molto bassi. Recenti approcci di imaging a singola molecola hanno migliorato questa specificità tracciando il legame e il distacco di sonde individuali, ma sono comunque rimasti relativamente lenti, impiegando circa dieci minuti per analizzare un singolo bersaglio.
Osservare il lampeggiare della luce per trovare il bersaglio giusto
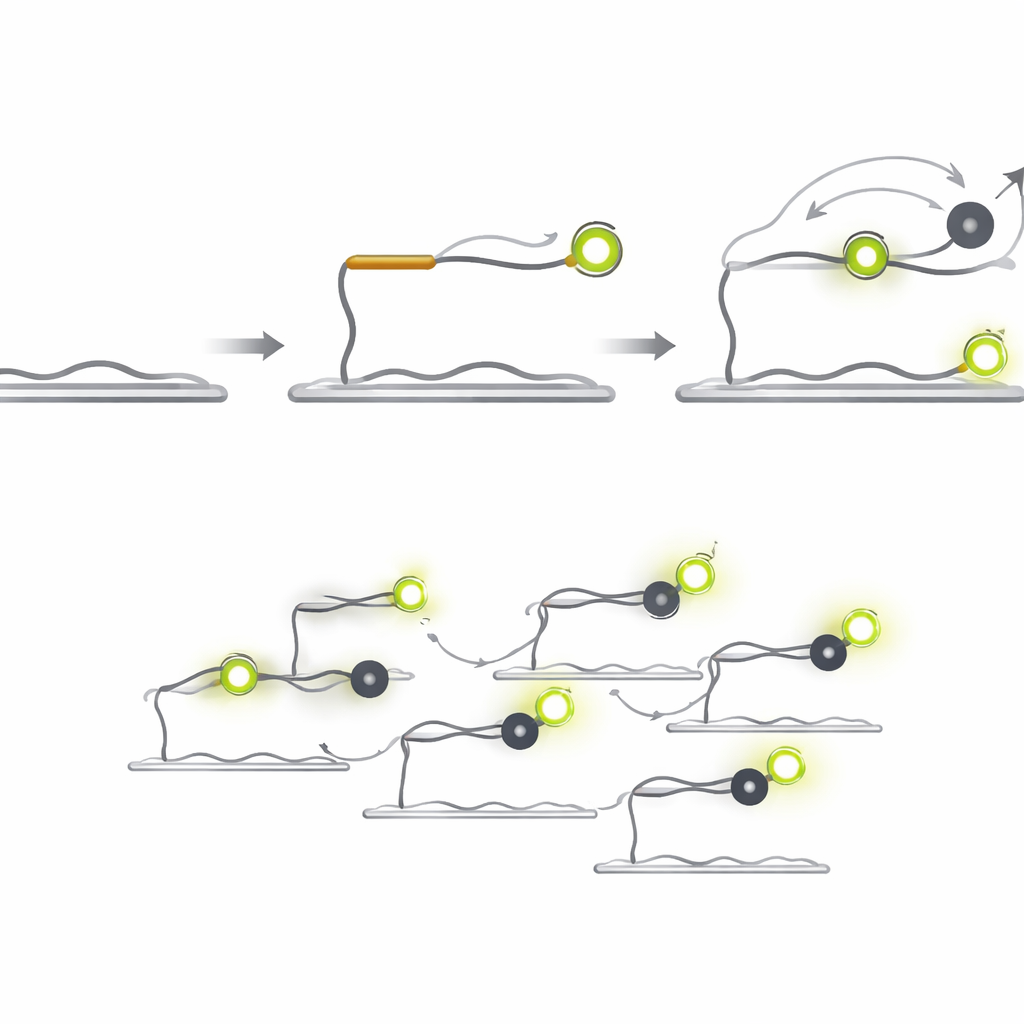
Q‑FISH ribalta il problema sfruttando i brevi lampi di luce delle singole molecole. Il metodo utilizza due sonde di DNA corte che riconoscono posizioni adiacenti su un microRNA bersaglio. Una sonda porta un colorante fluorescente che brilla sotto un laser, mentre l’altra porta un “quencher” che assorbe la luce quando si avvicina. La sonda fluorescente si lega al bersaglio e resta abbastanza a lungo da essere vista, mentre la sonda quencher è progettata per legarsi e staccarsi molto rapidamente. Ogni volta che il quencher si avvicina al colorante, la luce cala all’improvviso; quando si allontana, la luce riprende. Registrando questi rapidi lampeggi on‑off dalle singole molecole e analizzando la durata dei periodi luminosi e spenti, il sistema può decidere se è presente un vero bersaglio.
Da minuti a millisecondi
Poiché la sonda quencher non emette luce propria, può essere usata a concentrazioni molto più alte delle sonde fluorescenti senza creare un’abbagliamento di fondo. Accorciare la sonda quencher aumenta la velocità con cui si stacca, e aumentare la sua concentrazione fa crescere la frequenza con cui si lega. Insieme, queste scelte progettuali portano a un salto drammatico nella velocità. Nei test con un microRNA legato al cancro chiamato let‑7a, Q‑FISH ha raggiunto oltre il 70% della sua efficienza massima di rilevamento in appena un secondo di osservazione. Metodi comparabili a singola molecola richiedevano decine o centinaia di secondi per ottenere prestazioni simili, rendendo Q‑FISH oltre 600 volte più veloce in termini pratici.
Distinguere segnali quasi identici e misurare campioni reali
I ricercatori hanno inoltre dimostrato che Q‑FISH può distinguere tra diversi membri della famiglia di microRNA let‑7, che condividono sequenze quasi identiche ma hanno ruoli diversi nel controllo di geni legati al cancro. Hanno impiegato due strategie di multiplexing. In una, diverse sonde quencher sono state introdotte una dopo l’altra, ciascuna tarata su un microRNA leggermente diverso; nell’altra, le sonde sono state etichettate con colori diversi e immaginate contemporaneamente. In entrambi i casi, l’analisi dei pattern di lampeggio ha permesso al team di identificare correttamente quale microRNA fosse presente in circa un secondo. Infine, hanno applicato il metodo all’RNA totale estratto da tessuti umani di fegato e polmone. Aggiungendo quantità note di microRNA sintetici e contando i punti risultanti, hanno costruito curve di calibrazione e poi letto i livelli naturali presenti nei tessuti, rivelando differenze chiare tra gli organi.
Cosa potrebbe significare per i test futuri
Nel complesso, lo studio mostra che Q‑FISH può identificare microRNA specifici con altissima accuratezza, anche quando sono quasi identici tra loro, e farlo a velocità molto superiori rispetto ai precedenti metodi a singola molecola. Sebbene gli esperimenti siano stati condotti su campioni preparati usando un microscopio specializzato, l’idea di fondo—utilizzare rapidi eventi di spegnimento della luce invece del solo legame lento—potrebbe essere adattata a molti tipi di marker genetici, inclusi frammenti di DNA tumorale nel sangue. Con ulteriore ingegnerizzazione e una preparazione dei campioni più snella, questo approccio potrebbe avvicinare la diagnostica molecolare rapida, altamente multiplexata ed estremamente sensibile all’uso clinico quotidiano.
Citazione: Kim, J., Hohng, S. Ultrafast and specific miRNA quantification via single-molecule fluorescence quenching kinetics. Commun Biol 9, 432 (2026). https://doi.org/10.1038/s42003-026-09714-8
Parole chiave: rilevamento microRNA, imaging a singola molecola, diagnostica molecolare, spegnimento della fluorescenza, biopsia liquida