Clear Sky Science · it
Una strategia in due fasi mediata dall’actina consente a Campylobacter jejuni di promuovere l’aggregazione mitocondriale e l’omeostasi del ferro, per la sopravvivenza e la persistenza intracellulare
Perché questa piccola battaglia dentro le cellule è importante
Le intossicazioni alimentari da pollo poco cotto vengono spesso attribuite a un batterio chiamato Campylobacter jejuni. La maggior parte delle persone guarisce, ma questo microrganismo è sorprendentemente abile nel sopravvivere in molti ambienti, il che ne facilita la diffusione dalla fattoria alla tavola. Questo studio esamina cosa accade quando il batterio si nasconde all’interno di un’ameba libera—un comune microbo d’acqua dolce—e mette in luce un espediente di sopravvivenza sorprendentemente sofisticato che ruota attorno alla rimodellazione dello scheletro interno della cellula, all’aggregazione dei “pacchetti energetici” chiamati mitocondri e al controllo del ferro e della chimica ossidativa nociva. Comprendere questa fase nascosta del suo ciclo vitale potrebbe indicare nuove strategie per ridurre la contaminazione prima che il batterio raggiunga le persone.
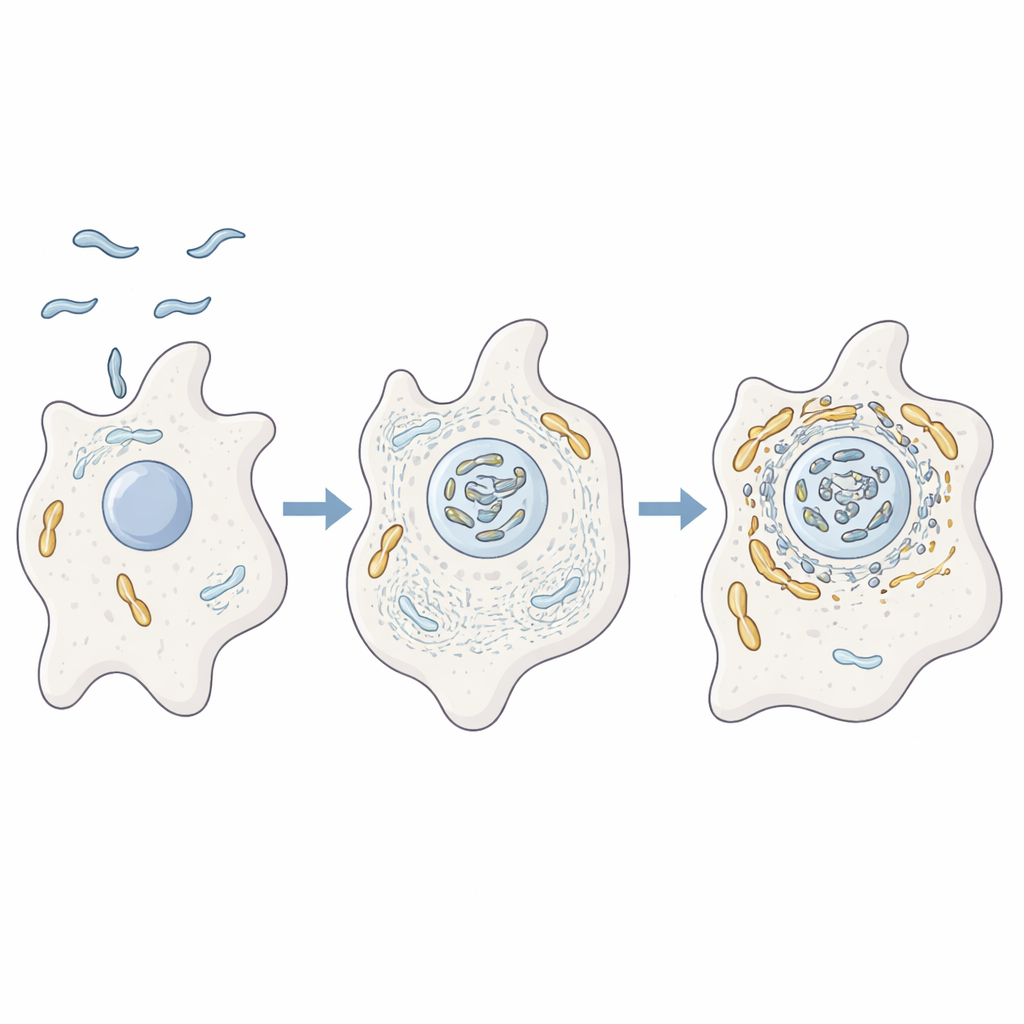
Un microrganismo che si allena nelle amebe
Gli autori hanno studiato come C. jejuni si comporta all’interno dell’ameba Acanthamoeba castellanii, un organismo unicellulare che vive nel suolo e nell’acqua. Queste amebe fungono da campo di addestramento per molti batteri patogeni, offrendo protezione da condizioni avverse e dai disinfettanti. Utilizzando analisi proteiche avanzate, microscopia e mutanti genetici, i ricercatori hanno mostrato che quando C. jejuni infetta le amebe finisce in stretta associazione con i mitocondri dell’ospite. Allo stesso tempo, lo scheletro interno dell’ameba fatto di actina, insieme a proteine che regolano forma e mobilità, è fortemente arricchito in prossimità di questi mitocondri, suggerendo che il batterio stia attivamente riorganizzando l’architettura interna della cellula ospite.
Piegare lo scheletro cellulare per spostare i pacchetti energetici
Per verificare se l’actina guida davvero questa interazione, il gruppo ha bloccato la formazione dei filamenti di actina o la loro ramificazione in reti. In queste condizioni i mitocondri non si raggruppavano più intorno ai batteri ma restavano sparsi come puntini, e la sopravvivenza del batterio diminuiva. Hanno quindi analizzato due proteine batteriche helper, CiaD e CiaI, che vengono iniettate nelle cellule ospiti tramite il flagello del batterio, una coda simile a una frusta. CiaD si è rivelata capace di potenziare la crescita dell’actina e promuovere proiezioni appuntite sulla superficie dell’ameba, aiutando la cellula a catturare i batteri. Una volta all’interno, i mitocondri sono stati osservati aggregarsi intorno al compartimento batterico in modo dipendente dall’actina, collocando il batterio in una zona privilegiata ricca di macchine energetiche dell’ospite.
Un interruttore molecolare che rimodella i mitocondri
Se CiaD è fondamentale per l’ingresso, CiaI controlla ciò che avviene dopo. Quando i ricercatori hanno cancellato il gene per CiaI, C. jejuni non ha più indotto un forte aggregamento mitocondriale e è sopravvissuto meno bene all’interno delle amebe. L’aggiunta di CiaI purificata attaccata a microsfere, senza batteri vivi, è stata sufficiente a indurre la fusione e l’aggregazione dei mitocondri vicini e a rimuovere localmente actina. Test biochimici hanno mostrato che CiaI si lega a molecole trasportatrici di energia in modo cooperativo, comportandosi come un interruttore molecolare che può accendere o spegnere la sua attività a seconda delle condizioni all’interno dell’ospite. Gli autori propongono che dopo che la crescita dell’actina guidata da CiaD avvicina i mitocondri, CiaI promuova la degradazione locale dell’actina e rimodelli la rete mitocondriale in densi aggregati che circondano il compartimento contenente il batterio.
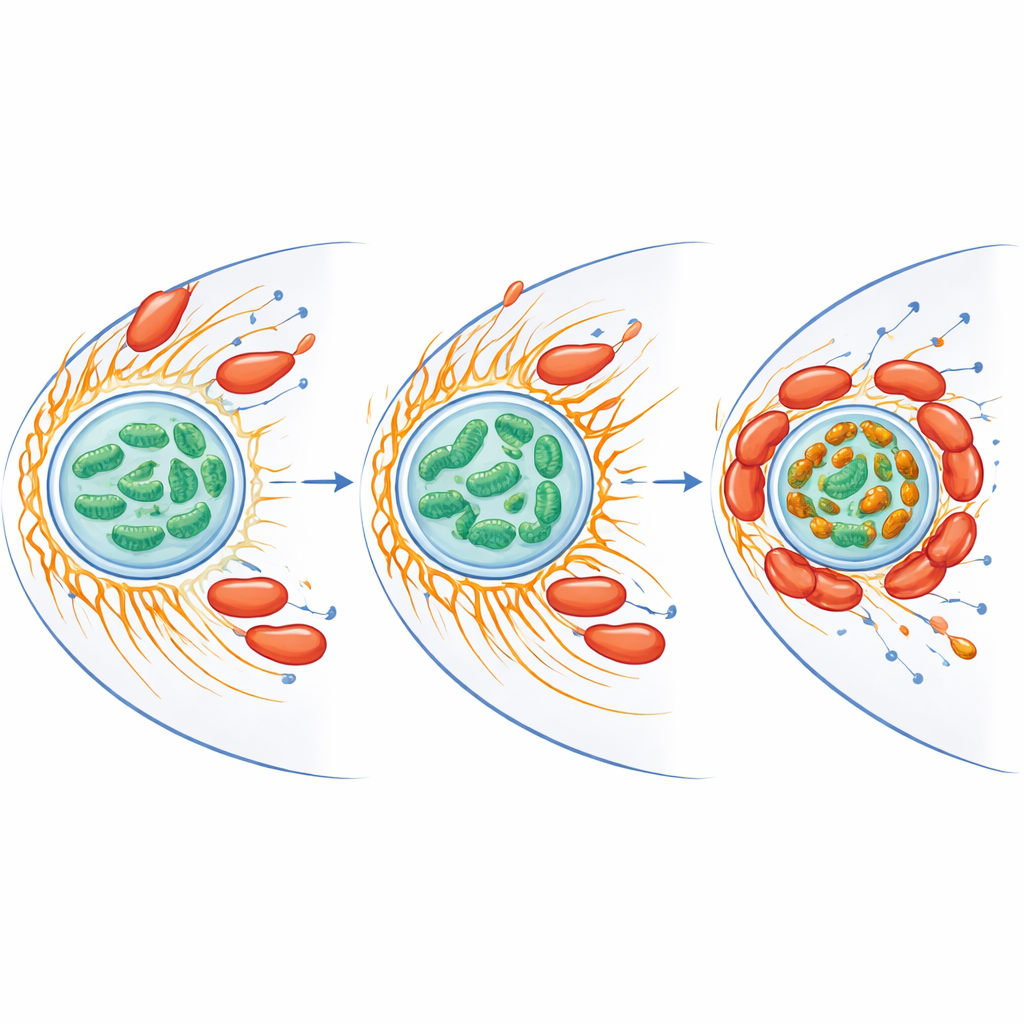
Riprogrammare il ferro e lo stress all’interno della cellula ospite
I mitocondri non si limitano a produrre energia: gestiscono anche il ferro e producono specie reattive dell’ossigeno, forme chimicamente aggressive di ossigeno che possono uccidere i microrganismi. I ricercatori hanno riscontrato che l’infezione riduceva il ferro libero complessivo all’interno dei mitocondri ma, allo stesso tempo, creava vividi aggregati ricchi di ferro dove i mitocondri si riunivano intorno ai batteri. Le proteine coinvolte nella gestione del ferro e nella difesa contro lo stress ossidativo aumentavano sia nell’ospite sia nel batterio. Quando il gruppo ha rimosso il ferro libero usando un agente cheloante, l’esplosione di specie reattive dell’ossigeno dell’ameba è diminuita e la sopravvivenza di C. jejuni è aumentata drasticamente. I mitocondri nelle cellule infette mostravano anche un potenziale di membrana più elevato, segno di attività aumentata, suggerendo che il batterio spinga i “pacchetti energetici” dell’ospite in uno stato che favorisce la sua persistenza limitando al contempo la chimica ossidativa dannosa.
Cosa significa per la sicurezza alimentare e le infezioni
Nel complesso, i risultati supportano una strategia in due fasi: prima, CiaD stimola la crescita dell’actina per aiutare il batterio a entrare nelle amebe e ad attirare i mitocondri verso il sito di ingresso; secondo, CiaI smantella localmente l’actina e rimodella i mitocondri in aggregati ricchi di ferro avvolti attorno al compartimento batterico, attenuando le difese ossidative dell’ospite. Questo controllo finemente sintonizzato della forma cellulare, dell’uso energetico e dell’equilibrio dei metalli aiuta C. jejuni a sopravvivere all’interno delle amebe e probabilmente contribuisce alla sua capacità di persistere nell’ambiente e successivamente infettare gli esseri umani. Rivelando i protagonisti chiave in questa lotta microscopica, lo studio indica nuovi bersagli—come le proteine Cia, i contatti actina‑mitocondri o le vie di gestione del ferro—che potrebbero essere interrotti per ridurre contaminazione e malattia.
Citazione: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Parole chiave: Campylobacter, amebe, mitocondri, cit Scheletro di actina, omeostasi del ferro