Clear Sky Science · it
La regolazione multilivello dei recettori kainato GluK3 è mediata dalle subunità Neto e dallo zinco
Perché contano gli interruttori minimi del cervello
Ogni pensiero, ricordo e stato d’animo nel cervello dipende da microscopici interruttori che consentono il passaggio di particelle cariche dentro e fuori le cellule nervose. Questo studio si concentra su uno di questi interruttori, un recettore poco noto chiamato GluK3. Scoprendo come proteine partner e ioni zinco finemente modulano il comportamento di GluK3, il lavoro offre indizi su come i circuiti cerebrali mantengano l’equilibrio — e su come tale equilibrio possa sbilanciarsi in disturbi come l’epilessia, la depressione e la schizofrenia.
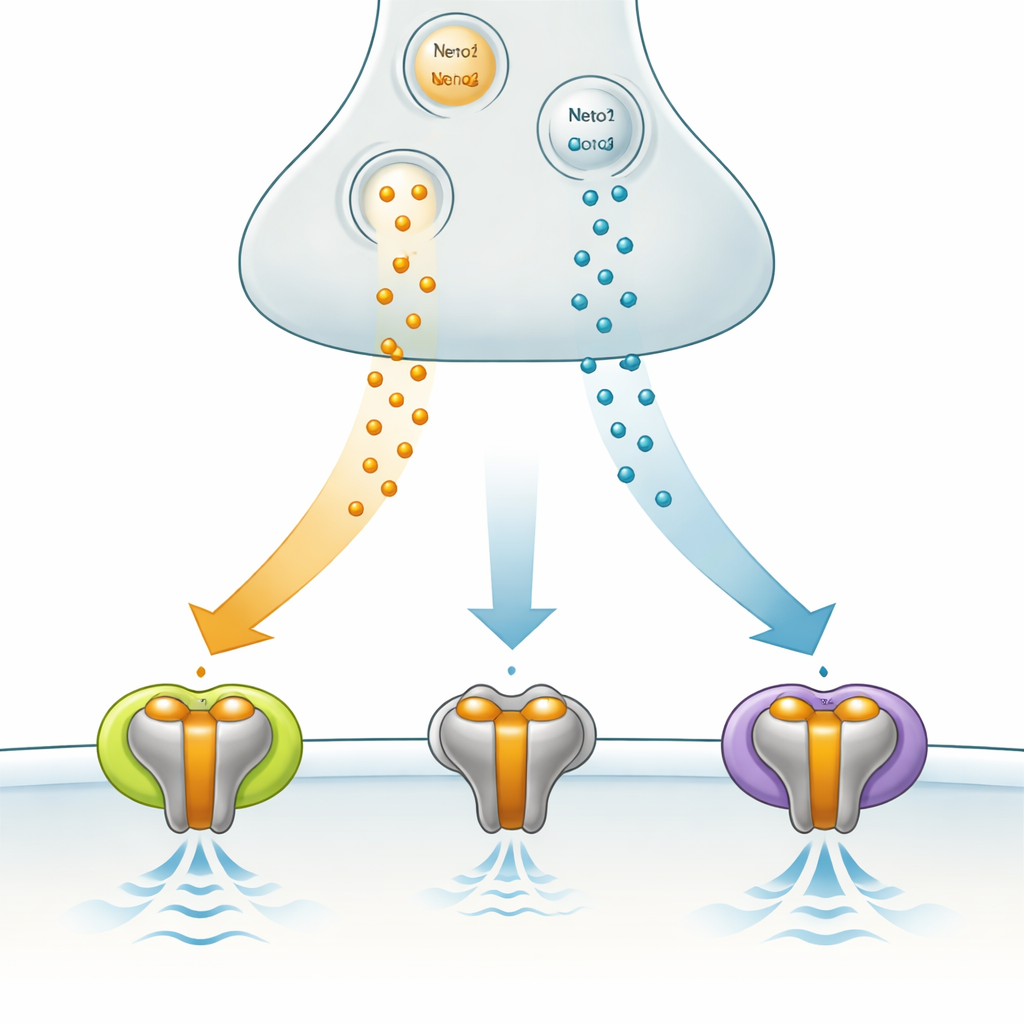
Una porta di segnale specializzata nel cervello
GluK3 appartiene alla famiglia dei recettori kainato, parte del più ampio gruppo dei recettori del glutammato che mediano la comunicazione rapida tra neuroni. A differenza di alcuni suoi parenti, GluK3 non si limita ad accendere o spegnere i segnali; funziona piuttosto come un filtro che risponde al meglio a raffiche brevi e intense del messaggero chimico glutammato. È arricchito in regioni cerebrali come l’ippocampo, fondamentale per la memoria e per la modulazione dei ritmi di rete, e cambiamenti nella funzione di GluK3 sono stati collegati a comportamenti legati all’ansia. Queste caratteristiche rendono GluK3 un bersaglio promettente, ma ancora poco compreso, per modulare l’attività cerebrale in salute e malattia.
Proteine helper che tirano le fila
Il gruppo ha esaminato come due proteine helper, Neto1 e Neto2, influenzino il comportamento di GluK3 in cellule umane ingegnerizzate per produrre questi componenti. Entrambi i helper rallentavano la velocità con cui GluK3 si spegne dopo essere stato attivato e riducevano una forma naturale di blocco interno che normalmente limita il flusso di corrente. Tuttavia, avevano effetti opposti sulla rapidità con cui GluK3 può essere riutilizzato. Con Neto1, i recettori recuperavano rapidamente, pronti a rispondere a segnali rapidi e ripetuti. Con Neto2, il recupero diventava molto più lento, favorendo l’integrazione dei segnali su intervalli più lunghi. In sostanza, scegliendo diversi helper, una sinapsi può decidere se far comportare GluK3 come un rilevatore a fuoco rapido o come un sensore più lento e aggregante.
Lo zinco come secondo livello di controllo
Molte terminazioni nervose che rilasciano glutammato liberano anche zinco, che può legarsi ai recettori e modificarne il funzionamento. Lavori precedenti hanno mostrato che lo zinco aumenta in modo inusuale l’attività di GluK3, mentre tende a smorzare altri tipi di recettori. Qui, gli autori hanno riscontrato che questo potenziamento dipende fortemente da quale proteina Neto è presente. Quando GluK3 è da solo, lo zinco raddoppia grossolanamente il tempo durante il quale il recettore rimane attivo e aumenta modestamente la corrente. L’aggiunta di Neto1 attenua questo effetto. Al contrario, quando GluK3 si associa a Neto2, zinco e Neto2 agiscono insieme per potenziare fortemente la corrente, molto più di quanto possano fare singolarmente. Ciò suggerisce che sinapsi ricche di Neto2 e zinco possono amplificare notevolmente i segnali mediati da GluK3 durante attività intense, mentre le sinapsi ricche di Neto1 restano più contenute.
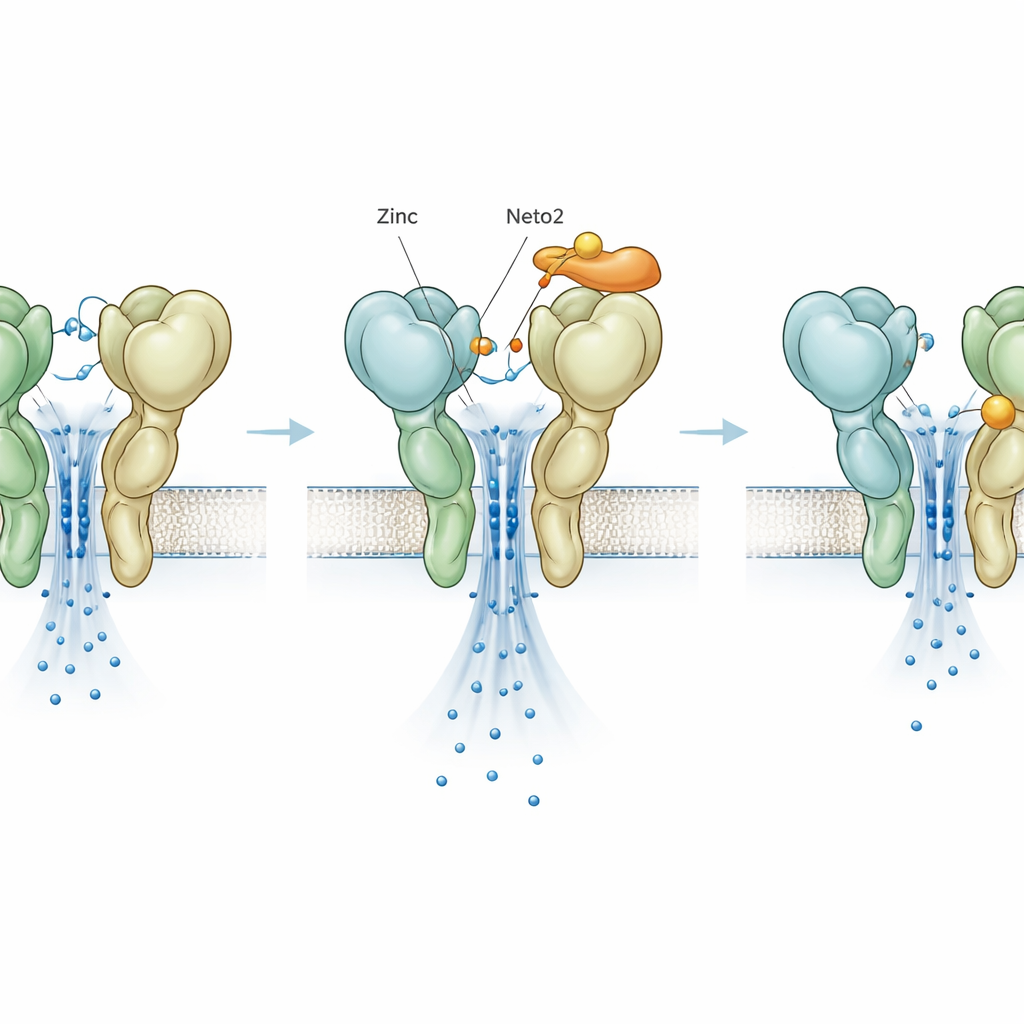
Un freno nascosto rivelato da una mutazione
Per separare le azioni dello zinco da quelle delle proteine helper, i ricercatori hanno introdotto una modifica di una singola lettera in GluK3, chiamata D759G, che rimuove un noto sito di legame per lo zinco. Come previsto, questa mutazione da sola ha reso il recettore più stabile e più lento a spegnersi, imitando l’effetto usuale dello zinco. Sorprendentemente, quando lo zinco è stato aggiunto a questo mutante, non ha più aumentato l’attività; al contrario, ha accelerato lo spegnimento e ridotto la corrente, rivelando un secondo sito di legame per lo zinco precedentemente nascosto che agisce come un freno. Neto1 e Neto2 hanno comunque esercitato i loro effetti caratteristici sul mutante, mostrando che la loro influenza principale non dipende dal sito di zinco originale. Tuttavia, anche questa azione inibitoria dello zinco appena scoperta è stata modulata in modo diverso dai due helper, aggiungendo un ulteriore comando regolabile al sistema.
Vedere la struttura dietro il comportamento
Per collegare funzione e forma, il gruppo ha utilizzato la microscopia crio‑elettronica per visualizzare il recettore GluK3 mutante congelato in uno stato non attivo. Le immagini hanno rivelato che la regione che lega il glutammato forma un’unità più compatta e strettamente impacchettata nel mutante D759G rispetto al GluK3 normale. Questo irrigidimento strutturale probabilmente rende più difficile per il recettore assumere una conformazione di spegnimento, spiegando perché il mutante, come il GluK3 legato allo zinco, rimane attivo più a lungo. Allo stesso tempo, le immagini hanno mostrato che non tutte le parti del recettore erano bloccate in un’unica disposizione, indicando un’architettura intrinsecamente flessibile particolarmente sensibile a piccoli stimoli chimici.
Cosa significa per la salute del cervello
Complessivamente, lo studio ritrae GluK3 non come un semplice interruttore acceso‑spento ma come un hub finemente regolabile dove convergono glutammato, proteine helper e zinco. Neto1 e Neto2 determinano quanto rapidamente i segnali si attenuano e quanto velocemente i recettori possono rispondere di nuovo, mentre lo zinco può sia potenziare ulteriormente sia, in alcune condizioni, limitare l’attività attraverso più siti di legame. Poiché GluK3, le proteine Neto e lo zinco coesistono nelle sinapsi coinvolte nella memoria e sono implicati nell’epilessia e in condizioni psichiatriche, comprendere questo controllo multilivello potrebbe guidare terapie future che ritunano delicatamente la segnalazione sinaptica anziché sopprimerla del tutto.
Citazione: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Parole chiave: recettori kainato, GluK3, proteine Neto, zinco sinaptico, plasticità sinaptica