Clear Sky Science · it
Abuso di droghe psicotrope e depressione: un focus sull’epigenetica
Perché questa ricerca conta nella vita quotidiana
Le droghe che creano dipendenza e la depressione vengono spesso trattate come problemi separati, eppure compaiono frequentemente insieme nella stessa persona. Questa rassegna spiega come l’uso prolungato di sostanze come metanfetamina, cocaina, oppioidi e cannabis possa lasciare “cicatrici molecolari” durature nel cervello che aumentano il rischio di depressione. Scoprendo questi cambiamenti nascosti, l’articolo indica la strada verso test futuri in grado di segnalare chi è più vulnerabile — e verso terapie più precise che potrebbero invertire il danno invece di limitarsi a mascherarne i sintomi.
Come dipendenza e umore depresso si intrecciano
Gli autori iniziano delineando il stretto legame clinico tra abuso di sostanze e depressione. Chi fa uso ripetuto di sostanze che creano dipendenza ha molte più probabilità di riferire tristezza persistente, perdita di piacere, disturbi del sonno e pensieri suicidari. Regioni cerebrali che controllano ricompensa, motivazione, memoria e processo decisionale — l’area tegmentale ventrale, il nucleo accumbens, la corteccia prefrontale e l’ippocampo — sono centrali in entrambe le condizioni. L’esposizione cronica alle droghe altera neuromediatori come dopamina e serotonina, ormoni dello stress regolati dall’asse ipotalamo-ipofisi-surrene, segnali immunitari e l’apporto energetico dei neuroni. Questi cambiamenti insieme rendono il cervello meno resiliente allo stress e più incline a stati depressivi, anche molto tempo dopo l’ultima assunzione.
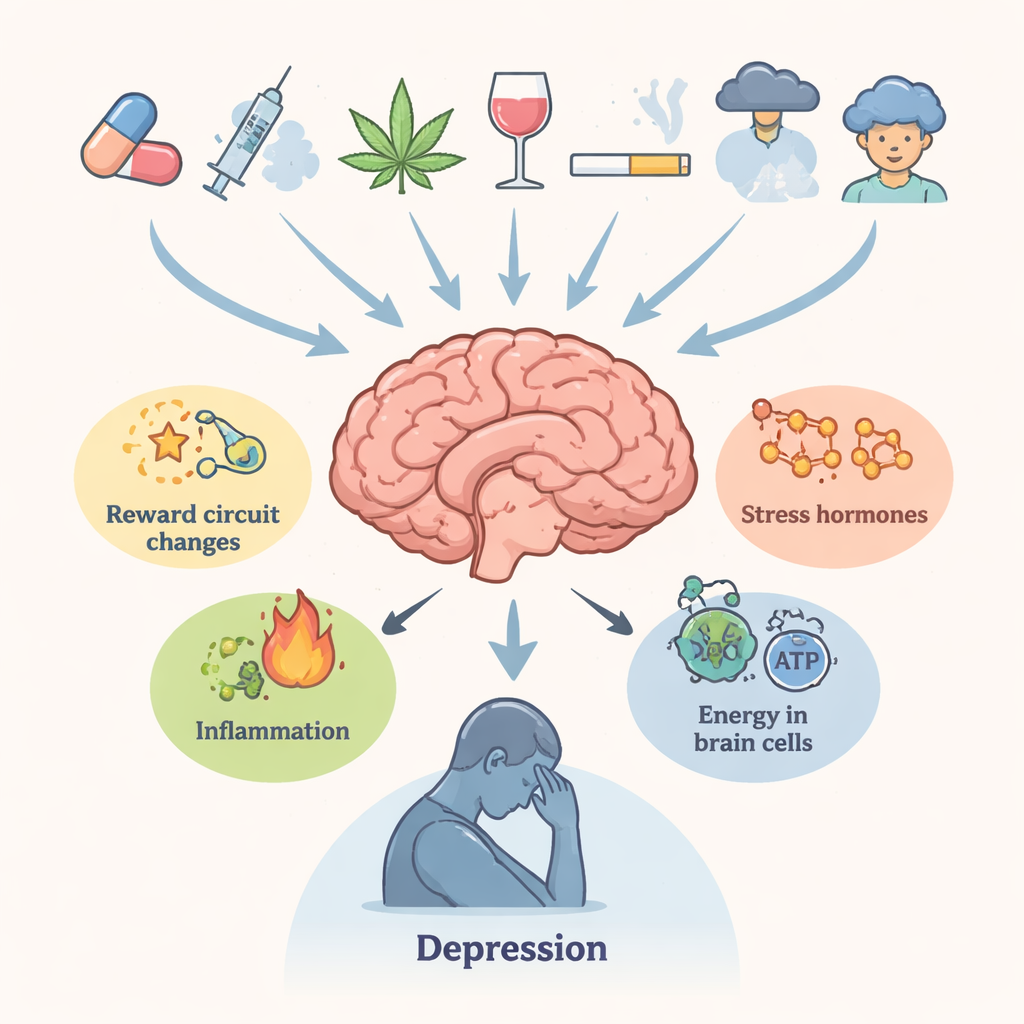
Sostanze che rimodellano la chimica cerebrale
La rassegna passa in esame diverse classi principali di droghe. Gli stimolanti di tipo anfetaminico e i loro parenti, comprese le sostanze sintetiche note come “bath salts”, provocano forti ondate di dopamina e altri trasmettitori che, nel tempo, danneggiano le terminazioni nervose, alterano l’equilibrio del glutammato, affaticano il reticolo endoplasmico e spingono le cellule verso forme dannose di autodigestione (autofagia). L’uso di cannabis in adolescenza è associato a un maggior rischio di depressione e suicidio in età successiva, verosimilmente attraverso cambiamenti duraturi nei recettori dei cannabinoidi, nella struttura della materia bianca e nella sensibilità dei circuiti dopaminergici. Gli oppioidi, pur alleviando il dolore, possono innescare infiammazione, disfunzione mitocondriale e una riduzione dei segnali che supportano la crescita neuronale, come il fattore neurotrofico derivato dal cervello (BDNF). La cocaina attiva ripetutamente il sistema dello stress e modifica regolatori chiave come FKBP5, contribuendo ad ansia e umore basso durante l’astinenza. In ogni caso, le perturbazioni biologiche tendono a persistere, contribuendo a spiegare perché i sintomi emotivi possano durare oltre l’intossicazione evidente.
Epigenetica: la memoria dell’esposizione
Per capire perché gli effetti delle droghe durino nel tempo, gli autori si concentrano sull’epigenetica — tag chimici e interruttori molecolari che modulano l’attività genica senza cambiare le lettere del DNA. Le droghe che creano dipendenza modificano la metilazione del DNA (un marchio sulla base citosina), cambiano gruppi chimici sulle proteine istoniche che impacchettano il DNA e alterano gli RNA non codificanti che regolano finemente quali proteine vengono prodotte. Per esempio, metanfetamina e cocaina spostano i profili di metilazione in regioni cerebrali legate alla ricompensa, modificando i livelli di enzimi che aggiungono o rimuovono questi marchi. Oppioidi e stimolanti rimodellano acetilazioni e metilazioni degli istoni su geni che controllano i recettori del glutammato, la segnalazione dello stress e la struttura sinaptica. Dozzine di microRNA, RNA lunghi non codificanti e RNA circolari aumentano o diminuiscono con l’esposizione alle droghe, influenzando collettivamente infiammazione, crescita neuronale e forza delle sinapsi. Questi cambiamenti epigenetici funzionano come una “memoria” molecolare della storia di consumo.
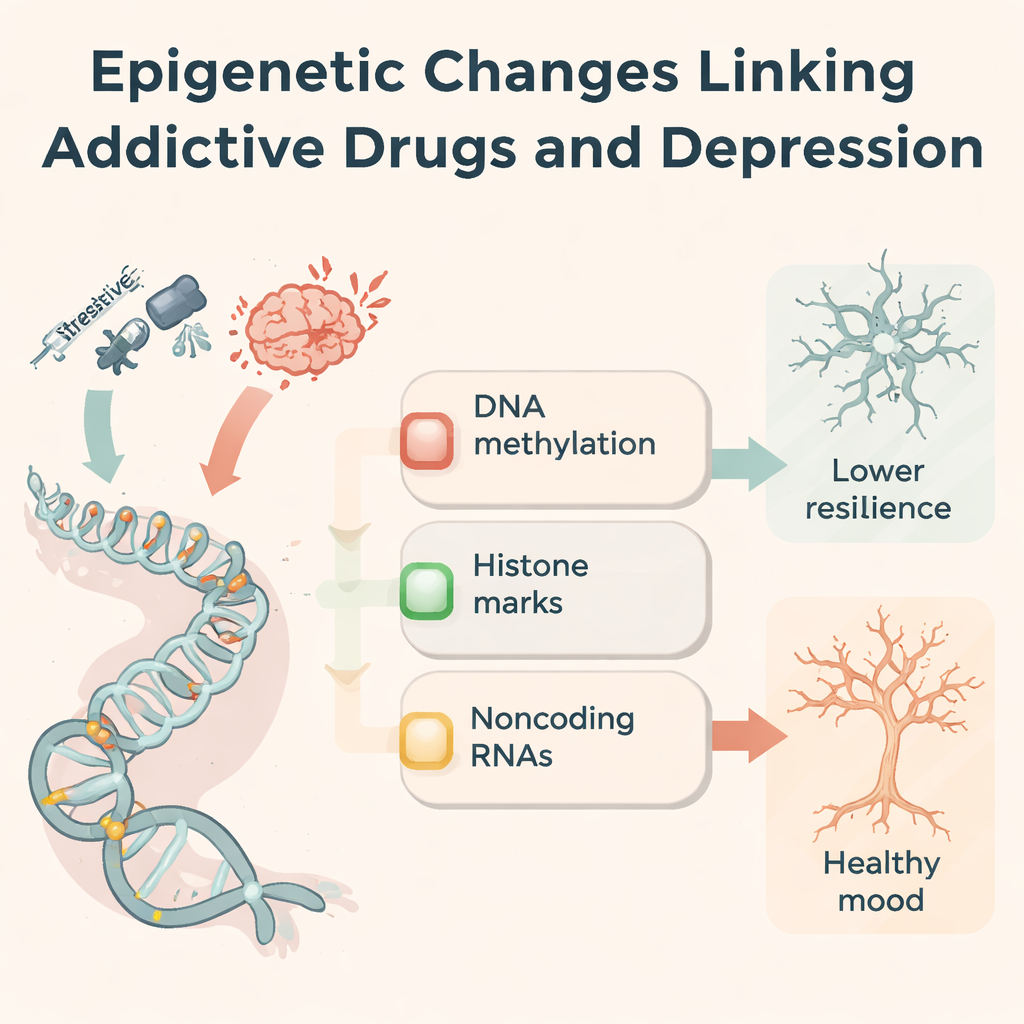
Vie molecolari condivise nella depressione e nella dipendenza
La stessa macchina epigenetica si osserva anche in persone e animali con depressione che non hanno mai assunto droghe. Esperienze stressanti possono modificare la metilazione di recettori coinvolti nella risposta allo stress (come NR3C1 e FKBP5), ridurre fattori di crescita utili come il BDNF e rimodellare vie immunitarie e del glutammato. Molti degli stessi RNA non codificanti alterati dalle droghe risultano disregolati anche nella depressione, influenzando la nascita di nuovi neuroni, la risposta delle microglia all’infiammazione e la forza delle connessioni sinaptiche. Gli autori propongono un quadro in tre parti: regolazione della risposta allo stress, ristrutturazione dei circuiti della ricompensa e plasticità sinaptica. Lungo questi assi, dipendenza e depressione convergono ripetutamente su un piccolo insieme di geni e marchi, suggerendo una ragione biologica per cui i due disturbi coesistono così spesso.
Cosa significa questo per prevenzione e trattamento futuri
Concludendo, la rassegna sostiene che i cambiamenti epigenetici potrebbero diventare biomarcatori di allerta precoce e bersagli per terapie di nuova generazione. Farmaci ad ampio spettro che rimuovono marchi epigenetici hanno già mostrato alcuni effetti simili agli antidepressivi negli animali, ma sono troppo grossolani per l’uso umano di routine. Nuovi strumenti — come editor dell’epigenoma basati su CRISPR e terapie che modulano microRNA o RNA lunghi specifici — potrebbero un giorno correggere geni problematici in particolari cellule cerebrali preservando le altre. Gli autori avvertono che la maggior parte dei dati attuali proviene da roditori e da tessuto cerebrale in massa, e che la biologia umana è più complessa. Tuttavia, rivelando come droghe che causano dipendenza e depressione scrivano sullo stesso “quaderno” molecolare, questo lavoro apre una strada promettente verso terapie più personalizzate e durature.
Citazione: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Parole chiave: dipendenza e depressione, epigenetica, abuso di droghe, metilazione del DNA, RNA non codificanti