Clear Sky Science · it
Med13 è coinvolto nella migrazione radiale e nella proiezione controlaterale dei neuroni corticali tramite PlxnA4
Come un singolo gene contribuisce a costruire il cervello pensante
I cervelli non si limitano a crescere; vengono costruiti, cellula dopo cellula, in strati e schemi di connessioni precisamente organizzati. Questo studio analizza come un gene, chiamato Med13, aiuti le giovani cellule cerebrali nella corteccia a spostarsi nel posto giusto e a connettersi attraverso i due emisferi. Poiché errori sottili in questo processo costruttivo sono sempre più associati a condizioni come l’autismo e il deficit intellettivo, comprendere Med13 offre una finestra su come lo sviluppo cerebrale precoce possa deviare dal percorso normale.
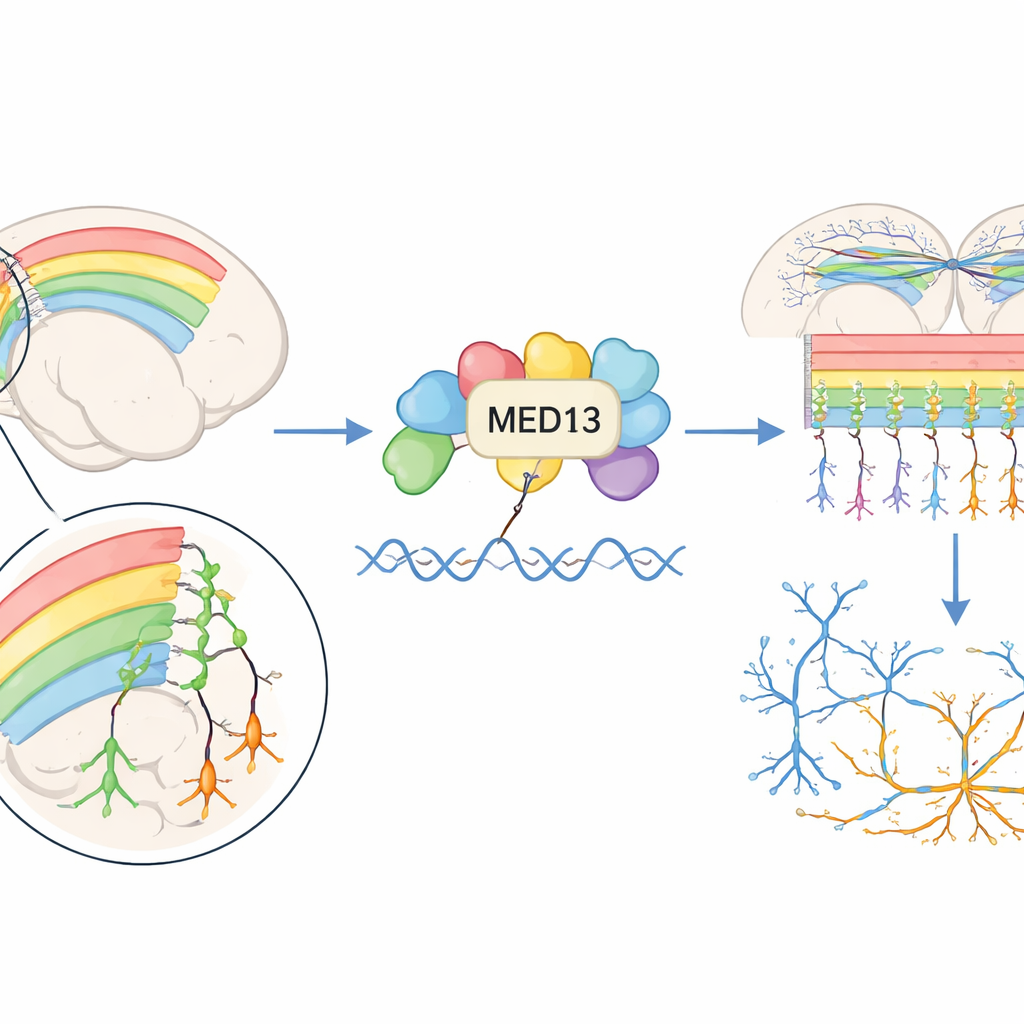
Costruire il quartiere di sei strati della corteccia
La corteccia cerebrale, il foglio esterno increspato del cervello, è organizzata in sei strati di neuroni che si formano durante la vita embrionale. I neuroni neonati nascono in profondità e poi migrano verso l’esterno in una sequenza “dall’interno verso l’esterno” per formare questi strati. Gli autori hanno prima indagato dove e quando Med13 è attivo durante questo processo. Negli embrioni di topo, Med13 è risultato presente ad alti livelli nelle regioni in cui le cellule staminali neurali si dividono e dove i giovani neuroni sono in movimento, in particolare attorno a un punto chiave di mezza gestazione quando vengono generate molte cellule corticali. Med13 era presente sia nelle cellule precursori in divisione sia nei neuroni in maturazione, suggerendo che partecipi in modo ampio alla formazione della corteccia.
Quando i neuroni perdono la strada
Per verificare cosa faccia concretamente Med13, il gruppo ha ridotto selettivamente i suoi livelli nei neuroni corticali in sviluppo dei topi utilizzando una tecnica che introduce DNA progettato nel cervello fetale. I neuroni etichettati privi di Med13 sono stati seguiti nel tempo. Rispetto ai neuroni di controllo, molte cellule carenti di Med13 si sono fermate a metà percorso invece di raggiungere gli strati corticali superiori dove dovrebbero trovarsi. Anche giorni dopo la nascita, una larga frazione è rimasta dispersa nei tessuti più profondi o nella sostanza bianca sotto la corteccia. Queste cellule mal posizionate mostravano inoltre segni di maturazione incompleta: alcune non esprimevano marcatori tipici dei neuroni degli strati superiori completamente sviluppati, pur senza trasformarsi in altri tipi cellulari come neuroni degli strati inferiori o glia. Questo indica che Med13 è necessario non solo perché i neuroni raggiungano la loro destinazione, ma anche perché assumano pienamente la loro identità corretta.
Ponti interrotti tra gli emisferi cerebrali
Il corretto funzionamento cerebrale dipende da connessioni a lungo raggio tra neuroni, comprese le fibre che attraversano la linea mediana attraverso il corpo calloso per collegare emisfero sinistro e destro. I ricercatori hanno scoperto che i neuroni privi di Med13 avevano proiezioni verso il lato opposto molto più scarse. Meno assoni penetravano nella regione appropriata della corteccia controlaterale, e questo deficit si accentuava con il progredire dello sviluppo. Allo stesso tempo, gli «alberi» dendritici che ricevono i segnali erano visibilmente più semplici: i neuroni privi di Med13 avevano meno rami e una lunghezza dendritica totale più corta. Complessivamente, questi cambiamenti indicano Med13 come un organizzatore chiave sia di dove i neuroni finiscono sia di quanto riccamente si connettono con i loro partner.
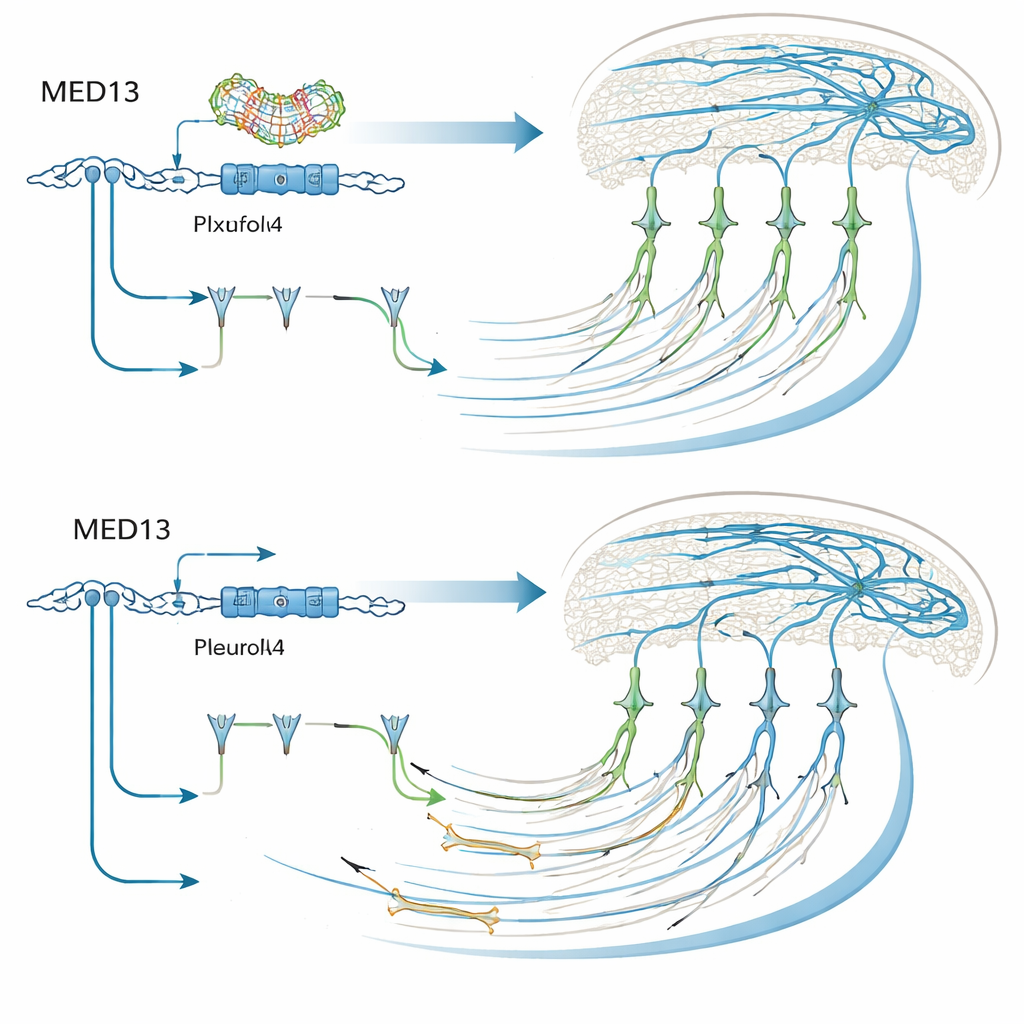
Dal controllo genico ai segnali guida
Med13 fa parte di un ampio complesso proteico che regola l’attivazione di molti altri geni, quindi gli autori hanno cercato i fattori a valle che potessero spiegare i suoi effetti. Utilizzando cellule umane simili a neuroni ingegnerizzate per essere prive di MED13, hanno catalogato migliaia di proteine e trovato oltre un centinaio i cui livelli cambiavano. Molte erano coinvolte nella forma neuronale, nel movimento e nello sviluppo corticale, e diverse si sovrapponevano con geni di rischio noti per disturbi dello sviluppo neurologico. Una in particolare è emersa come rilevante: PlxnA4, un recettore che aiuta i neuroni a rispondere a segnali guida durante la migrazione e l’estensione degli assoni. I livelli di PlxnA4 diminuivano in assenza di MED13, sia nelle cellule umane coltivate sia nei neuroni murini con Med13 ridotto. In modo notevole, forzare i neuroni a produrre PlxnA4 in eccesso poteva in larga misura risolvere i loro problemi di migrazione e ripristinare buona parte della proiezione callosale, anche quando Med13 era silenziato. Tuttavia, questo non correggeva l’architettura dendritica semplificata, il che implica che Med13 agisce anche attraverso altri bersagli per plasmare i rami neuronali.
Cosa significa per i disturbi cerebrali
Nel complesso, questi risultati dimostrano che Med13 aiuta i giovani neuroni corticali a spostarsi negli strati corretti e a formare connessioni a lunga distanza, in parte sostenendo la molecola guida PlxnA4. Quando Med13 è alterato, i neuroni si posizionano in modo errato, sviluppano meno i rami e inviano meno fibre attraverso il corpo calloso—tutti cambiamenti che riecheggiano alterazioni cerebrali osservate in alcuni disturbi dello sviluppo neurologico. Pur essendo chiaro che molti altri geni e segnali sono coinvolti, collocare Med13 come regolatore centrale offre un quadro più nitido di come alterazioni genetiche precoci possano propagarsi fino a modificare il cablaggio cerebrale e, in ultima analisi, il comportamento.
Citazione: Li, ZX., Tu, SX., Li, YW. et al. Med13 is involved in the radial migration and contralateral projection of cortical neurons via PlxnA4. Commun Biol 9, 394 (2026). https://doi.org/10.1038/s42003-026-09704-w
Parole chiave: sviluppo corticale, migrazione neuronale, corpo calloso, disturbi dello sviluppo neurologico, regolazione genica