Clear Sky Science · it
Dimostrazione di principio della terapia genica per NF1 in modelli murini xenoinnesto di neurofibroma plexiforme
Perché questa ricerca è importante
Le persone con la condizione genetica neurofibromatosi di tipo 1 (NF1) sviluppano spesso grandi tumori nervosi deformanti chiamati neurofibromi plexiformi. Queste formazioni possono causare dolore, problemi di movimento e gravi preoccupazioni estetiche, mentre le opzioni di trattamento attuali sono limitate e l’intervento chirurgico spesso non è praticabile. Poiché la NF1 è causata da alterazioni in un singolo gene, molti ricercatori hanno sperato che la terapia genica — riparare o sostituire il gene difettoso — possa un giorno ridurre o addirittura eliminare questi tumori. Questo studio propone un test iniziale ma incisivo di tale idea nei topi, ponendo una domanda semplice ma dalle grandi implicazioni: se si ripristina il gene NF1 mancante in tumori già stabiliti, questi scompaiono?
Costruire un modello tumorale realistico nei topi
I ricercatori avevano innanzitutto bisogno di un sistema di laboratorio che imitasse da vicino i neurofibromi plexiformi umani. Hanno utilizzato cellule di Schwann umane, le cellule di supporto che normalmente avvolgono i nervi, prelevate da una paziente le cui cellule avevano perso entrambe le copie funzionanti del gene NF1. Queste cellule sono state posizionate vicino ai nervi sciatici lesionati in topi immunocompromessi. Nel corso di settimane, i nervi hanno sviluppato in modo coerente tessuto ispessito, altamente cellulare, con struttura disorganizzata e bande dense di collagene — caratteristiche tipiche dei neurofibromi plexiformi. Interventi di controllo senza queste cellule carenti di NF1, o usando cellule con una sola copia difettosa di NF1, non hanno formato tumori in modo affidabile. Ciò ha dimostrato che le cellule umane con perdita completa di NF1 guidavano la crescita tumorale e ha creato un modello robusto e rapido della malattia.
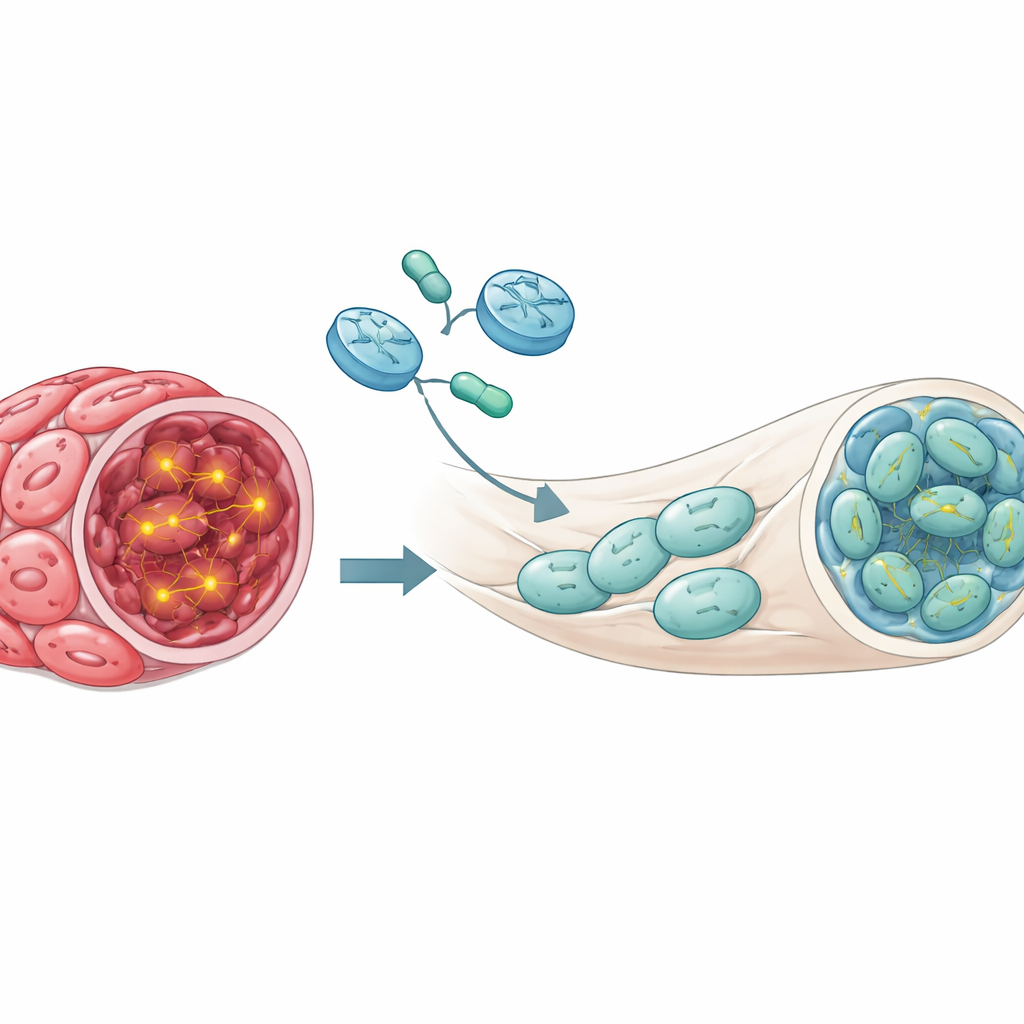
Riaccendere NF1 nelle cellule tumorali
Con questo modello a disposizione, il gruppo ha ingegnerizzato le cellule di Schwann tumorali per portare una versione commutabile del gene NF1 di topo. L’interruttore rispondeva al comune antibiotico doxiciclina: quando i topi bevevano acqua contenente doxiciclina, il gene NF1 aggiunto si attivava nelle cellule impiantate. I topi sono stati lasciati sviluppare i tumori e solo in seguito il gene è stato attivato. I risultati sono stati sorprendenti. Negli animali in cui NF1 rimaneva spento, la maggior parte dei nervi sciatici ospitava ancora neurofibromi. Al contrario, quando NF1 è stata riattivata, la maggior parte dei nervi appariva normale al microscopio e i marcatori chimici della segnalazione di crescita iperattiva erano fortemente ridotti. In sostanza, riaccendere NF1 ha spinto il tessuto tumorale verso uno stato nervoso sano.
Invertire la perdita di NF1 in un secondo modo
Per mostrare che questo effetto non dipendeva da un unico espediente di ingegneria, gli scienziati hanno costruito un secondo modello complementare. Questa volta hanno iniziato con cellule di Schwann umane che avevano solo una copia danneggiata di NF1 — simile a quanto ereditano le persone con NF1 in tutte le loro cellule. Hanno introdotto un interruttore genetico che poteva temporaneamente ridurre l’attività della copia rimanente di NF1 quando era presente doxiciclina. Quando i topi hanno bevuto doxiciclina, i livelli di NF1 sono calati ulteriormente e i tumori si sono formati con facilità. In modo cruciale, quando la doxiciclina è stata rimossa dopo lo sviluppo dei tumori, i livelli di NF1 sono risaliti e molti nervi sono tornati verso una struttura normale. Anche in questo caso, i parametri della segnalazione correlata alla crescita sono diminuiti nei nervi che si sono normalizzati. Insieme, queste due strategie opposte di commutazione — riaccendere NF1 o rimuovere la sua soppressione — convergono sulla stessa conclusione: ripristinare NF1 nelle cellule tumorali può annullare una malattia già stabilita.
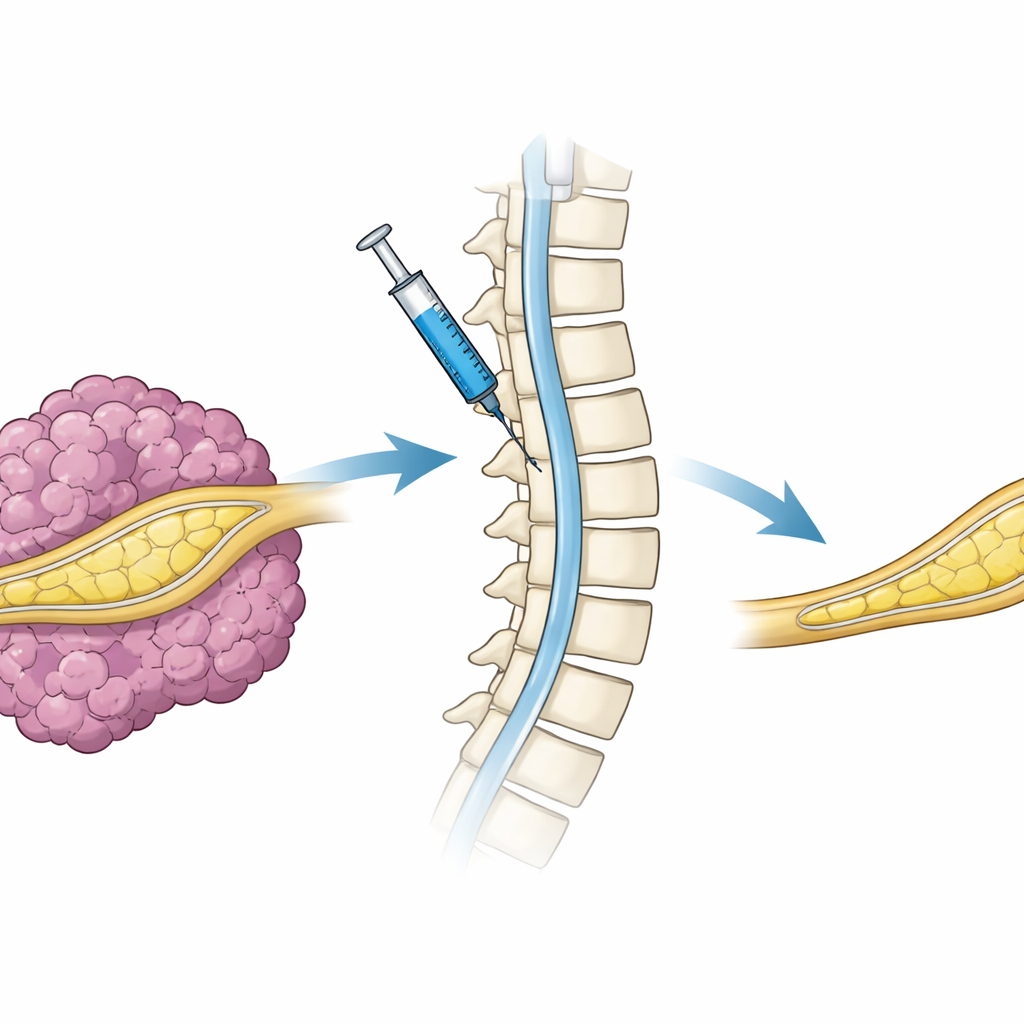
Testare un approccio di consegna più realistico
Oltre agli interruttori genetici inseriti nelle cellule in laboratorio, una vera terapia dovrebbe consegnare un gene NF1 funzionante nel sistema nervoso di un paziente vivo. Per esplorare questo passaggio, i ricercatori hanno impacchettato il gene NF1 completo in un vettore lentivirale e lo hanno iniettato nello spazio fluido intorno al midollo spinale dei topi portatori di tumori, una via nota come somministrazione intratecale. Gli animali hanno quindi ricevuto doxiciclina in modo che il gene consegnato si attivasse. Rispetto ai topi trattati con un virus di controllo, quelli ricevuto il virus contenente NF1 hanno sviluppato significativamente meno tumori e il loro tessuto nervoso è apparso più normale. Pur essendo un esperimento breve e con una singola dose, ha dimostrato che la somministrazione del gene NF1 attraverso il fluido spinale può raggiungere i nervi periferici e ridurre in modo significativo il carico tumorale.
Cosa significa questo lavoro per le persone con NF1
Questo studio non offre ancora una cura pronta per i pazienti, ma risponde a una domanda cruciale: in modelli murini progettati con cura che somigliano alle neurofibromatosi plexiformi umane, ripristinare NF1 nelle cellule tumorali può ridurre o normalizzare tumori già stabiliti. Il lavoro fornisce una dimostrazione di principio che la terapia genica per NF1 è una strategia plausibile, non solo una speranza teorica. Rimangono molte sfide — trovare i vettori più sicuri ed efficienti, determinare quanta attività di NF1 sia sufficiente e testare gli effetti a lungo termine in modelli più naturali. Tuttavia, questi risultati gettano una base scientifica per future terapie basate sui geni che potrebbero un giorno offrire sollievo duraturo dai neurofibromi plexiformi alle persone che vivono con NF1.
Citazione: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
Parole chiave: neurofibromatosi di tipo 1, terapia genica, neurofibroma plexiforme, cellule di Schwann, consegna lentivirale