Clear Sky Science · it
Base strutturale per il riconoscimento dei recettori nei pipistrelli da parte di SARS-CoV-2 e coronavirus simili a SARS2 nei pipistrelli
Perché questa storia pipistrello–virus è ancora importante
La pandemia di COVID-19 è iniziata più di sei anni fa, eppure gli scienziati stanno ancora ricostruendo come il virus che la causa, SARS-CoV-2, sia diventato così abile nell’infettare gli esseri umani. Un enigma centrale è come questo virus, e i suoi stretti parenti trovati nei pipistrelli, si leghino a una proteina chiamata ACE2 sulla superficie delle cellule—il primo e cruciale passo per l’infezione. Comprendere queste interazioni microscopiche a incastro può chiarire da dove proviene il virus, come si è adattato e cosa potrebbe accadere se virus correlati saltassero negli esseri umani in futuro. 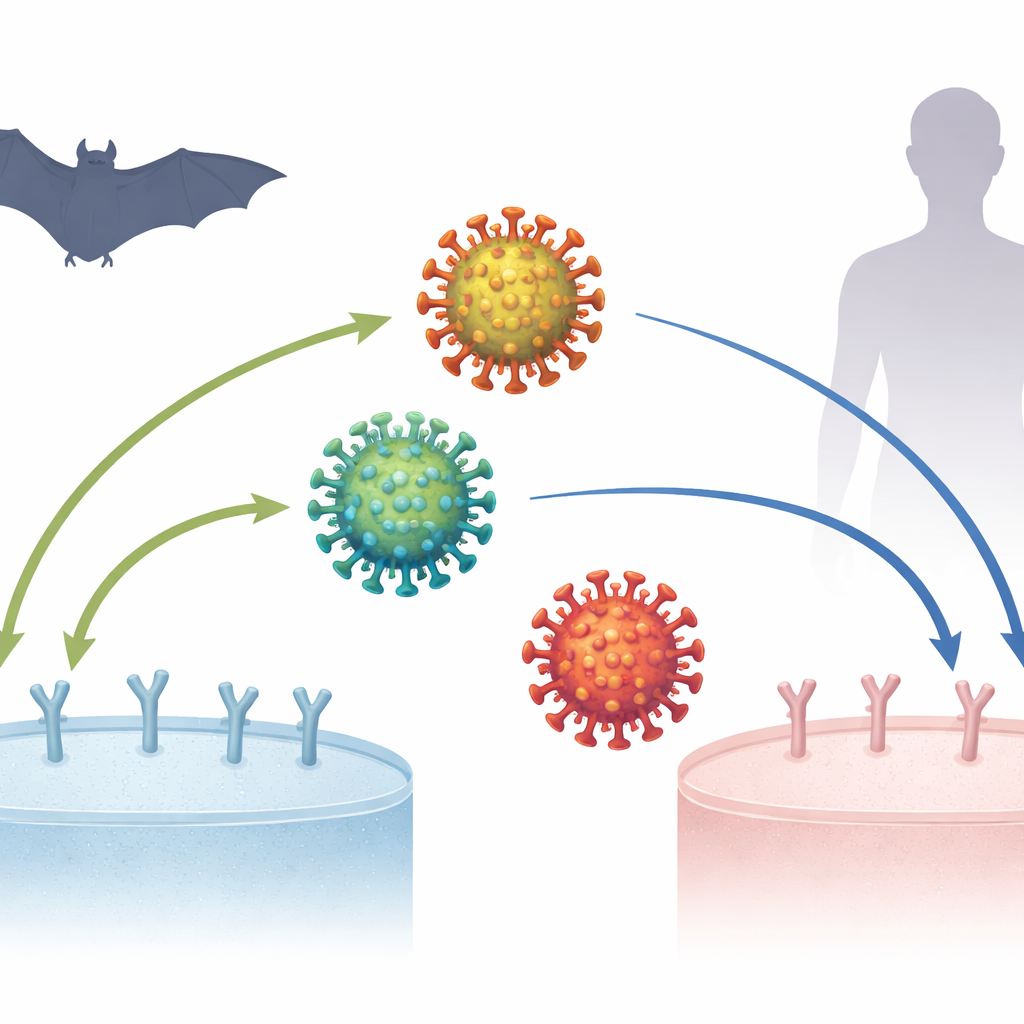
Osservare la stretta di mano virale
Lo studio si concentra sulla proteina spike, la struttura a corona sulla superficie del virus che afferra ACE2. Una piccola regione della spike, il dominio di legame al recettore (RBD), agisce come una punta che afferra la «manopola» ACE2. Lavori precedenti hanno mostrato che quando i coronavirus saltano tra specie—per esempio dai pipistrelli ai zibetti agli esseri umani—l’RBD spesso accumula mutazioni che migliorano la presa sull’ACE2 del nuovo ospite. Ma SARS-CoV-2 ha posto un enigma: la sua forma originale si legava già molto bene all’ACE2 umano, anche prima che si accumulasse molto tempo per l’adattamento, e alcuni virus di pipistrello correlati a SARS-CoV-2 sembravano legare l’ACE2 umano meglio che l’ACE2 dei pipistrelli. Ciò ha portato alcuni a chiedersi se SARS-CoV-2 fosse un’eccezione alle regole evolutive usuali.
Mettere alla prova i recettori di pipistrello e umano
Per sondare questo mistero, i ricercatori hanno esaminato due coronavirus di pipistrello strettamente correlati a SARS-CoV-2, noti come BANAL-52 e BANAL-236. Hanno confrontato quanto saldamente gli RBD di questi virus e di SARS-CoV-2 si attaccassero all’ACE2 umano e a quello di diverse specie di pipistrello. Usando saggi di legame cellulari, misurazioni ad alta precisione con biosensori e test di infezione con «pseudovirus» innocui, hanno trovato uno schema chiaro. L’RBD di BANAL-52 si legava più fortemente all’ACE2 di una specie di pipistrello, Rhinolophus sinicus, e leggermente meno all’ACE2 umano. L’RBD di SARS-CoV-2, al contrario, mostrava una preferenza modesta per l’ACE2 umano rispetto a quella dei pipistrelli. Complessivamente, l’RBD di BANAL-52 afferrava sia i recettori di pipistrello sia quelli umani più saldamente rispetto a SARS-CoV-2, ma risultava più finemente sintonizzato su quell’ACE2 di pipistrello in particolare. 
Come una singola modifica a scala atomica cambia l’equilibrio
Il gruppo si è poi rivolto alla cristallografia a raggi X, che rivela strutture a livello atomico, per vedere esattamente come il «dito» virale e la «manopola» ACE2 si toccano. Si sono concentrati su due posizioni chiave: una sull’RBD virale (chiamata residuo 498) e una sull’ACE2 (residuo 41). In BANAL-52, sia il sito virale sia il sito dell’ACE2 del pipistrello utilizzano lo stesso mattoncino, l’istidina, che permette un’interazione molto compatta e stratificata—impilamento come due monete e formazione anche di un legame a idrogeno. Nell’ACE2 umano, lo stesso punto contiene un mattoncino correlato ma leggermente diverso, la tirosina, che si impila comunque bene con l’istidina di BANAL-52 ma è priva del legame a idrogeno aggiuntivo. SARS-CoV-2 invece utilizza glutamina in questa posizione virale, che non può impilarsi nello stesso modo, risultando in un legame più debole sia con l’ACE2 dei pipistrelli sia con quello umano. Modificando deliberatamente questi amminoacidi nell’ACE2 dei pipistrelli, i ricercatori hanno confermato che rafforzare o indebolire questo singolo punto di contatto può invertire quale virus o ospite è favorito.
Perché l’ACE2 umano è una porta così accogliente
Oltre a questo singolo contatto, gli autori si sono chiesti perché l’ACE2 umano in generale sia un passaggio così efficiente per i coronavirus. Confrontando l’ACE2 di pipistrello e quella umana fianco a fianco, hanno identificato diverse caratteristiche specifiche dell’uomo che migliorano la stretta virale. Due posizioni sull’ACE2 umano, contenenti gli amminoacidi istidina (in posizione 34) e metionina (in posizione 82), creano legami a idrogeno più forti e zone «grasse» che aiutano l’RBD virale ad annidarsi più saldamente. Un altro residuo umano, treonina in posizione 27, in realtà rende il legame un po’ più debole rispetto alla versione dei pipistrelli, ma nel complesso i contatti favorevoli aggiuntivi prevalgono. Questi dettagli concordano con lavori precedenti che mostrano come l’ACE2 umano presenti più «hotspot» che lo rendono naturalmente un recettore attraente per un’ampia gamma di coronavirus.
Riformulare la storia dell’origine
Mettendo insieme tutti i dati, lo studio sostiene che SARS-CoV-2 e i suoi parenti nei pipistrelli seguono ancora il copione evolutivo usuale. La spike di BANAL-52 sembra meglio adattata all’ACE2 di certi pipistrelli, pur essendo compatibile con l’ACE2 umano. La spike di SARS-CoV-2, a sua volta, è meglio sintonizzata sull’ACE2 umano rispetto a quella dei pipistrelli, aiutata da punti di contatto speciali sul recettore umano. Piccoli cambiamenti in poche posizioni—in particolare al residuo virale 498 e sui siti vicini—possono spostare l’equilibrio di quale ospite sia favorito. Per i non specialisti, la conclusione è che non è necessario invocare spiegazioni esotiche: principi strutturali standard e ben compresi delle interazioni proteina–proteina sono sufficienti per spiegare come questi virus riconoscano le cellule di pipistrelli e umane, e sostengono un legame evolutivo stretto tra SARS-CoV-2 e i coronavirus correlati dei pipistrelli.
Citazione: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Parole chiave: Evoluzione di SARS-CoV-2, coronavirus dei pipistrelli, recettore ACE2, gamma di ospiti virali, legame della proteina spike