Clear Sky Science · it
La proteina codificata dal virus della peste suina africana MGF 505–3R compromette l’immunità innata tramite degradazione di MyD88 mediata dall’ubiquitina
Perché è importante per la salute animale e oltre
La peste suina africana ha devastato allevamenti di maiali in tutto il mondo, minacciando le riserve alimentari e causando ingenti perdite economiche. Il virus responsabile è particolarmente letale in parte perché sfugge ai sistemi di allerta precoce dell’organismo. Questo studio svela come una proteina virale, chiamata MGF 505–3R, saboti silenziosamente un interruttore chiave dell’allarme cellulare e mostra che un piccolo frammento di questa proteina può essere trasformato in uno strumento antinfiammatorio efficace nei topi.
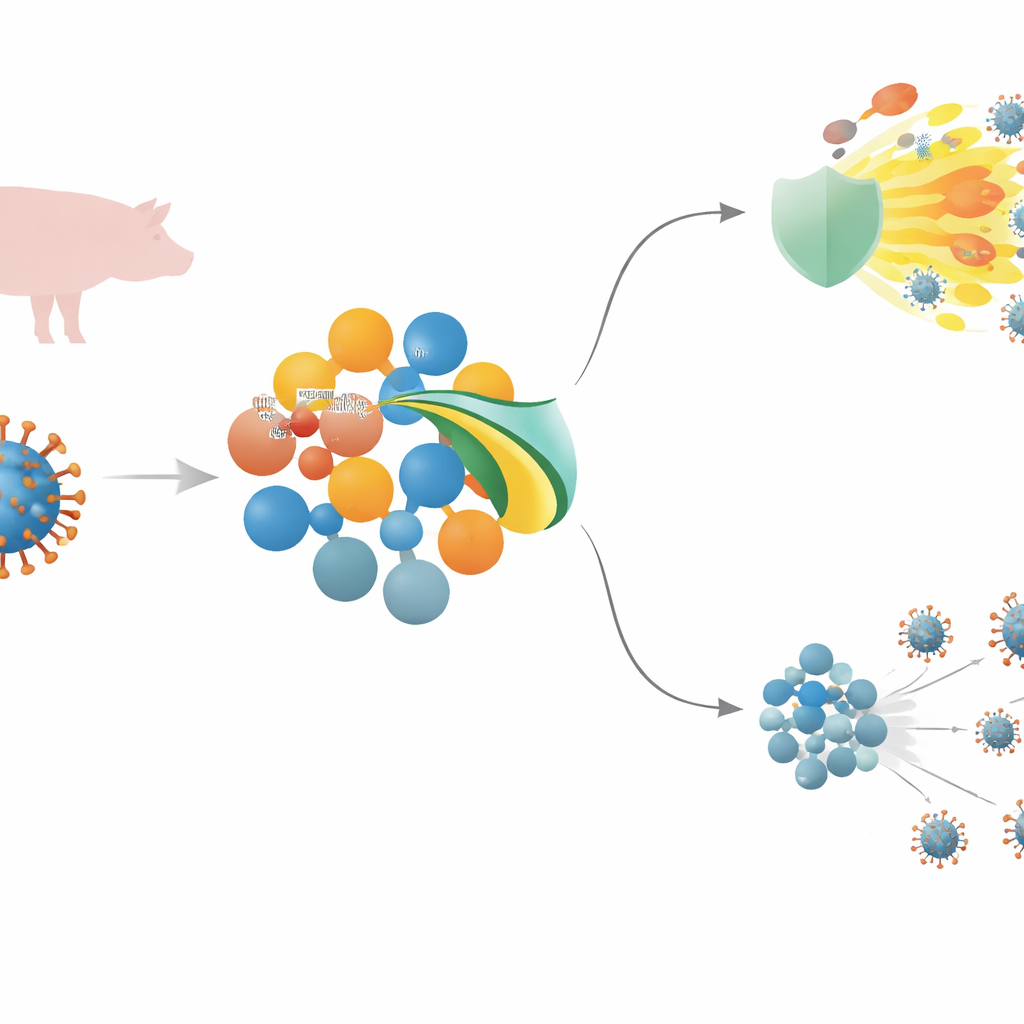
Un virus mortale per i suini e la prima linea di difesa dell’organismo
Il virus della peste suina africana (ASFV) è un grande virus a DNA che può uccidere quasi tutti i maiali infettati. Per impiantarsi deve eludere l’immunità innata — la difesa rapida e di primo livello che rileva gli invasori e innesca infiammazione e molecole antivirali. Al centro di questa risposta c’è una catena di segnalazione che include sensori sulla superficie cellulare, una proteina di collegamento chiamata MyD88 e un interruttore maestro noto come NF–κB, che insieme guidano la produzione di messaggeri infiammatori e interferoni antivirali. L’ASFV porta numerosi geni ritenuti in grado di interferire con questi segnali, ma per alcuni di essi, inclusa MGF 505–3R, i meccanismi esatti non erano ben compresi.
Come il virus taglia i fili dell’allarme immunitario
I ricercatori hanno esaminato le proteine dell’ASFV per valutarne la capacità di attenuare l’attività di NF–κB e hanno scoperto che MGF 505–3R è un inibitore particolarmente potente. Quando questa proteina virale era presente, le cellule esposte a diversi stimoli immunitari producevano molte meno citochine infiammatorie e livelli molto più bassi di interferoni di tipo I e III. Un’analisi più approfondita ha mostrato che MGF 505–3R agisce direttamente su MyD88, l’adattatore centrale che collega molti sensori immunitari a NF–κB. MGF 505–3R si lega a MyD88 e lo marca per la rimozione tramite il macchinario di degradazione proteica della cellula, usando una forma di etichettatura chiamata ubiquitinazione legata a K48. Man mano che MyD88 viene degradato, NF–κB non riesce a entrare nel nucleo e ad attivare i geni protettivi, rendendo le cellule più permissive alla replicazione virale.
Ingrandire un frammento piccolo ma potente di proteina
Per individuare la parte cruciale di MGF 505–3R, il gruppo ha prodotto versioni accorciate della proteina e ne ha testato gli effetti. Hanno scoperto che gli amminoacidi 89–277 erano sia necessari sia sufficienti per legare MyD88, promuoverne l’ubiquitinazione e bloccare l’attivazione di NF–κB. Guidati da previsioni computazionali della struttura proteica, hanno isolato due brevi peptidi da questa regione. Uno di essi, pep3R–1, si è distinto: ha ridotto nettamente l’attività di NF–κB, ha bloccato la fosforilazione e il transito nucleare della subunità p65 di NF–κB e ha abbassato l’espressione di citochine infiammatorie e interferoni in cellule immunitarie stimolate con molteplici segnali di pericolo. In colture cellulari, sia la MGF 505–3R a lunghezza intera sia pep3R–1 non solo attenuavano la segnalazione antivirale, ma permettevano anche a un virus di prova di replicarsi più efficacemente, sottolineando quanto potente sia questa via nel controllare le infezioni.
Trasformare un trucco virale in un possibile medicinale
Il team ha quindi valutato se il peptide potesse essere impiegato per calmare l’infiammazione dannosa piuttosto che favorire i virus. In un modello murino di colite indotta da un agente chimico chiamato DSS, gli animali normalmente perdono peso, sviluppano diarrea emorragica e mostrano gravi danni e infiltrazione di cellule immunitarie nel colon. I topi trattati con pep3R–1 hanno avuto esiti molto migliori: i punteggi di malattia erano inferiori, i coloni erano più lunghi e sani e l’esame microscopico ha rivelato una struttura tissutale preservata con molte meno cellule infiammatorie. I livelli di molecole chiave dell’infiammazione come TNF–α, IL–1β, IL–6 e di un enzima associato all’afflusso di leucociti sono risultati ridotti nei tessuti del colon e nel sangue. In un esperimento separato, pep3R–1 ha anche attenuato la risposta infiammatoria a una tossina batterica sistemica, indicando che può smorzare sia le tempeste infiammatorie locali sia quelle a livello dell’intero organismo.
Cosa significa per i maiali, le persone e i trattamenti futuri
Questo lavoro dimostra che la proteina ASFV MGF 505–3R aiuta il virus a prosperare smantellando un collegamento immunitario centrale, MyD88, spegnendo così sia le difese infiammatorie sia gli interferoni. Allo stesso tempo, un piccolo frammento di questa proteina virale, pep3R–1, può essere riproposto per moderare in sicurezza l’infiammazione eccessiva nei topi, incluso in un modello di malattia intestinale. Sebbene molto resti da fare — come migliorare stabilità, veicolazione e testare il peptide in altri contesti patologici — lo studio rivela sia un punto debole critico che le strategie antivirali potrebbero mirare a colpire, sia un promettente modello per progettare nuovi farmaci antinfiammatori peptidici ispirati all’evasione immunitaria virale.
Citazione: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Parole chiave: Peste suina africana, immunità innata, NF-kappaB, MyD88