Clear Sky Science · it
La proteina dell’involucro del ZIKV è un potente blocco della differenziazione direzionale precoce nella linea neuronale
Perché questo conta per i cervelli in crescita
Il virus Zika arrivò alle prime pagine per aver causato la nascita di bambini con teste insolitamente piccole e gravi danni cerebrali. Ma come può un’infezione nel corpo della madre deviare così potentemente i primissimi passaggi della costruzione del cervello nell’embrione? Questo studio si concentra su un singolo componente virale: la proteina dell’involucro che riveste le particelle del Zika, e indaga se quella proteina da sola possa disorientare la formazione delle cellule nervose. Ricreando in laboratorio le fasi iniziali dello sviluppo cerebrale con cellule staminali di topo, i ricercatori mostrano come questa proteina virale, in modo discreto ma potente, blocchi la normale costruzione dei circuiti neurali.
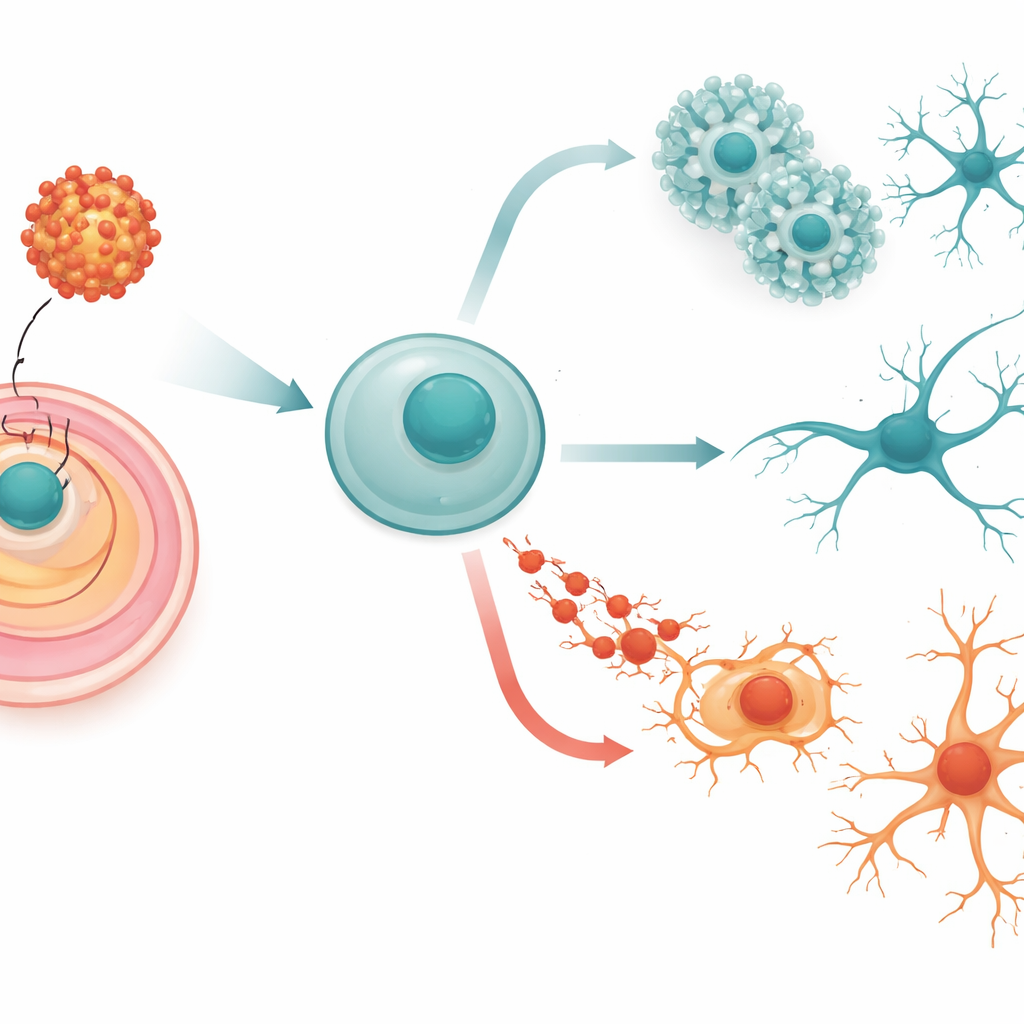
Dalle cellule starter flessibili alle future cellule nervose
I nostri cervelli iniziano come cellule semplici e altamente flessibili chiamate cellule staminali embrionali. Queste cellule possono trasformarsi in qualsiasi tessuto del corpo, ma nelle giuste condizioni seguono un percorso accuratamente coreografato verso la formazione di cellule nervose. Prima si impegnano nella via «neurale», poi formano strutture a rosetta che ricordano il sistema nervoso primitivo e infine maturano in neuroni che si connettono tramite lunghi processi ramificati. Il gruppo ha usato cellule staminali embrionali di topo come modello per queste fasi iniziali e le ha ingegnerizzate per produrre la proteina dell’involucro del Zika, con o senza una piccola modifica in un sito chiave di attacco degli zuccheri noto per influenzare la potenza del virus.
La proteina del rivestimento virale congela i primi passi della costruzione cerebrale
Quando le cellule staminali producevano la proteina dell’involucro del Zika, continuavano ad apparire sane e mantenevano la loro ampia potenzialità di generare diversi tessuti. Tuttavia, se lasciate differenziare liberamente, la loro capacità di formare complessi aggregati 3D che rappresentano i tre strati tissutali di base dell’embrione risultò fortemente ridotta, e i marcatori di tutti e tre gli strati diminuirono. Questo suggerisce che la proteina virale non uccide le staminali in modo diretto, ma interferisce sottilmente con la loro capacità di intraprendere i percorsi di sviluppo normali. Una versione mutante della proteina, priva di un particolare legame zuccherino, alterava questo quadro in maniera più disomogenea, lasciando intendere che la fine decorazione chimica della proteina modula il modo in cui danneggia lo sviluppo.
Ostruire la strada dalla cellula staminale al neurone
I ricercatori si sono poi concentrati sul percorso dalla cellula staminale al neurone precoce usando due modelli di laboratorio consolidati: una coltura piatta a «monostrato» e una coltura 3D a «neurosfera» che imita il tessuto cerebrale iniziale. In entrambi i sistemi, le cellule di controllo aumentavano in modo regolare l’espressione di marcatori di staminali neurali e di neuroni nel corso dei giorni, formando rosette organizzate e numerosi giovani neuroni. Le cellule che producevano la proteina dell’involucro, al contrario, generavano molte meno cellule staminali neurali, meno rosette e un numero molto inferiore di neuroni precoci, come evidenziato dai livelli ridotti di geni e proteine chiave legati all’identità nervosa. La forma mutante priva di zuccheri provocava in genere un blocco ancora più marcato a livello genico e attivava percorsi infiammatori di morte cellulare aggiuntivi, suggerendo una via verso un danno più grave.
Smorzare la comunicazione nelle giovani reti nervose
Per capire cosa stesse andando storto all’interno delle cellule, il gruppo ha confrontato l’attività genica globale in cellule normali e in cellule produttrici dell’involucro in fasi critiche della differenziazione. Hanno riscontrato che molti geni legati alla crescita neurale, alla formazione delle sinapsi e alle piccole spine dendritiche che conservano i ricordi risultavano soppressi. Anche le vie coinvolte nel carico e nel rilascio dei neurotrasmettitori, nel collegamento degli assoni ai loro bersagli e nell’assemblaggio delle sinapsi erano tutte attenuate. Allo stesso tempo, venivano attivate vie di segnalazione collegate al calcio e ad alcuni recettori di superficie cellulare, potenzialmente rendendo le cellule iper‑eccitabili o con segnali errati. Questi cambiamenti estesi apparivano sia nelle colture piatte sia in quelle 3D, dimostrando che la proteina dell’involucro devia ripetutamente le cellule neurali in sviluppo dal costruire reti robuste e ben connesse.
Cosa significa per i difetti congeniti legati allo Zika
Per i non specialisti, il messaggio chiave è che il virus Zika non deve necessariamente moltiplicarsi attivamente e uccidere le cellule per danneggiare il cervello in sviluppo. Questo lavoro dimostra che la sua proteina esterna dell’involucro da sola può deviare le cellule staminali precoci dal percorso normale verso i neuroni e può indebolire i programmi genetici necessari a formare sinapsi sane e spine dendritiche. Disruptions così precoci e silenziose aiutano a spiegare come l’esposizione in utero possa portare a condizioni come la microcefalia e a problemi cognitivi a lungo termine. I risultati mettono inoltre in guardia sul fatto che vaccini o terapie che impiegano proteine dell’involucro virale devono essere valutati con attenzione per i possibili effetti sullo sviluppo cerebrale, anche in assenza di virus vivo.
Citazione: Ma, ZH., Wang, Y., Hassaan, N.A. et al. ZIKV envelope protein is a strong blocker of early directional differentiation in the neural lineage. Commun Biol 9, 395 (2026). https://doi.org/10.1038/s42003-026-09672-1
Parole chiave: virus Zika, sviluppo cerebrale, cellule staminali neurali, proteina dell’involucro virale, microcefalia