Clear Sky Science · it
Attivazione del recettore accoppiato a proteine G codificato dal citomegalovirus UL33 da parte di un peptide N‑terminal innato
Come un virus comune riorganizza le nostre cellule
Il citomegalovirus umano (HCMV) infetta silenziosamente la maggior parte delle persone e di solito passa inosservato. Tuttavia, nei neonati, nei pazienti trapiantati e in chi ha un sistema immunitario indebolito può provocare malattia grave. Questo studio rivela, a livello molecolare, come una proteina virale chiamata UL33 si comporti da interruttore interno che spinge costantemente le cellule infette a favore del virus. Comprendere questo interruttore nascosto aiuta a spiegare come l'HCMV persista per tutta la vita e indica nuove vie per disarmarlo senza danneggiare la normale segnalazione cellulare.
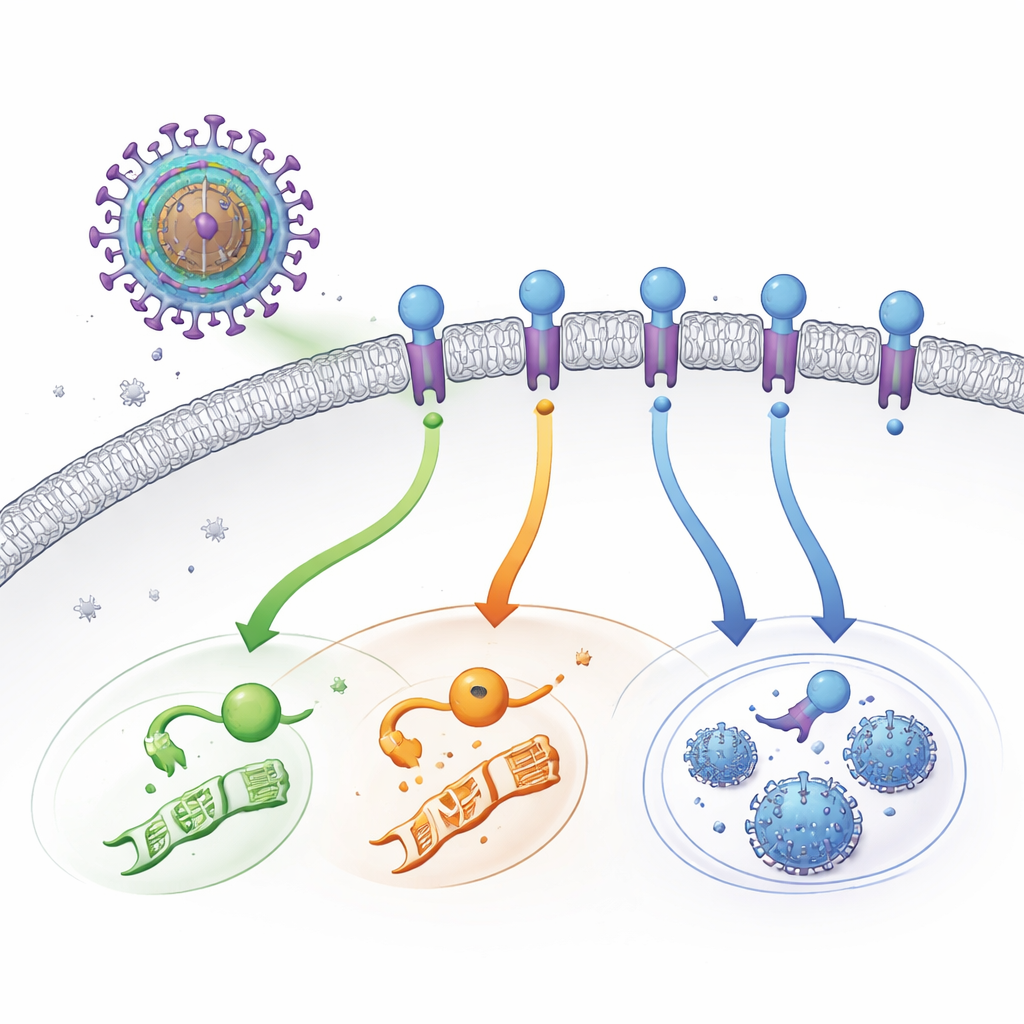
Uno switch virale furtivo sulla superficie cellulare
L'HCMV porta le proprie versioni di recettori di superficie cellulare—proteine che normalmente percepiscono ormoni o segnali immunitari. UL33 è uno di questi recettori virali. Diversamente dai recettori tipici, che attendono un segnale esterno, UL33 è “sempre attivo”. Una volta inserito nella membrana esterna di una cellula infetta, può agganciarsi contemporaneamente a più delle principali vie di comunicazione cellulare. Queste vie controllano processi come l’attività genica, il metabolismo e la decisione di entrare in latenza o di produrre nuovo virus. Per anni, gli scienziati sapevano che UL33 era attivo ma non capivano cosa lo attivasse, soprattutto perché non era mai stato trovato un ligando esterno che lo stimolasse.
Un auto‑avviatore: il recettore che porta la propria chiave
Utilizzando avanzate ricostruzioni in crio‑microscopia elettronica, gli autori hanno catturato istantanee tridimensionali di UL33 legato a uno dei partner di segnalazione della cellula, una proteina G chiamata Gs. Le immagini mostrano che l’estremità iniziale della proteina UL33—la sua breve coda N‑terminale—si ripiega in una tasca dello stesso recettore, come una chiave lasciata permanentemente nella serratura. Questa coda “anclata” si inserisce in una piccola tasca laterale che, nei recettori umani correlati, normalmente accoglierebbe parte di una proteina di segnalazione immunitaria chiamata chemochina. Occupando questa tasca dall’interno, UL33 impedisce alle chemochine esterne di legarsi del tutto, spiegando perché si comporta da recettore “orfano” che non risponde ai normali messaggeri dell’ospite.
Atomi cruciali nell’interruttore virale
Per confermare che questa coda interna è davvero il grilletto, il team ha alterato sistematicamente singoli mattoni di UL33 in cellule umane. Si sono concentrati sui primi amminoacidi della coda e sui punti corrispondenti all’interno della tasca che la trattengono. Quando hanno sostituito questi residui chiave con altri più neutri o ne hanno rimosso uno del tutto, la capacità di segnalazione di UL33 è crollata quasi a zero—anche se i recettori mutati raggiungevano la superficie cellulare in quantità normali. In altre parole, la proteina era presente ma muta. Ciò dimostra che la coda non è solo un elemento strutturale; è il pezzo auto‑attivante essenziale che mantiene UL33 acceso.
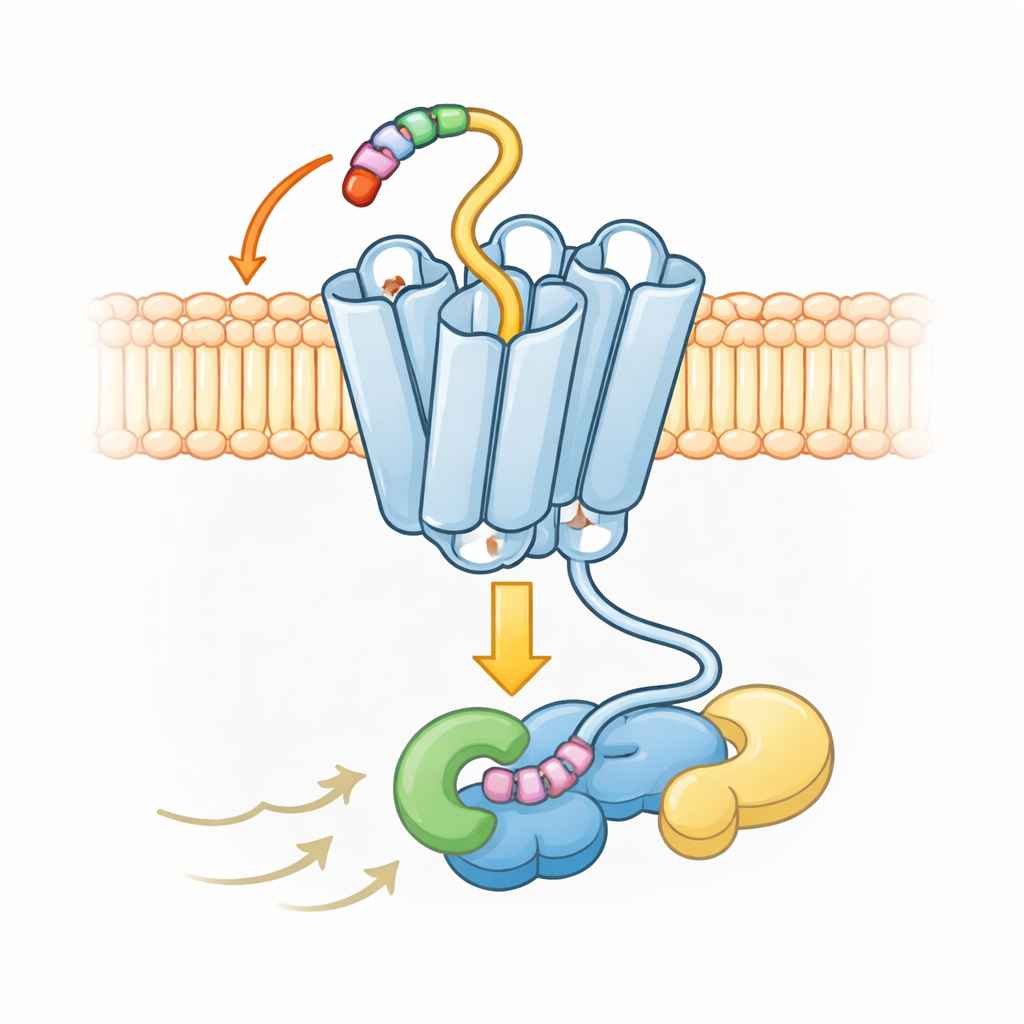
Una forma insolita per una segnalazione ampia ma controllata
Le mappe strutturali rivelano inoltre che UL33 adotta una conformazione attiva leggermente diversa rispetto ai recettori umani tipici. Nella maggior parte dei recettori di questa famiglia, una delle sette eliche vicino all’interno della cellula si sposta drasticamente verso l’esterno quando il recettore è attivato, aprendo una grande cavità per l’ingaggio delle proteine G. In UL33, quell’elica rimane molto più vicina al centro, creando un incastro più stretto. Nonostante ciò, UL33 può ancora interagire con diversi tipi di proteine G—Gs, Gq e Gi—stabilendo contatti precisi con la punta della proteina G che si inserisce nel recettore. Questi contatti favoriscono alcune proteine G ed escludono altre, come il gruppo G12/13, permettendo al virus di orientare le risposte cellulari senza scatenare una segnalazione incontrollata.
Nuove vulnerabilità per un vecchio virus
Combinando immagini strutturali con test funzionali, lo studio dipinge un quadro chiaro: UL33 è un recettore virale auto‑avviante la cui coda funge da attivatore permanentemente legato. Questo disegno permette all'HCMV di modulare in modo sottile ma persistente la segnalazione delle cellule ospiti per favorire la replicazione virale e la riattivazione, soprattutto potenziando vie che attivano i geni virali. Allo stesso tempo, il lavoro mette a nudo punti deboli che i farmaci potrebbero sfruttare, come un tunnel stretto che conduce nella tasca dove si lega la coda. Molecole progettate per incuneare questa regione o sbloccare la coda potrebbero attenuare l’attività di UL33 e ridurre il danno virale, risparmiando i recettori normali dell’organismo. Per i pazienti a rischio da HCMV, mirare a questo “interruttore maestro” virale potrebbe un giorno offrire un modo più preciso per controllare il virus.
Citazione: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Parole chiave: citomegalovirus, GPCR virale, segnalazione cellulare, struttura crio‑EM, target farmacologico