Clear Sky Science · it
La privazione del sonno interrompe l’omeostasi della ghiandola lacrimale tramite l’asse ipotalamo-ipofisi-surrene e la disbiosi intestinale nei topi
Perché la mancanza di sonno può far sentire gli occhi sabbiosi
La maggior parte delle persone sa che dormire poco può lasciare stanchi e confusi il giorno dopo. Meno evidente è che la perdita cronica di sonno può anche danneggiare silenziosamente le ghiandole che mantengono i nostri occhi confortevoli e protetti. Questo studio sui topi esplora come la privazione di sonno prolungata secchi la superficie oculare disturbando gli ormoni dello stress e i microbi intestinali, e indica possibili strategie per preservare la vista in un mondo senza sonno. 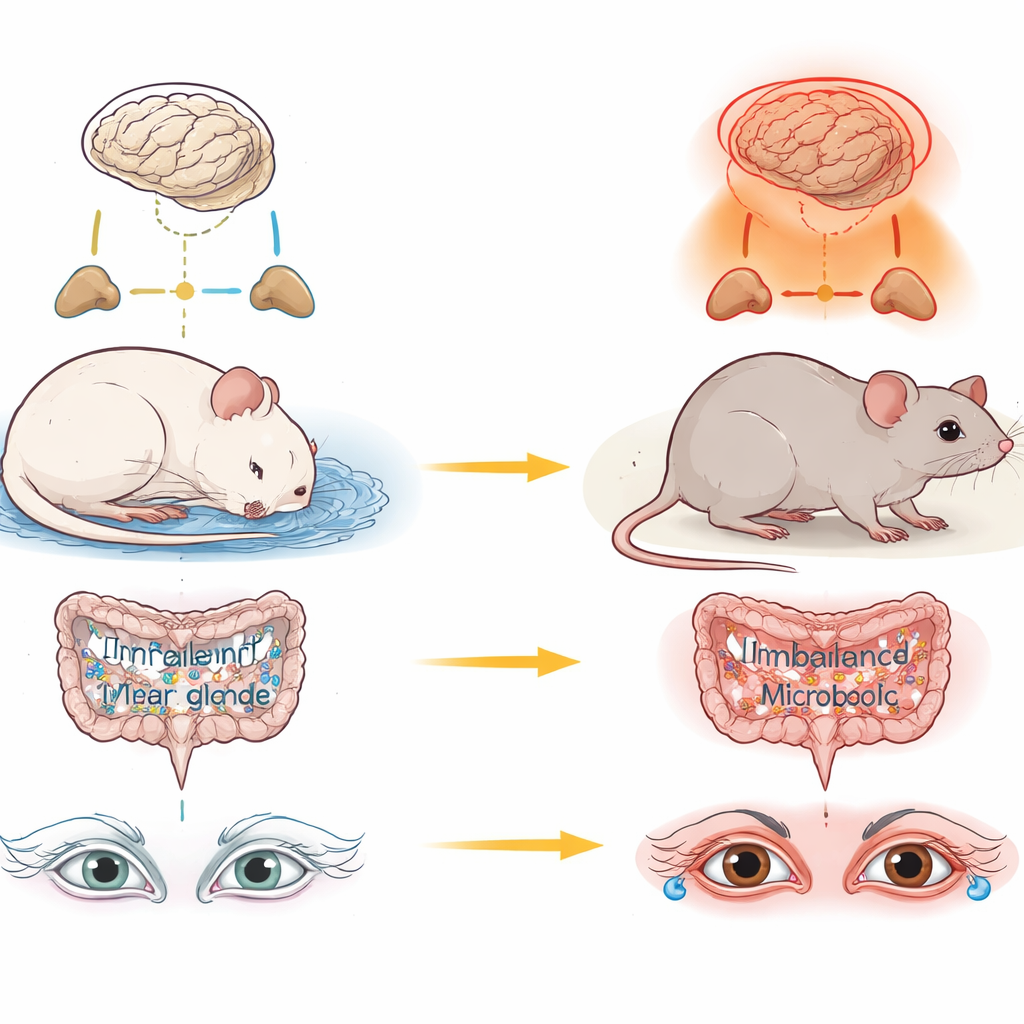
Una catena nascosta dal cervello all’intestino fino all’occhio
I ricercatori si sono concentrati sulle ghiandole lacrimali, piccole strutture vicino agli occhi che producono lo strato acquoso delle nostre lacrime. Quando il team ha tenuto svegli i topi per settimane usando un sistema automatico e delicato, gli animali hanno prodotto meno lacrime e le loro ghiandole lacrimali si sono ridotte e hanno perso la normale struttura cellulare. Allo stesso tempo, l’attività genica in queste ghiandole si è spostata marcatamente verso programmi immunitari e infiammatori, incluso un potente percorso guidato da una molecola chiamata IL-17. In termini semplici, le ghiandole che dovrebbero irrigare l’occhio con calma cominciarono invece a somigliare e a comportarsi come tessuto irritato e infiammato.
Gli ormoni dello stress aumentano il danno
La perdita di sonno è un noto attivatore del principale circuito dello stress del corpo, chiamato asse ipotalamo–ipofisi–surrene, che termina con il rilascio di ormoni dello stress dalle ghiandole surrenali. Nei topi privati del sonno, i livelli dello steroide corticosterone sono aumentati e le stesse ghiandole surrenali mostravano segni di attivazione immunitaria. Quando gli scienziati hanno somministrato un farmaco chiamato metyrapone per bloccare la produzione di questi ormoni dello stress, gran parte del danno si è ridotta: le ghiandole lacrimali hanno mantenuto dimensioni e struttura più normali, la produzione di lacrime è migliorata e le cellule immunitarie infiammatorie erano meno numerose. Ciò suggerisce che la segnalazione dello stress iperattiva non è solo un effetto collaterale della perdita di sonno, ma un fattore determinante del danno alle ghiandole oculari.
Microbi intestinali fuori equilibrio
Il team si è poi rivolto all’intestino, dove trilioni di microrganismi aiutano a digerire il cibo e a “istruire” il sistema immunitario. La privazione cronica di sonno ha reso la parete intestinale più permeabile e ha alterato notevolmente la composizione dei batteri intestinali. I livelli di acidi grassi a catena corta — piccole molecole prodotte da microbi benefici che contribuiscono a contenere l’infiammazione — sono diminuiti sia nell’intestino sia nel sangue. Quando i ricercatori hanno eliminato i batteri intestinali con antibiotici, il danno alle ghiandole lacrimali è peggiorato, suggerendo che una comunità microbica sana aiuta normalmente a proteggere l’occhio. 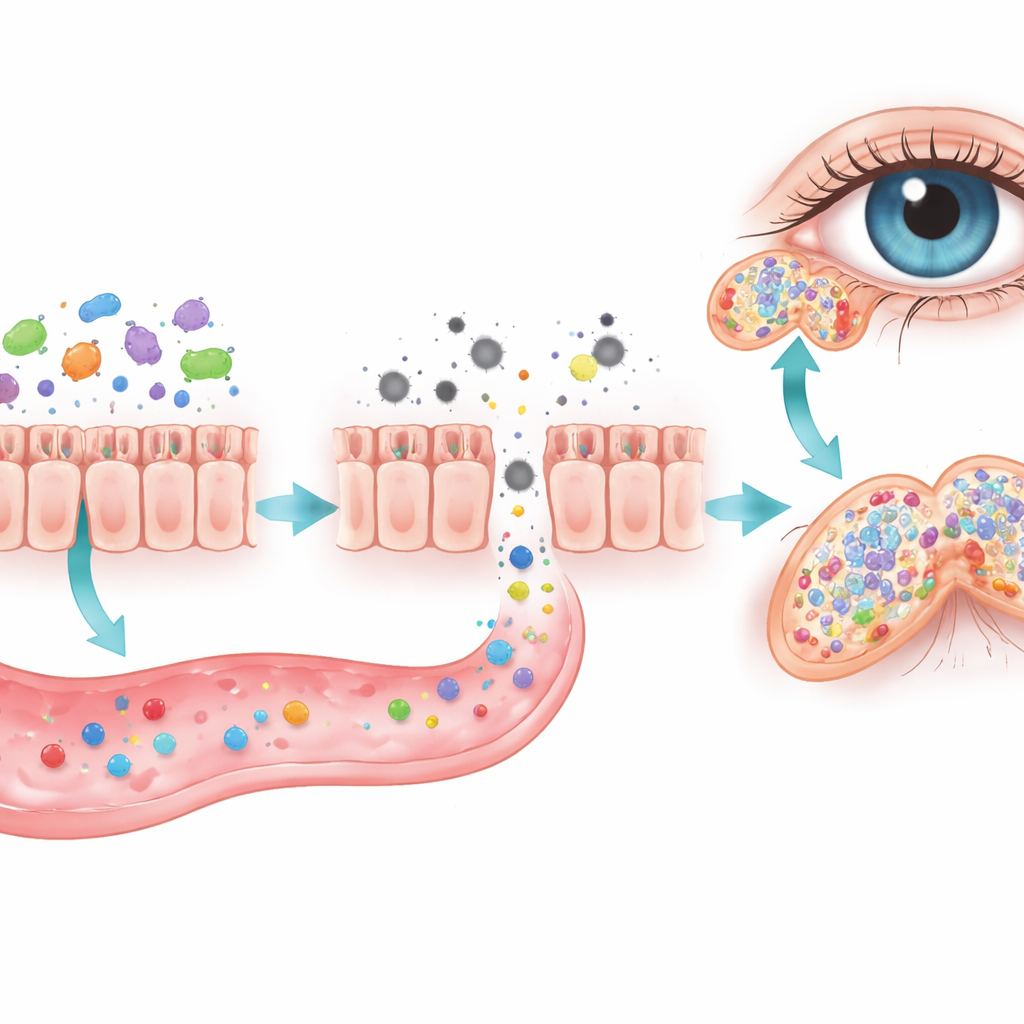
Ripristinare i microbi e i loro metaboliti utili
Per verificare se rimettere a posto l’intestino potesse salvare gli occhi, gli scienziati hanno provato due strategie. In una, hanno trapiantato microbi intestinali da topi sani in animali privati del sonno. Nell’altra, hanno reintegrato una miscela di acidi grassi a catena corta nell’acqua da bere. Entrambi gli approcci hanno parzialmente ripristinato comunità intestinali normali, aumentato questi metaboliti benefici e attenuato il danno alle ghiandole lacrimali. La produzione di lacrime è aumentata, la struttura delle ghiandole è migliorata e le cellule immunitarie infiltrate sono diminuite. Fondamentalmente, tutti e tre gli interventi — il blocco degli ormoni dello stress, il trapianto microbico e la supplementazione di acidi grassi a catena corta — hanno convergito nel ridurre l’infiammazione correlata a IL-17 nelle ghiandole.
Cosa significa per occhi stanchi
Nel complesso, il lavoro delinea un “asse” che collega stress guidato dal cervello, microbi intestinali e ghiandole lacrimali. In questo modello, la perdita cronica di sonno iperattiva gli ormoni dello stress, altera l’ecosistema intestinale, esaurisce i prodotti microbici lenitivi e rende più permeabile la barriera intestinale. Segnali che filtrano dall’intestino contribuiscono quindi a innescare un’infiammazione centrata su IL-17 nelle ghiandole lacrimali, facendole rimpicciolire e riducendo la produzione lacrimale. Sebbene lo studio sia stato condotto su topi maschi, i risultati suggeriscono la possibilità che un sonno migliore, un controllo accurato dello stress e future terapie basate sul microbioma possano un giorno aiutare a proteggere le persone affette da occhio secco e altri problemi oculari legati al sonno.
Citazione: Huang, S., Yu, S., Zhang, W. et al. Sleep deprivation disrupts lacrimal gland homeostasis via hypothalamic-pituitary-adrenal axis and gut dysbiosis in mice. Commun Biol 9, 367 (2026). https://doi.org/10.1038/s42003-026-09657-0
Parole chiave: privazione del sonno, occhio secco, microbioma intestinale, ormoni dello stress, acidi grassi a catena corta