Clear Sky Science · it
Indagare le risposte dei biofilm di Salmonella al trattamento antibiotico usando la spettroscopia ottica fototermica a infrarossi
Perché le città adesive di germi sono importanti
Molti batteri patogeni preferiscono vivere in comunità molto dense chiamate biofilm, dove le cellule aderiscono tra loro e alle superfici all’interno del corpo o sui dispositivi medici. All’interno di queste “città” vischiose, i microbi possono resistere ad antibiotici che normalmente li ucciderebbero. Questo studio presenta un nuovo modo di osservare i biofilm in dettaglio, rivelando quali cellule sono attivamente in crescita e come reagiscono quando vengono aggiunti farmaci potenti. Comprendere questi modelli di attività invisibili potrebbe aiutare i medici a progettare terapie che finalmente spezzino le tenaci difese dei biofilm.
Vita nascosta dentro le città batteriche
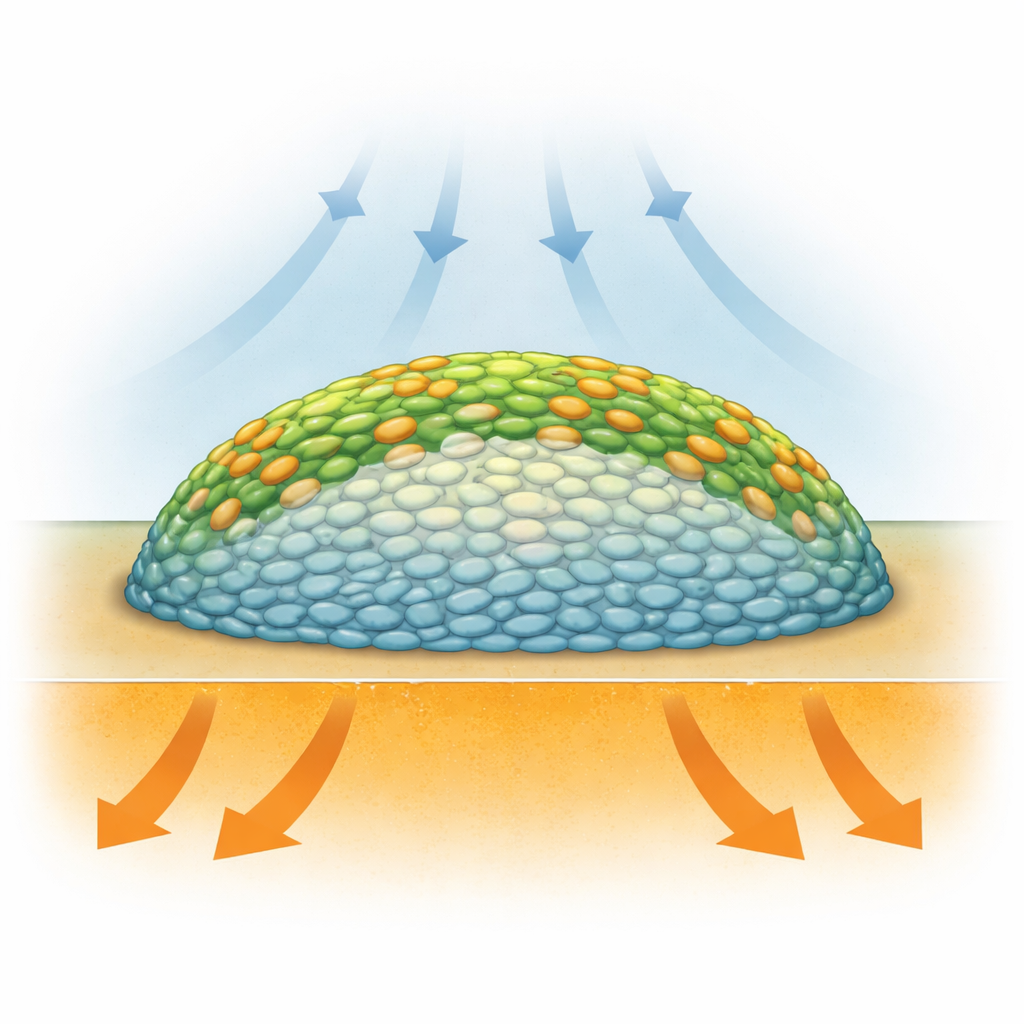
I biofilm non sono solo ammassi casuali di germi: sono strutture stratificate dove i batteri vivono in condizioni molto diverse a seconda della loro posizione. Le cellule in superficie hanno maggiore accesso all’ossigeno dall’aria, mentre quelle sepolte al centro sono prive di ossigeno e possono rallentare o andare in uno stato di quiescenza. Metodi precedenti come la microscopia a fluorescenza potevano mostrare la struttura, ma spesso richiedevano coloranti aggiunti o marcatori genetici che potevano perturbare la biologia, e non misuravano direttamente cosa facessero chimicamente le cellule. I ricercatori avevano bisogno di un modo per “vedere” la chimica dei biofilm vivi, strato per strato, senza distruggerli o alterarne pesantemente le condizioni.
Vedere la chimica con la luce invisibile
Il team si è rivolto a una tecnica chiamata spettroscopia ottica fototermica a infrarossi (O-PTIR), che usa impulsi di luce infrarossa invisibile e un laser visibile per rilevare piccole vibrazioni nelle molecole. Queste vibrazioni fungono da impronte digitali dei componenti chiave delle cellule, come proteine, lipidi e DNA. Per tracciare il metabolismo — l’uso attivo dei nutrienti — hanno nutrito i biofilm di Salmonella Typhimurium con una forma speciale di zucchero in cui gli atomi di carbonio erano leggermente più pesanti del normale (un isotopo stabile noto come carbonio-13). Quando le cellule sono attive nella crescita e nella sintesi di nuove proteine, incorporano questi atomi più pesanti nelle loro strutture, causando spostamenti sottili ma rilevabili nel segnale infrarosso. Congelando e sezionando il biofilm e scansionando sottili sezioni trasversali, i ricercatori hanno prodotto mappe chimiche che mostrano dove nel biofilm questo carbonio pesante era stato incorporato.
Anelli di attività e nuclei silenziosi
Le immagini a infrarossi dei biofilm di Salmonella non trattati hanno rivelato un pattern sorprendente: le regioni esterne e gli strati di superficie mostravano forte incorporazione del carbonio pesante, mentre un ampio nucleo centrale mostrava pochissimo. In altre parole, il biofilm si comportava come un anello di cellule attive che circondava un interno silenzioso. L’analisi statistica degli spettri infrarossi ha confermato che i segnali delle vibrazioni correlate alle proteine si spostavano più negli strati esterni che nel centro, indicando una maggiore produzione proteica ai bordi. Questi risultati supportano l’idea che la disponibilità di ossigeno, maggiore vicino alla superficie, sia il principale motore delle “zone calde” metaboliche in questo modello coloniale, nonostante i nutrienti defluiscano dal basso. Lo studio ha fornito una delle visualizzazioni più chiare e ad alta risoluzione finora di come il metabolismo sia stratificato all’interno di un biofilm.
Come differenti antibiotici rimodellano l’attività del biofilm
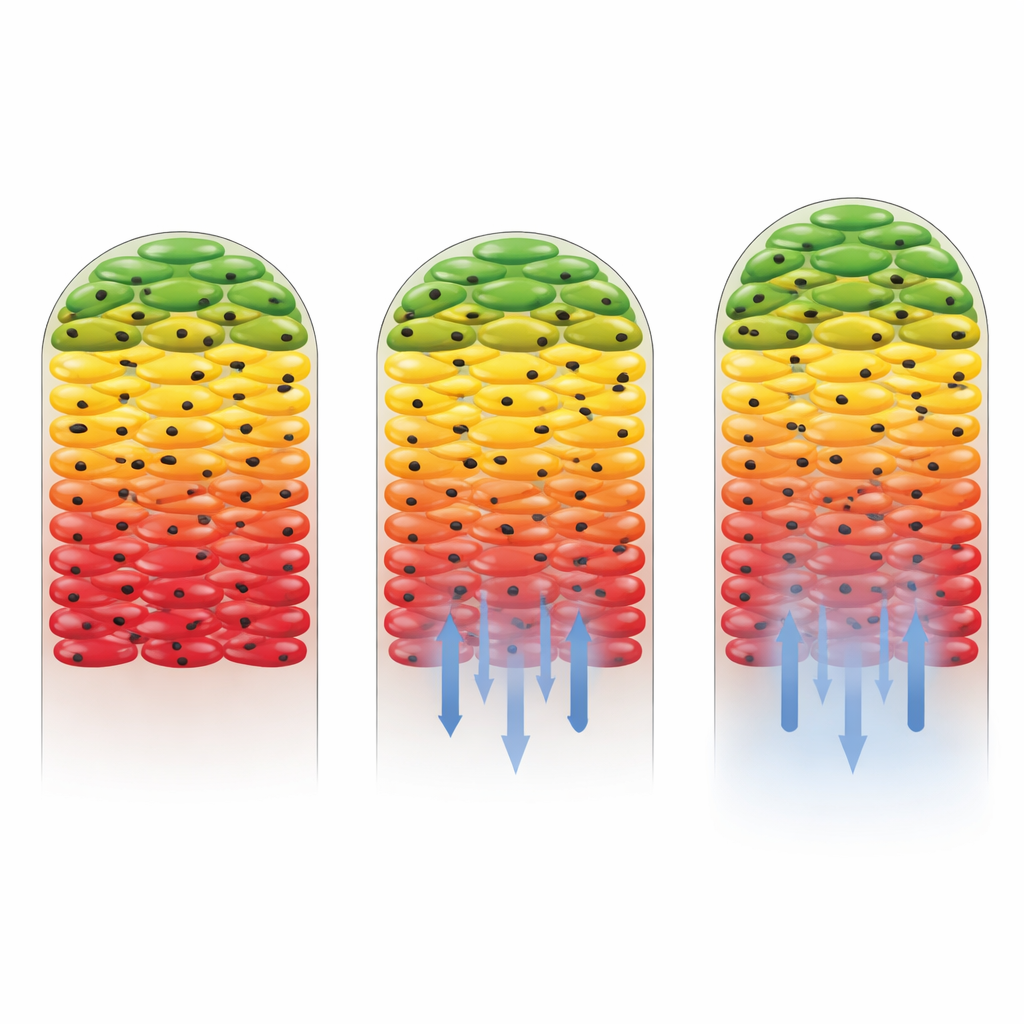
I ricercatori hanno poi chiesto cosa accade quando vengono introdotti antibiotici. Hanno usato due farmaci: kanamicina, a cui il ceppo di Salmonella è sensibile, e gentamicina, verso la quale il ceppo era stato ingegnerizzato per essere in gran parte non suscettibile. Quando era presente la gentamicina, il quadro complessivo degli strati esterni attivi e di un nucleo silenzioso è cambiato poco, mostrando che le cellule resistenti continuavano a crescere e a incorporare carbonio pesante in gran parte del biofilm. Al contrario, la kanamicina ha ridotto drasticamente l’attività metabolica, soprattutto vicino al fondo del biofilm dove la concentrazione del farmaco era più alta. Solo una sottile fascia di cellule più lontane dalla fonte dell’antibiotico mostrava ancora segni di assimilazione del carbonio. Questo ha rivelato non solo che il farmaco era efficace, ma anche che la struttura stessa del biofilm aiutava a proteggere alcune cellule indebolendo il farmaco man mano che diffondeva verso l’interno.
Nuove finestre per trattare infezioni difficili
Da un punto di vista divulgativo, il messaggio chiave è che questo lavoro offre un potente “microscopio chimico” per osservare come le comunità batteriche vivono e sopravvivono ai trattamenti in tre dimensioni. Combinando un metodo di imaging a infrarossi non distruttivo con una forma sicura di carbonio pesante, i ricercatori sono stati in grado di individuare dove i batteri crescevano attivamente e come quell’attività cambiava sotto diversi antibiotici. I loro risultati confermano che i biofilm ospitano un mix di cellule attive e quasi dormienti, e che farmaci efficaci possono comunque essere attenuati dalla barriera fisica del biofilm. In futuro, questo approccio potrebbe essere usato per testare nuove terapie, esplorare come diverse specie cooperino o condividano la resistenza all’interno di biofilm misti e, in ultima analisi, aiutare a progettare strategie più intelligenti per eliminare infezioni persistenti.
Citazione: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Parole chiave: biofilm, Salmonella, resistenza agli antibiotici, immagine a infrarossi, sondaggio con isotopi stabili