Clear Sky Science · it
Selezione dei modelli nella ricerca preclinica sulle terapie con acidi nucleici
Trasformare i geni in farmaci
Le terapie con acidi nucleici sono una nuova classe di medicinali che non agiscono bloccando le proteine, come fanno la maggior parte dei farmaci, ma intervenendo un livello prima, sui messaggi genetici. Questa recensione spiega come gli scienziati scelgono i modelli di laboratorio e animali più adatti per testare questi farmaci che prendono di mira l'RNA prima che raggiungano i pazienti. Un lettore non specialista potrebbe interessarsene perché scelte intelligenti dei modelli possono significare trattamenti più rapidi, più sicuri e più efficaci per malattie genetiche, incluse patologie rare dell'infanzia e condizioni più comuni come le malattie cardiovascolari.
Che cosa rende diverse queste medicine genetiche?
Le terapie con acidi nucleici (NAT) comprendono brevi filamenti chiamati oligonucleotidi antisenso (ASO) e piccoli RNA interferenti (siRNA). Piuttosto che basarsi sulla forma e sulla chimica dei target proteici, questi farmaci riconoscono i loro bersagli tramite regole di appaiamento delle basi—lo stesso abbinamento A‑T e G‑C alla base del DNA. Questo li rende programmabili: una volta nota la sequenza di RNA che si vuole modificare, spesso è possibile progettare rapidamente molti candidati senza anni di chimica tradizionale. La parte difficile non è più «possiamo creare un composto attivo?» bensì «come misuriamo se funziona davvero in un contesto biologico realistico?» Poiché anche una singola lettera di differenza nella sequenza può determinare l'attività, la scelta dei sistemi di prova diventa critica.
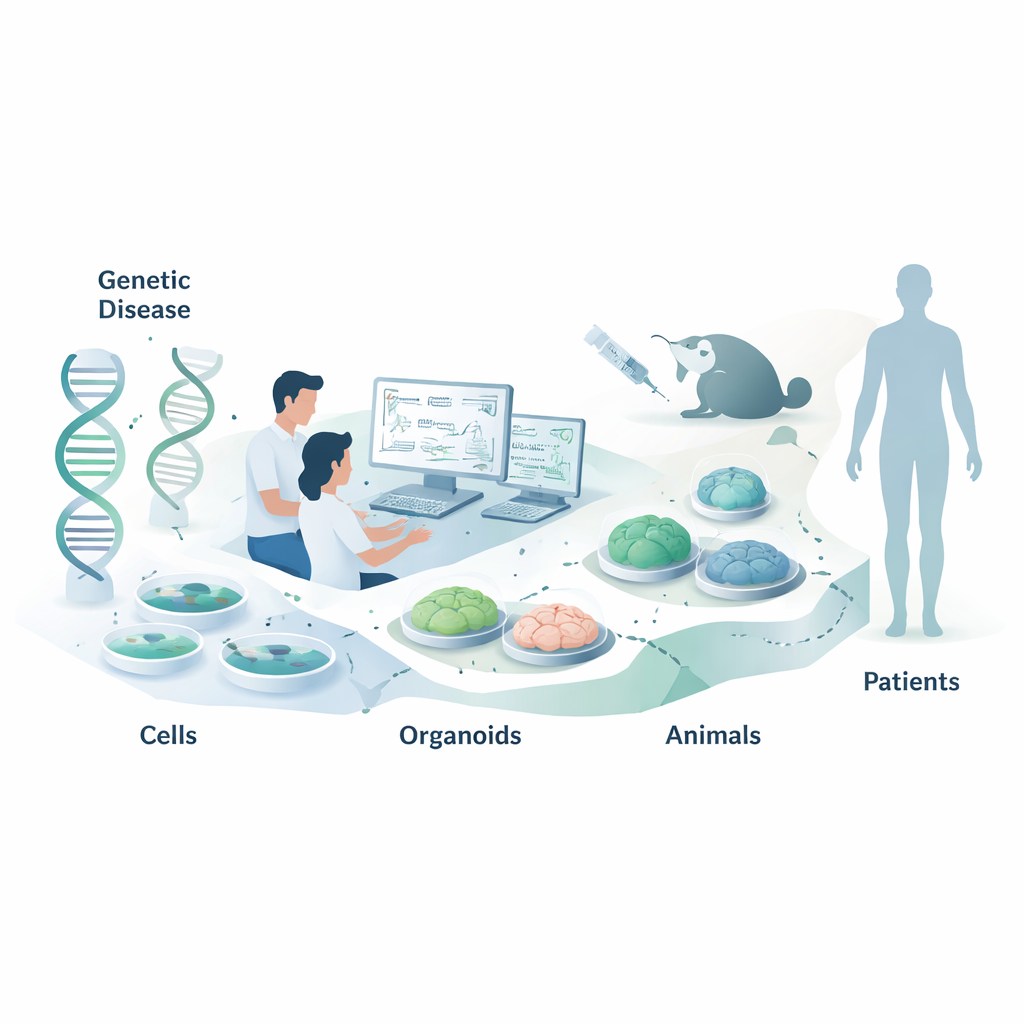
Test cellulari semplici: rapidi ma non esaustivi
Il primo approdo per la maggior parte delle NAT è una batteria di linee cellulari relativamente facili da coltivare, come HeLa o HEK293, che esprimono già l'RNA bersaglio. I ricercatori aggiungono grandi librerie di ASO o siRNA candidati e poi misurano quanto diminuiscono l'RNA bersaglio e la relativa proteina, usando tecniche come PCR e Western blot. Possono anche lavorare con cellule derivate da pazienti, che catturano meglio il background genetico individuale e permettono di testare farmaci «selettivi per allele» che silenziano solo la copia difettosa di un gene. Quando il gene naturale non è espress o in modo conveniente, gli scienziati talvolta introducono mini‑geni artificiali o plasmidi reporter che brillano quando l'RNA viene tagliato o correttamente splicato. Questi sistemi sono potenti per confrontare molti progetti rapidamente, ma possono perdere dettagli importanti, come la struttura naturale dell'RNA o l'elaborazione specifica per tipo cellulare, quindi i risultati devono essere confermati in contesti più realistici.
Dalle correzioni molecolari al comportamento cellulare reale
Molte NAT non mirano solo a distruggere un RNA difettoso, ma a ripararlo modificando lo splicing, il processo che ricuce i pezzi del messaggio genico. ASO progettati con cura possono indurre le cellule a escludere un esone dannoso, ripristinare una parte mancante o prevenire l'inserimento di un «pseudo‑esone» che interrompe il codice. Per verificare se tali cambiamenti migliorano effettivamente la funzione cellulare, i ricercatori vanno oltre le semplici misure di RNA e proteina. In cellule derivate da pazienti testano se ritorna l'attività enzimatica, se il trasporto di ioni nelle cellule polmonari si normalizza o se le vie di segnalazione nelle cellule immunitarie rispondono correttamente. Sempre più spesso usano organoidi tridimensionali—mini‑tessuti coltivati da cellule staminali dei pazienti—che possono imitare battiti cardiaci, attività di rete cerebrale o altri comportamenti complessi. Questi modelli 3‑D sono più vicini agli organi reali ma sono più difficili, lenti e costosi da gestire, quindi i team devono bilanciare realismo e produttività.
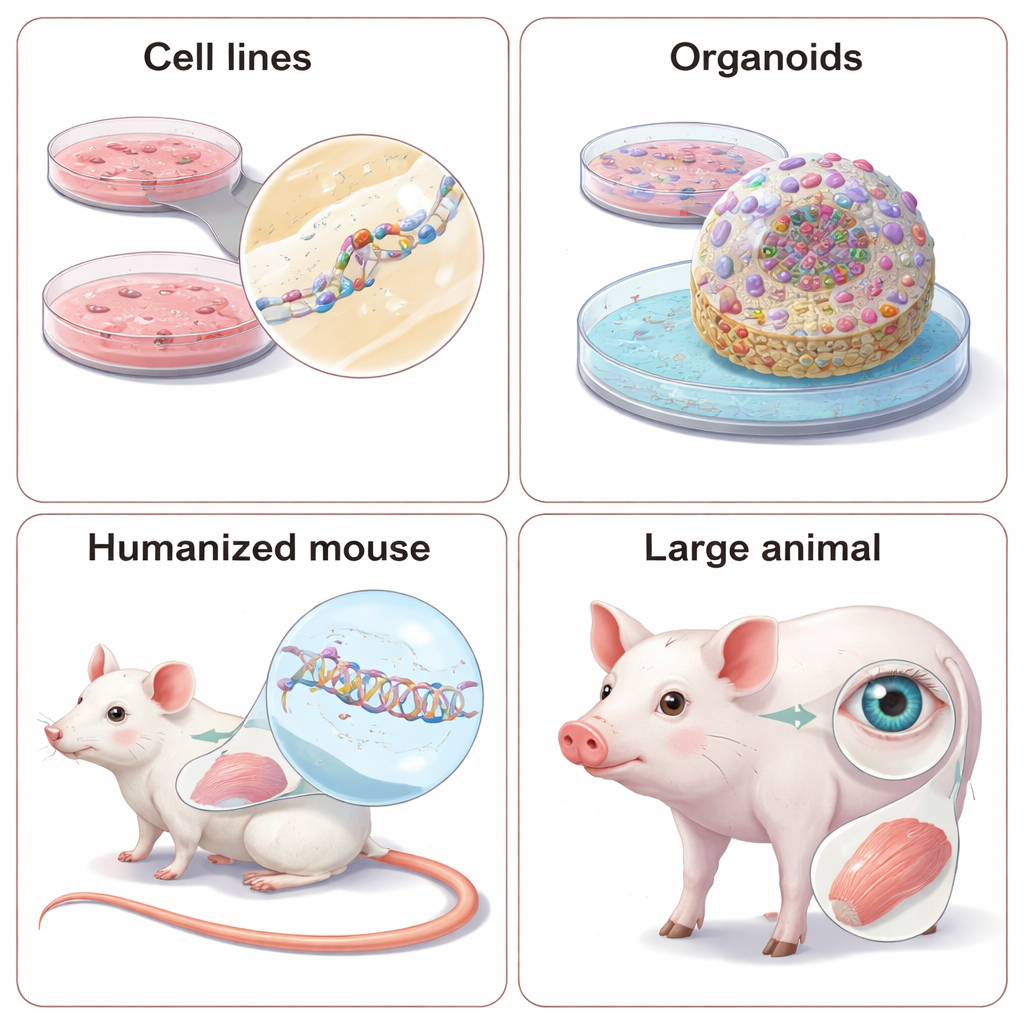
Perché gli animali contano ancora—e come umanizzarli
Alcune caratteristiche della malattia, come il metabolismo dell'intero organismo, le interazioni organo‑organo o il comportamento, semplicemente non possono essere catturate in provetta. Per questo le NAT vengono testate in animali vivi. Poiché questi farmaci dipendono da sequenze di RNA esatte, gli scienziati devono scegliere: progettare farmaci «surrogati» che corrispondano alla versione del gene dell'animale, o reingegnerizzare l'animale per portare sequenze genetiche umane. ASO e siRNA surrogati possono mostrare se abbassare l'espressione di un gene migliora i sintomi in modelli murini consolidati, ma non mimano perfettamente il farmaco che prende di mira l'uomo. I modelli umanizzati—topi o persino mini‑maiali con sezioni o copie intere di geni umani—permettono di testare il candidato clinico reale ma richiedono tempo e costi significativi, e differenze sottili nella regolazione genica tra specie possono comunque riservare sorprese. La recensione evidenzia anche l'uso crescente di animali di grandi dimensioni, particolarmente utile per malattie dell'occhio e del muscolo, dove l'anatomia assomiglia di più a quella umana.
Guardando avanti: modelli più intelligenti e meno congetture
Gli autori concludono che non esiste un unico «miglior» modello per i farmaci a base di acidi nucleici; ogni progetto necessita di un percorso su misura che parta da saggi veloci e semplici e progredisca verso sistemi più complessi e rilevanti per l'uomo. Con l'aumento della pressione da parte di regolatori e finanziatori per ridurre l'uso di animali, organoidi sofisticati, dispositivi organ‑on‑a‑chip e modelli computazionali dovrebbero svolgere una quota maggiore del lavoro, soprattutto se combinati con strumenti di machine learning che predicono quali sequenze e chimiche funzioneranno meglio. In ultima analisi, comprendendo pregi e punti ciechi di ciascun modello—e condividendo pratiche ottimali e dati nell'intero settore—i ricercatori possono trasformare in modo più affidabile idee genetiche programmabili in farmaci sicuri ed efficaci per i pazienti.
Citazione: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Parole chiave: terapie con acidi nucleici, oligonucleotidi antisenso, siRNA, modelli preclinici, terapia genica