Clear Sky Science · it
I percorsi paralleli dipendenti da Tbr2 regolano lo sviluppo di distinti sottotipi di ipRGC
Come i nostri occhi dicono l’ora e modellano la forma
Oltre a formare immagini, i nostri occhi regolano silenziosamente l’orologio biologico, controllano l’apertura della pupilla e ci aiutano a percepire la luminosità generale. Una piccola popolazione di neuroni retinici speciali, chiamati cellule gangliari retiniche intrinsecamente fotosensibili (ipRGC), gestisce gran parte di queste funzioni. Rispondono alla luce tramite un pigmento chiamato melanopsina e inviano segnali nelle aree profonde del cervello. Questo studio affronta una domanda fondamentale dalle grandi implicazioni: come una popolazione iniziale di neuroni in sviluppo si differenzia in diversi sottotipi di ipRGC, ciascuno cablato per un compito diverso?
Un interruttore maestro, molti tipi di cellule fotosensibili
Nella retina del topo, tutti e sei i sottotipi noti di ipRGC derivano da una popolazione precoce di cellule gangliari che attivano il gene Tbr2. Questo gene funziona come un interruttore maestro, avviando i programmi necessari per creare le ipRGC e mantenere attivo il gene della melanopsina, Opn4. Ma un singolo interruttore maestro non basta a spiegare come emergano sei varietà diverse di ipRGC, ognuna con forme, risposte alla luce e destinazioni cerebrali peculiari. Gli autori hanno usato il sequenziamento dell’RNA nelle retine di topo in sviluppo per cercare geni la cui attività dipenda da Tbr2. Tra un piccolo gruppo di candidati, ne sono emersi due: Irx1 e Tbx20, entrambi noti regolatori dell’identità cellulare in altre parti dell’organismo. 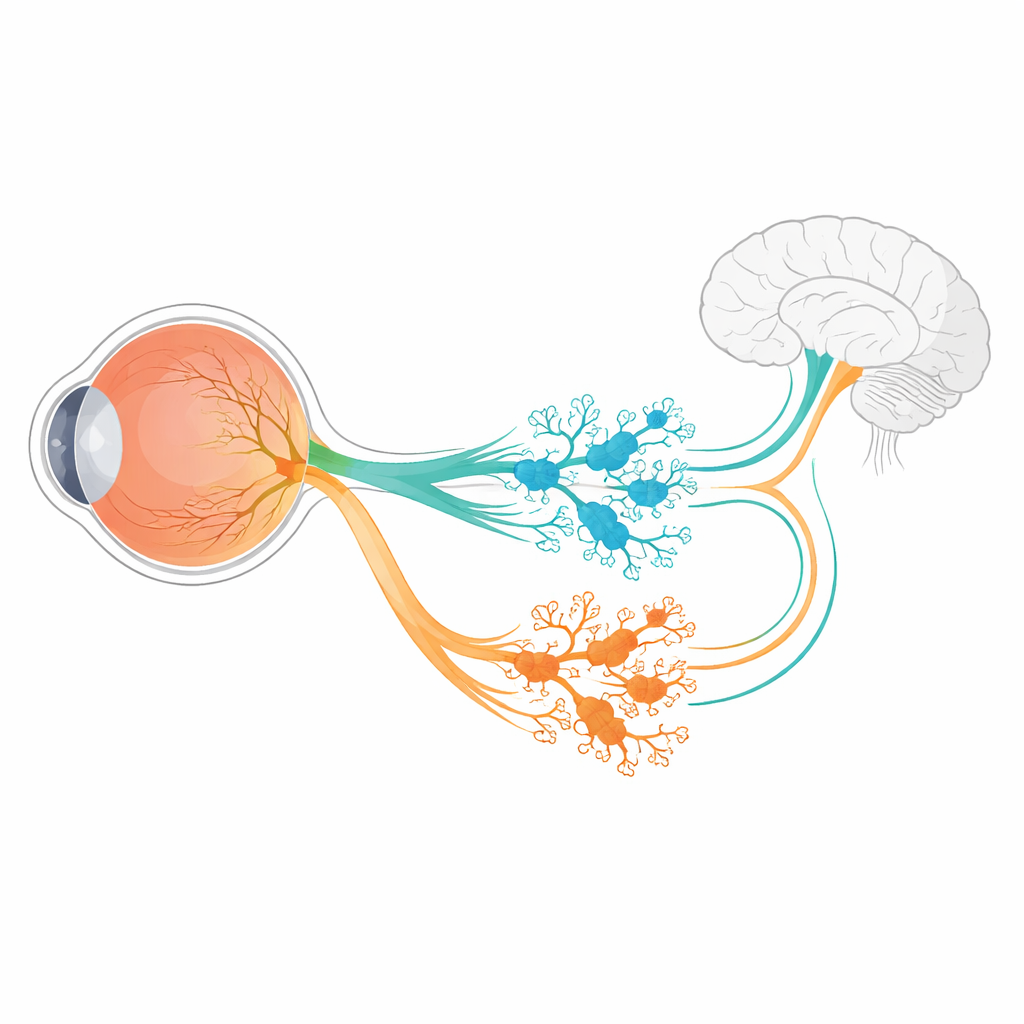
Due percorsi divergenti dentro la retina
Usando linee murine recentemente ingegnerizzate che segnano le cellule produttrici di Irx1 e Tbx20 con marcatori fluorescenti o enzimatici, i ricercatori hanno tracciato dove e quando questi fattori vengono espressi. Hanno scoperto che Irx1 e Tbx20 compaiono in gruppi sovrapposti di giovani cellule gangliari retiniche verso la metà della gestazione, ma si separano rapidamente in insiemi quasi completamente distinti nell’adulto. Irx1 è presente principalmente nei tre tipi ipRGC etichettati M3, M4 e M5, mentre Tbx20 è concentrato nelle cellule M1, M2 e M6, con solo una lieve sovrapposizione in alcune M3 e M5. Imaging dettagliato, registrazioni elettriche e tracciamenti cerebrali hanno mostrato che ciascun fattore identifica una collezione distinta di ipRGC con disposizioni dendritiche, risposte alla luce e schemi di proiezione caratteristici verso regioni cerebrali coinvolte nell’impostazione dell’orologio, nei riflessi e nell’elaborazione visiva.
Interruttori che modulano la sensibilità alla luce e la sopravvivenza cellulare
Il gruppo ha quindi esaminato cosa succede quando ciascun fattore viene rimosso. Quando Irx1 è stato eliminato nella retina in sviluppo, il numero e la struttura di base delle ipRGC marcate da Irx1 sono rimasti in gran parte intatti, ma i loro livelli di melanopsina sono diminuiti drasticamente. In altre parole, Irx1 si è dimostrato essenziale per l’attivazione completa del programma sensibile alla luce Opn4 nelle cellule M3, M4 e M5, ma non per la formazione iniziale di queste cellule. Tbx20 si è comportato diversamente. L’eliminazione di Tbx20 non solo ha ridotto l’espressione di Opn4, ma ha anche dimezzato approssimativamente il numero di ipRGC positive per Tbx20 e successivamente ha ridotto la sopravvivenza di queste cellule. Ciò indica che Tbx20 contribuisce sia alla costruzione sia al mantenimento di particolari sottotipi di ipRGC, specialmente M1, M2 e M6, sostenendo al contempo la loro sensibilità alla luce basata sulla melanopsina. 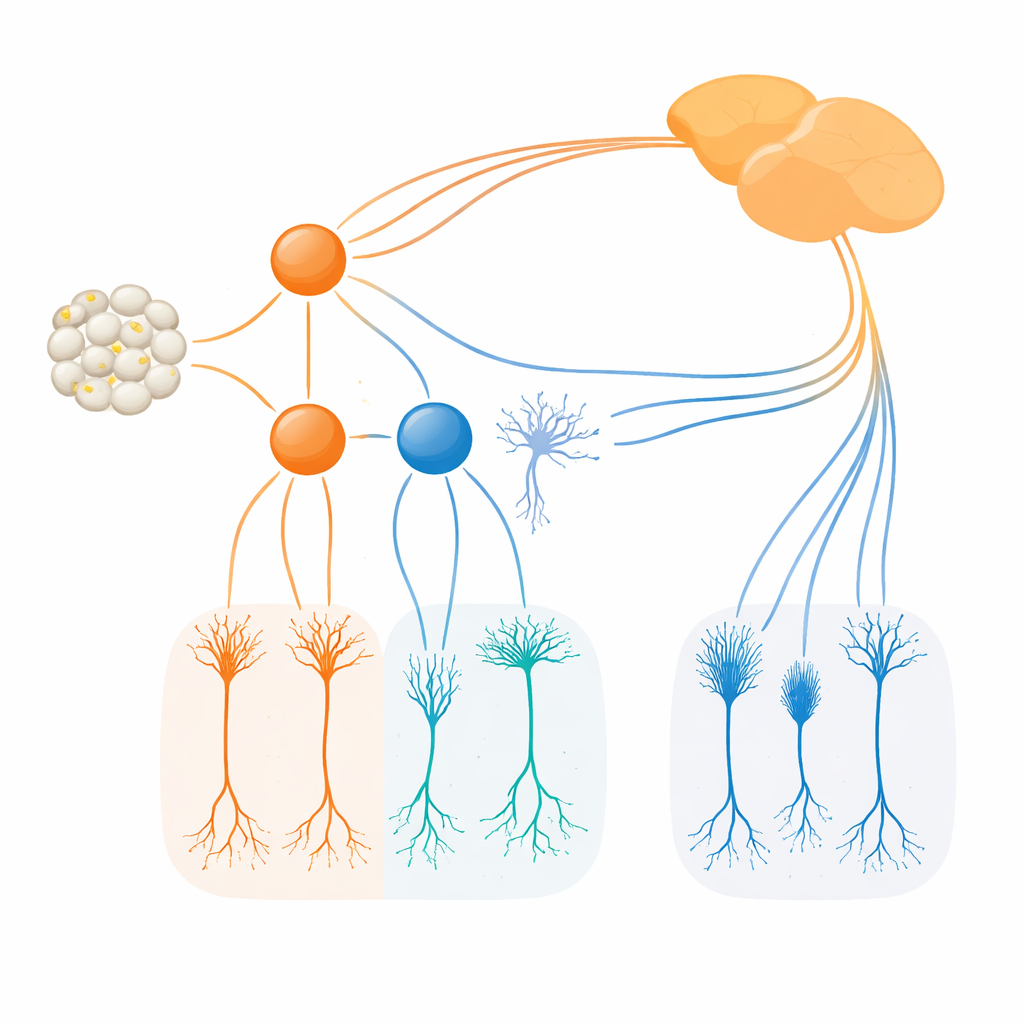
Temporizzare la separazione in famiglie cellulari distinte
Attivando brevemente i reporter genetici in giorni embrionali precisi, gli autori hanno potuto “timbrare” le cellule che esprimevano Irx1 o Tbx20 e seguirne il destino fino all’età adulta. Questi esperimenti hanno mostrato che le cellule marcate da Tbx20 si impegnano nelle loro identità finali di ipRGC leggermente prima delle cellule marcate da Irx1, con la maggior parte delle decisioni consolidate poco prima della nascita. Durante una finestra breve, sia Irx1 sia Tbx20 possono essere co‑espressi in alcune cellule, e i topi con doppio knockout privi di entrambi i geni hanno mostrato una perdita molto più marcata di ipRGC positive alla melanopsina rispetto a ciascun singolo mutante. Questo suggerisce che i due percorsi collaborano transitoriamente, per poi divergere e guidare sottoinsiemi differenti di ipRGC lungo tracce di sviluppo separate.
Cosa significa per la comprensione della visione e della salute
Per un lettore non specialista, il messaggio principale è che un singolo gene precoce, Tbr2, non agisce da solo. Piuttosto, si dirama in due vie di controllo parallele, una centrata su Irx1 e l’altra su Tbx20. Questi percorsi decidono che tipo di ipRGC diventerà una cellula giovane, ne regolano la forza della sensibilità alla luce e determinano se si collegherà a regioni cerebrali coinvolte nella regolazione dell’orologio biologico, nei riflessi pupillari o in altri ruoli visivi. Il lavoro fornisce uno schema più chiaro del cablaggio con cui sono costruiti i nostri “misuratori di luce” interni e mette in evidenza passaggi genetici specifici che potrebbero essere coinvolti quando queste cellule vengono perse o non funzionano correttamente, con potenziale rilevanza per disturbi del sonno, variazioni stagionali dell’umore e malattie che danneggiano la retina.
Citazione: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Parole chiave: cellule gangliari retiniche, melanopsina, sviluppo neuronale, ritmi circadiani, fattori di trascrizione