Clear Sky Science · it
L’analisi strutturale rivela che molecole d’acqua mediano l’auto‑attivazione di GPR99
Perché questo recettore è importante per l’infiammazione
Le nostre vie respiratorie e altri tessuti sono costantemente impegnati a percepire segnali chimici che indicano infezione o irritazione. Un sensore di questo tipo, una proteina chiamata GPR99 che si trova sulla superficie cellulare, emerge come un interruttore cruciale nelle malattie infiammatorie come l’asma e i polipi nasali. Questo studio spiega, a livello atomico, come GPR99 possa attivarsi da solo anche senza un segnale chimico esterno — e come piccoli ammassi di molecole d’acqua ne favoriscano l’attivazione — offrendo indizi utili per progettare nuovi farmaci anti‑infiammatori.
Un interruttore incorporato all’interno di un sensore cellulare
GPR99 appartiene a una vasta famiglia di proteine di membrana che trasferiscono messaggi dall’esterno all’interno della cellula, spesso cambiando conformazione e reclutando proteine partner chiamate proteine G. A differenza della maggior parte di questi recettori, GPR99 è insolitamente attivo anche in assenza di un ligando. Gli autori mostrano che un anello flessibile sul lato esterno di GPR99, noto come secondo loop extracellulare, si comporta come una chiave interna: si ripiega all’interno della tasca di legame, imitando un segnale attivante e accendendo il recettore autonomamente.
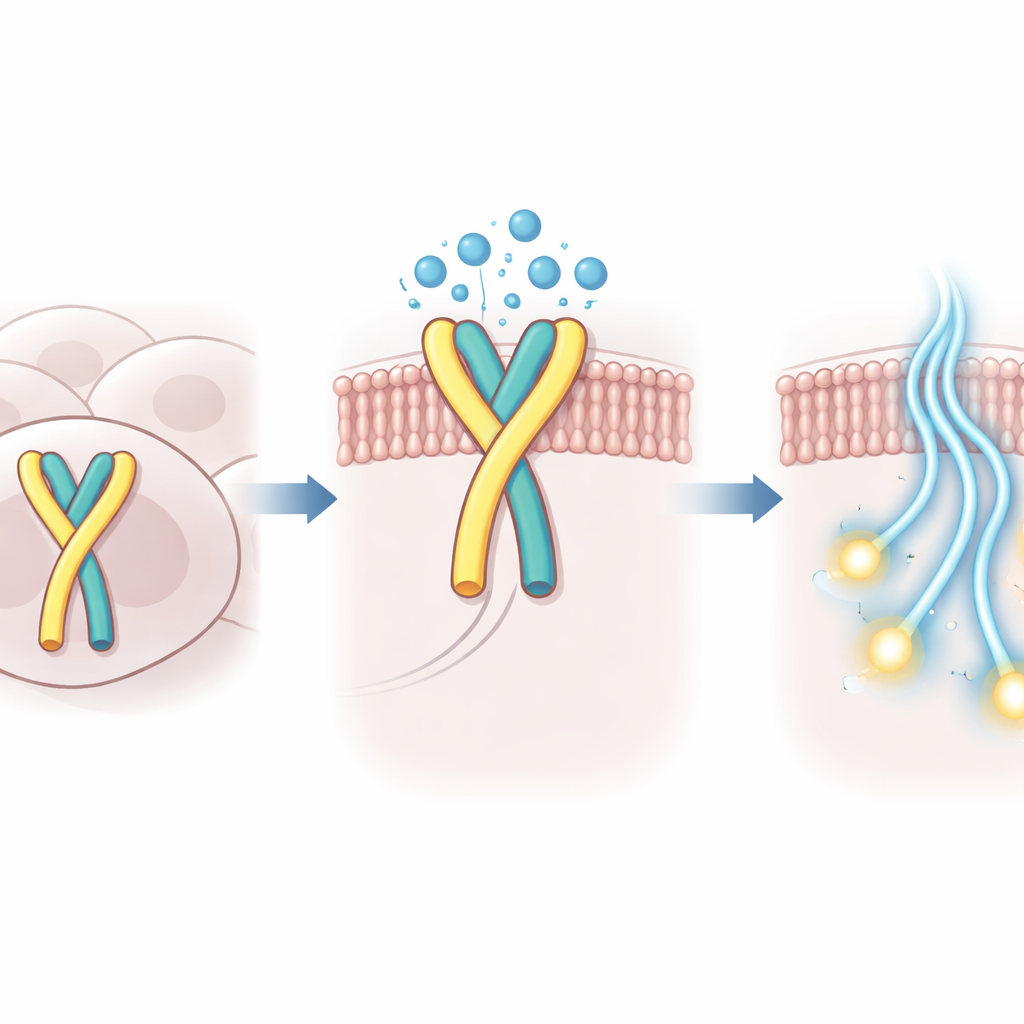
Come l’acqua contribuisce a tenere fissato l’interruttore
Usando la criomicroscopia elettronica ad alta risoluzione, i ricercatori hanno catturato la struttura tridimensionale dell’essere umano GPR99 legato al suo partner proteina G in questo stato auto‑attivato. Nella tasca di legame dove normalmente si sistemerebbero molecole esterne, hanno osservato non solo l’anello ripiegato ma anche un piccolo ammasso di molecole d’acqua ordinate. Queste molecole d’acqua formano un ponte polare tra l’anello e la proteina circostante, compensando l’inserimento meno profondo dell’anello e stabilizzando la conformazione attiva del recettore. Quando residui amminoacidici chiave nell’anello o nella tasca vicina sono stati alterati in modo da indebolire questi contatti mediati dall’acqua, l’attività intrinseca di GPR99 è caduta bruscamente in test su cellule.
Riorganizzare il funzionamento interno per una segnalazione costante
Il team ha confrontato la loro struttura auto‑attivata con altri membri della famiglia, incluso un recettore strettamente correlato che lega il sottoprodotto metabolico succinato e una forma attiva di GPR99 legata al metabolita 2‑ossoglutarato. Hanno trovato che GPR99, in assenza di qualsiasi ligando esterno, è già completamente predisposto in una conformazione attiva: diversi “microswitch” conservati all’interno del suo nucleo elicoidale assumono forme che normalmente si osservano solo quando questi recettori sono stimolati. Posizioni critiche che solitamente contribuiscono a mantenere i recettori nello stato spento sono sostituite o riorientate in GPR99, allentando i vincoli interni e favorendo la configurazione aperta che accoglie la proteina G partner.
Trasmettere il messaggio all’interno della cellula
Sul lato interno della membrana, la struttura rivela come GPR99 afferra la proteina G di tipo Gq che trasmette il suo segnale. Una coda elicoidale della proteina G si inserisce in una cavità aperta dallo slancio verso l’esterno di una delle eliche di GPR99, creando una rete di contatti polari e idrofobici con i loop interni e la coda del recettore. Mutazioni che disturbano questa interfaccia riducono anch’esse la segnalazione, confermando che l’auto‑attivazione generata dall’anello esterno e dall’ammasso d’acqua è efficacemente accoppiata ai partner intracellulari. Nel loro insieme, queste istantanee strutturali collegano i cambiamenti sulla superficie esterna del recettore alle ondate di segnalazione del calcio che esso innesca all’interno delle cellule.
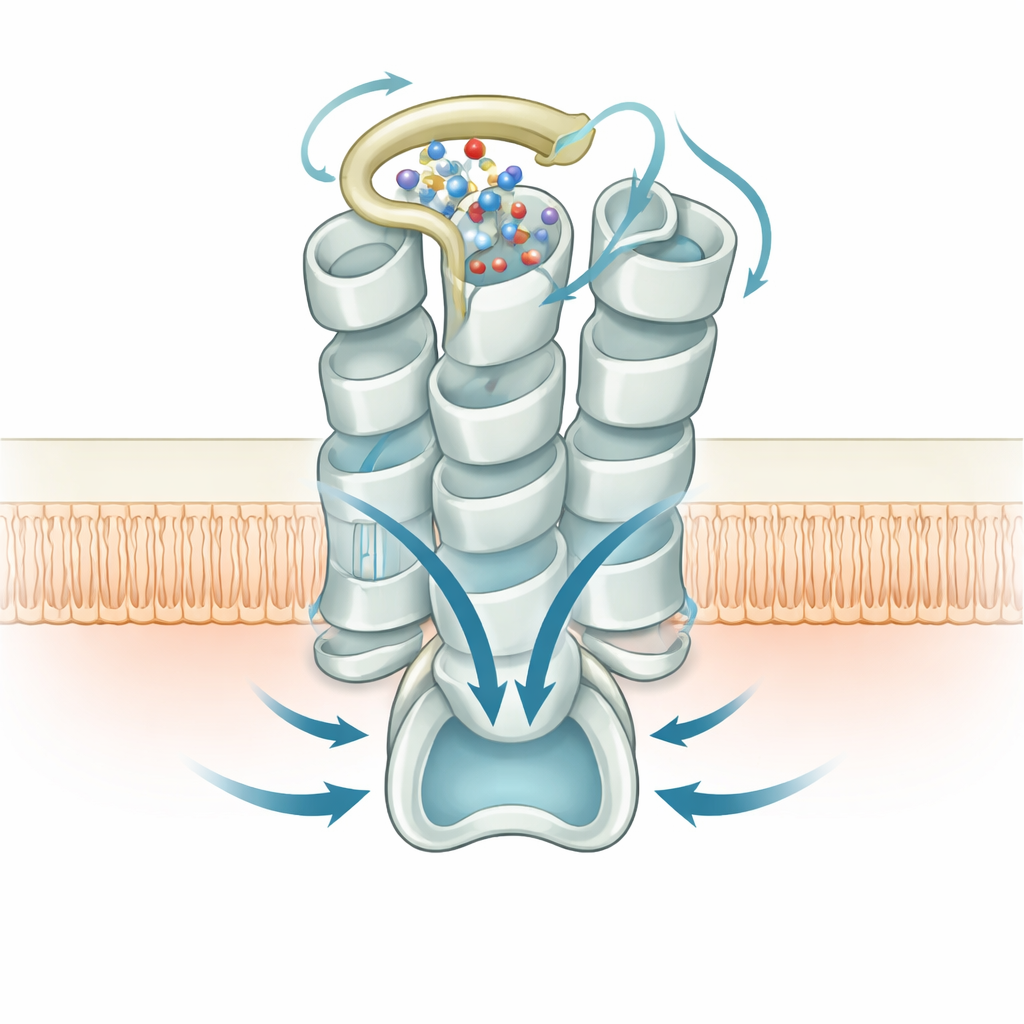
Implicazioni per la respirazione e oltre
Gli autori suggeriscono che l’attività intrinseca di GPR99, rinforzata da molecole d’acqua strutturali, possa mantenere i tessuti delle vie aeree in una modalità di “standby” — pronti a rilasciare muco e ad avviare una risposta immunitaria quando compaiono lipidi infiammatori o cambiamenti metabolici. Poiché GPR99 è altamente attivo anche senza segnali esterni, e poiché la sua attivazione dipende da un arrangiamento specifico di anello e acqua, queste intuizioni strutturali offrono bersagli concreti per i progettisti di farmaci. Piccole molecole che interrompono questo interruttore interno o la sua rete di acqua potrebbero attenuare l’infiammazione eccessiva, mentre composti che modulano finemente l’interazione potrebbero sfruttare la sensibilità di GPR99 a scopi terapeutici.
Citazione: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Parole chiave: GPR99, attivazione GPCR, structural biology, infiammazione, segnalazione mediata dall’acqua