Clear Sky Science · it
Meccanismo strutturale dell’anticorpo anti-MHC-I che blocca i recettori inibitori delle NK nell’immunità antitumorale
Risvegliare gli assassini silenziosi del corpo
Il nostro sistema immunitario dispone di potenti sentinelle chiamate cellule natural killer (NK) in grado di riconoscere e distruggere cellule tumorali e infettate da virus. Tuttavia i tumori spesso imparano a silenziare queste sentinelle. Questo studio rivela, a livello atomico, come un anticorpo appositamente progettato possa rimuovere quel “pulsante muto”, riattivando le NK affinché attacchino i tumori in modo più efficace. Il lavoro combina biologia strutturale d’avanguardia con esperimenti su topo per dimostrare come un singolo anticorpo possa integrare le immunoterapie antitumorali esistenti.
I tag di identità immunitaria sulle nostre cellule
Ogni cellula del nostro organismo espone sulla superficie dei “tag” molecolari chiamati MHC di classe I. Questi tag aiutano le cellule immunitarie a distinguere i tessuti normali dalle cellule pericolose diventate tumorali o infettate da virus. Le NK scandagliano costantemente questi tag. Quando percepiscono pattern normali, i recettori inibitori sulle NK inviano un segnale calmante che impedisce l’attacco. I tumori spesso mantengono visibili questi tag, usandoli come uno scudo protettivo: finché il segnale inibitorio è presente, le NK trattengono il fuoco e il cancro può crescere.
Un anticorpo che afferra lo scudo
I ricercatori hanno studiato un anticorpo monoclonale chiamato B1.23.2 che lega in modo robusto molte varianti umane del MHC di classe I sulle cellule tumorali. Utilizzando crio-microscopia elettronica e cristallografia a raggi X, hanno mappato esattamente come questo anticorpo si posiziona sulla superficie del MHC. B1.23.2 si ancora su una cresta conservata della molecola MHC — un’elica α2 — senza toccare il suo partner catena leggera e percependo solo marginalmente il peptide presentato. Ciò significa che l’anticorpo può riconoscere un’ampia gamma di molecole MHC-A, -B e -C umane con elevata affinità, risultando relativamente insensibile ai frammenti proteici specifici mostrati dal MHC.
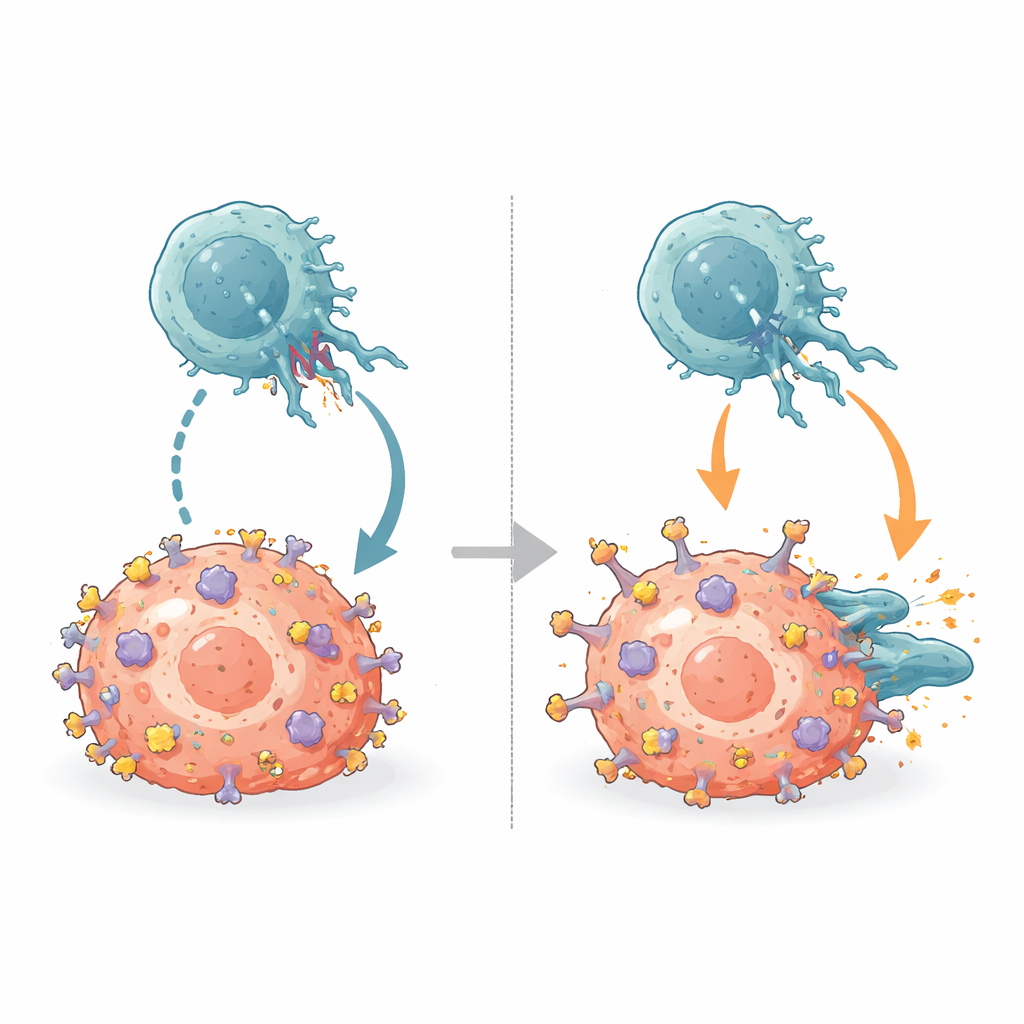
Superare i freni del sistema immunitario
Le NK portano recettori inibitori chiamati KIR che normalmente si ancorano sulla stessa cresta α2 dell’MHC. Allineando le nuove strutture anticorpo–MHC con strutture note KIR–MHC, il team ha dimostrato che B1.23.2 occupa fisicamente la porzione di MHC di cui i KIR hanno bisogno per aggrapparsi. Il sito di legame dell’anticorpo e le impronte dei KIR si sovrappongono così estensivamente che entrambi non possono legarsi simultaneamente. B1.23.2 inoltre si lega all’MHC con affinità maggiore rispetto ai KIR, il che le permette di vincere questa lotta molecolare. Di conseguenza, quando l’anticorpo ricopre le molecole MHC delle cellule tumorali, i KIR sulle NK non possono più trasmettere i loro segnali inibitori, spostando l’equilibrio verso l’attivazione delle NK.
Affinare l’adattamento e ampliare la copertura
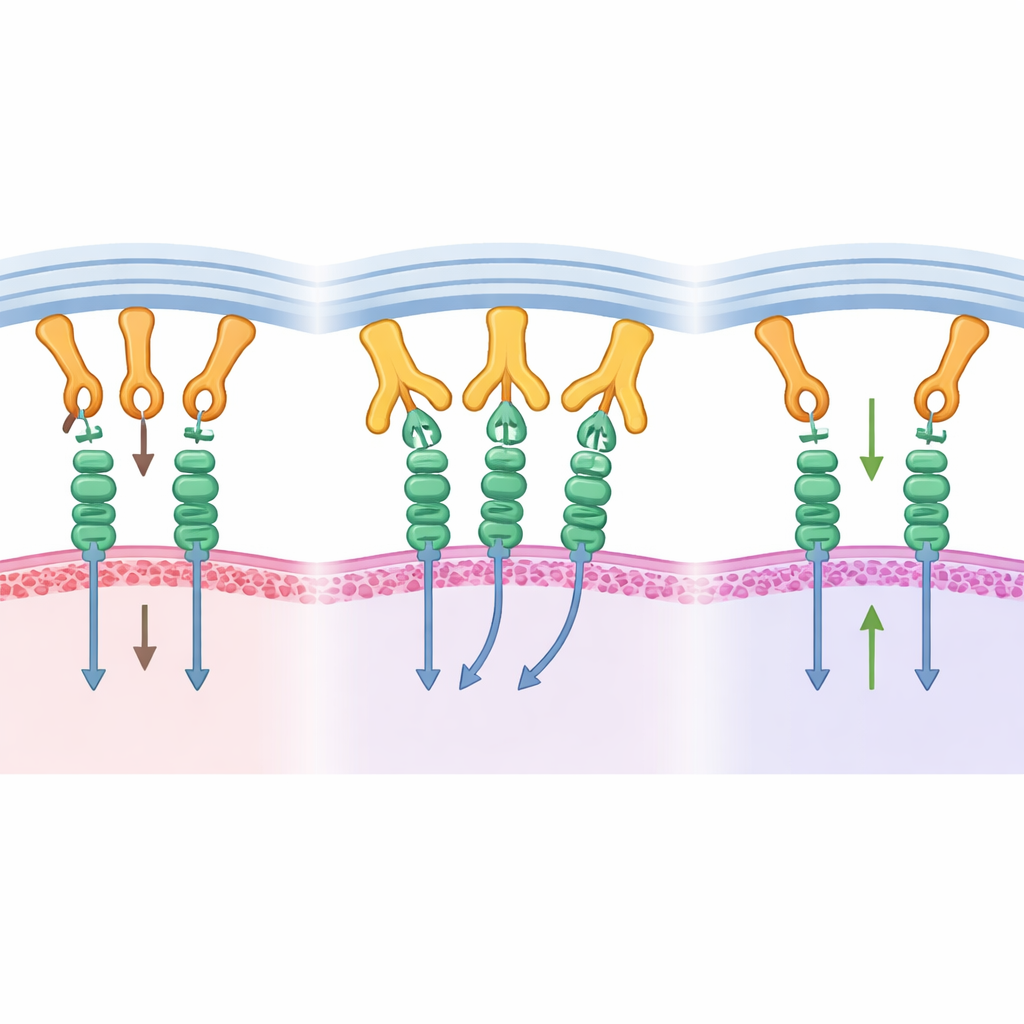
Sebbene B1.23.2 miri principalmente alla superficie conservata dell’MHC, gli autori hanno rilevato che piccole differenze nel peptide legato all’MHC possono modulare sottilmente la forza dell’anticorpo. Sostituendo sistematicamente una singola posizione amminoacidica nel peptide, hanno mostrato variazioni modeste nel legame — generalmente entro circa un fattore dieci — senza perdere il riconoscimento complessivo. Hanno inoltre indagato perché alcuni tipi comuni di MHC, come HLA-A*02:01, sfuggano al legame. Trapiantando residui di contatto chiave da una variante MHC reattiva in HLA-A*02:01, il team ha ingegnerizzato versioni che l’anticorpo è stato ora in grado di riconoscere, confermando con precisione quali posizioni formano la superficie di ancoraggio critica. Queste intuizioni suggeriscono che varianti future dell’anticorpo potrebbero essere progettate per coprire ancora più tipi di MHC o evitarne selettivamente altri.
Trasformare l’intuizione strutturale nel controllo del tumore
Questo blocco molecolare aiuta effettivamente a combattere i tumori? Per verificarlo, i ricercatori hanno utilizzato un modello murino umanizzato portatore di un tumore pancreatico umano. Hanno ingegnerizzato una forma di B1.23.2 incapace di segnalare tramite la propria coda Fc, così che eventuali effetti fossero dovuti principalmente al blocco dell’interazione MHC–KIR. Quando i topi hanno ricevuto l’anticorpo insieme a cellule NK umane, i tumori sono cresciuti molto più lentamente. Le NK hanno mostrato una proliferazione aumentata, maggiore attività delle vie di crescita e segnalazione, e una produzione superiore di molecole infiammatorie associate all’uccisione delle cellule tumorali. All’interno dei tumori, le NK esprimevano più recettori attivanti, coerente con il fatto di essere liberate dall’input inibitorio costante.
Cosa potrebbe significare per le terapie antitumorali future
In termini semplici, questo studio mostra come un singolo anticorpo possa insinuarsi tra le cellule tumorali e i freni del sistema immunitario, interrompendo il segnale “non attaccare” che normalmente mantiene le NK silenziose. Mappando l’interazione a risoluzione atomica e confermandone gli effetti in animali, il lavoro offre un progetto per una nuova classe di terapie: anticorpi che legano i tag d’identità del tumore anziché i recettori immunitari stessi. Tali agenti potrebbero essere combinati con gli attuali inibitori del checkpoint o con terapie cellulari per mobilitare sia le NK sia le cellule T, offrendo al sistema immunitario un ulteriore angolo d’attacco contro i tumori difficili da trattare.
Citazione: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Parole chiave: cellule natural killer, MHC di classe I, immunoterapia del cancro, anticorpi monoclonali, recettori inibitori