Clear Sky Science · it
LukS-PV che prende di mira C5aR inibisce l’EMT nel carcinoma epatocellulare tramite l’asse BCL6/HDAC6/HSPD1
Trasformare un’arma batterica in un agente anti-cancro
Il carcinoma epatocellulare, la forma più comune di cancro al fegato, è spesso letale perché si diffonde dal fegato ad altri organi. Questo articolo esplora un alleato inaspettato contro tale diffusione: una proteina, LukS-PV, originariamente parte di una tossina prodotta dal batterio Staphylococcus aureus. I ricercatori dimostrano come questa proteina possa legarsi a un recettore specifico sulle cellule del cancro epatico e, invece di danneggiare i tessuti normali, bloccare passaggi cruciali che permettono alle cellule tumorali di staccarsi, migrare e formare nuovi tumori.
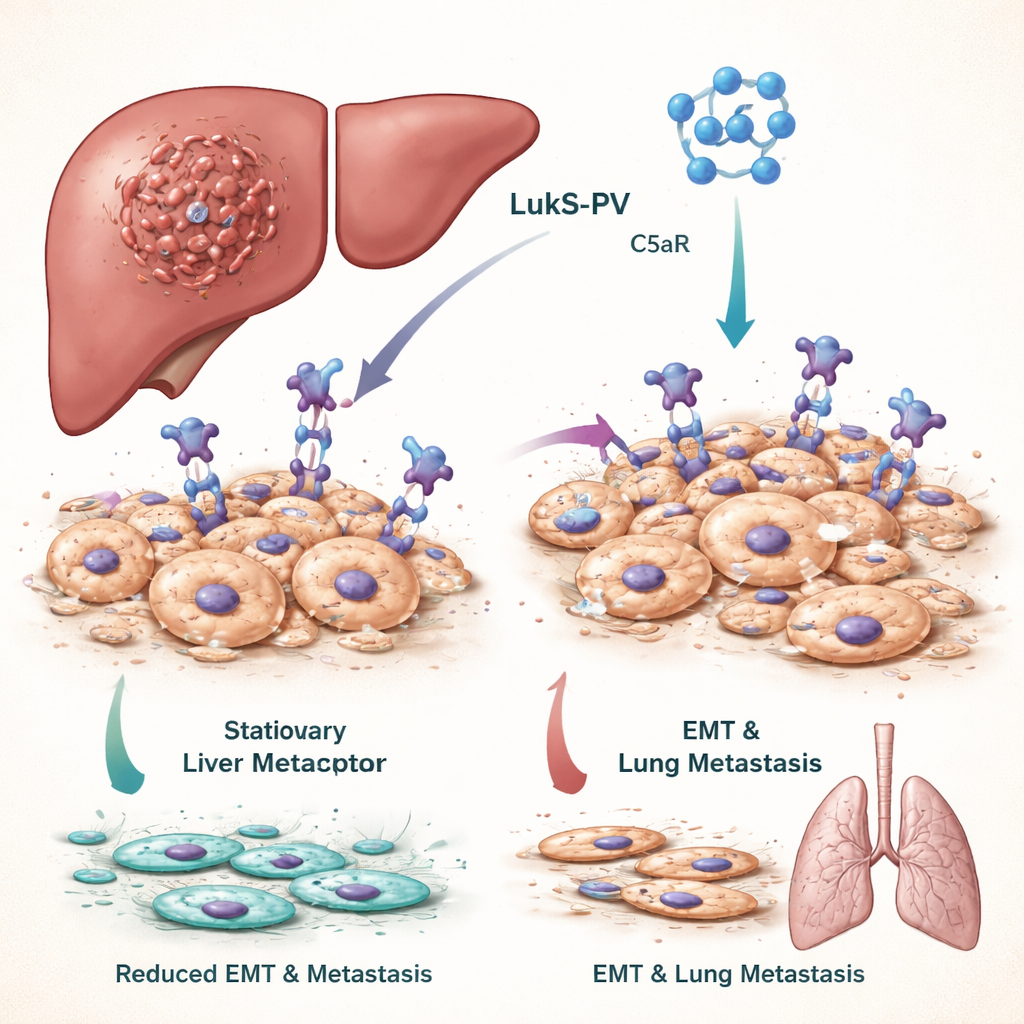
Perché fermare le cellule tumorali che cambiano forma è importante
Perché il cancro al fegato si diffonda, le cellule tumorali devono subire un drastico cambiamento di forma e comportamento chiamato transizione epitelio–mesenchimale, o EMT. Nell’EMT, cellule strettamente compatte che normalmente restano al loro posto diventano più flessibili, mobili e invasive, consentendo loro di infiltrarsi nei vasi sanguigni e colonizzare organi distanti come i polmoni. I pazienti i cui tumori mostrano una forte attività EMT tendono ad avere prognosi peggiori. Il gruppo si è concentrato su una via di segnalazione guidata da una molecola chiamata C5a e dal suo recettore C5aR, che è insolitamente abbondante su molte cellule tumorali e noto per alimentare EMT e metastasi.
Un componente di una tossina che prende di mira un segnale del cancro
La leucocidina di Panton–Valentine, una tossina di Staphylococcus aureus, contiene un componente chiamato LukS-PV che riconosce e si lega naturalmente a C5aR. Lavori precedenti degli autori avevano mostrato che una versione ricombinante, non poriformante, di LukS-PV può ridurre la crescita di diversi tumori senza tossicità evidente negli animali. In questo studio hanno trattato linee cellulari di carcinoma epatocellulare con LukS-PV e osservato che le cellule diventavano meno migratorie e invasive. Test molecolari hanno rivelato che i marcatori di cellule stazionarie e ben differenziate aumentavano, mentre i marcatori di cellule aggressive e mobili diminuivano. In topi inoculati con cellule di carcinoma epatocellulare, il trattamento con LukS-PV ha portato a un numero molto inferiore di noduli tumorali nei polmoni, indicando una riduzione delle metastasi.
Bloccare una reazione a catena all’interno delle cellule tumorali
Approfondendo, i ricercatori hanno scoperto una catena di proteine di controllo all’interno delle cellule tumorali che LukS-PV interrompe. Innanzitutto LukS-PV si lega a C5aR sulla superficie cellulare e blocca efficacemente il segnale pro-metastatico indotto da C5a. Questa attenuazione della segnalazione di C5aR abbassa i livelli di una proteina chiamata BCL6, un fattore di trascrizione che normalmente attiva certi geni nel nucleo. Uno dei bersagli di BCL6 è HDAC6, un enzima che rimuove piccoli gruppi chimici noti come gruppi acetile da altre proteine. Quando BCL6 è abbondante, i livelli di HDAC6 aumentano e la cellula diventa più incline a EMT e migrazione. L’interferenza di LukS-PV con C5aR riduce BCL6, il che a sua volta diminuisce la produzione di HDAC6 e rallenta questo programma pro-metastatico.
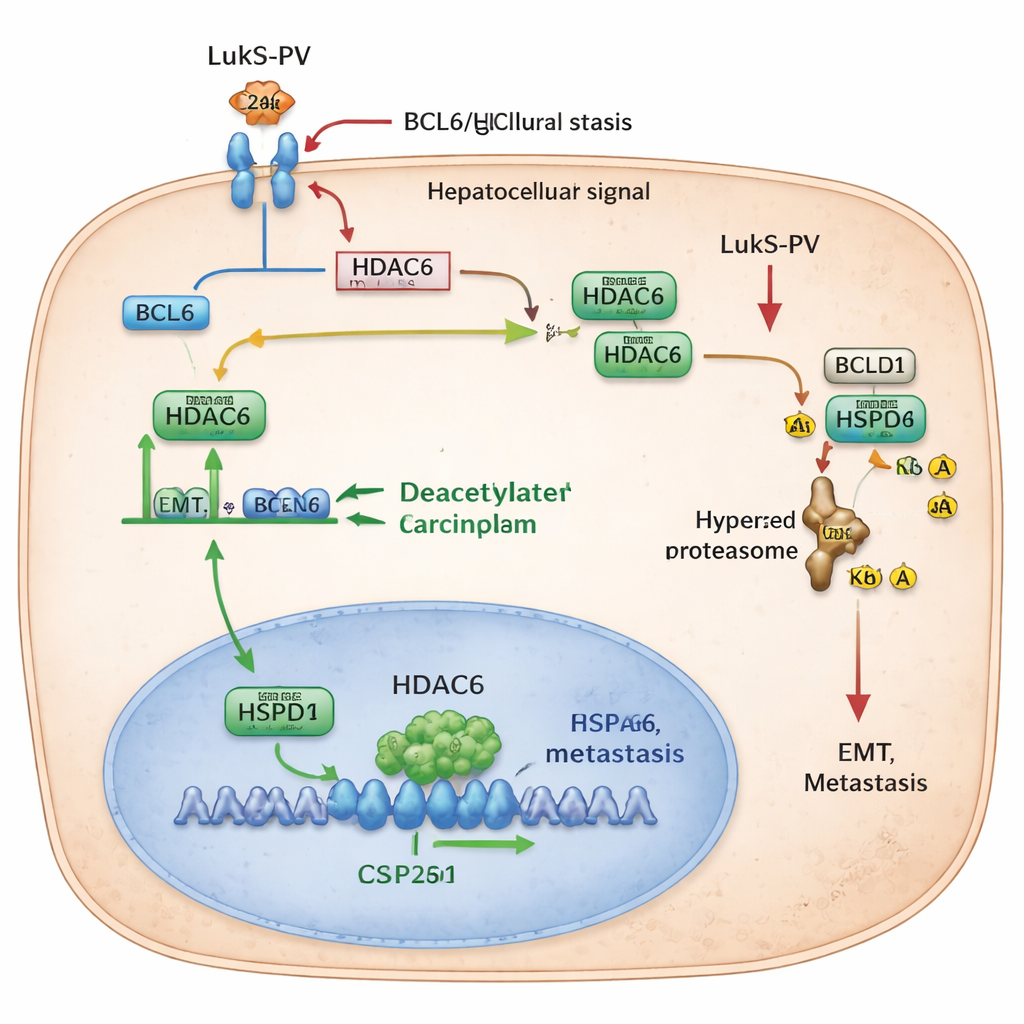
Marcare una chaperon per la distruzione
Il gruppo ha quindi identificato un partner chiave di HDAC6 chiamato HSPD1, noto anche come HSP60, una proteina “chaperone” che aiuta altre proteine a ripiegarsi e mantenersi stabili. Nel carcinoma epatocellulare i livelli di HSPD1 sono più elevati rispetto al tessuto normale circostante e sono associati a una sopravvivenza peggiore dei pazienti. I ricercatori hanno scoperto che HDAC6 interagisce fisicamente con HSPD1 e rimuove gruppi acetile da due posizioni specifiche su di essa. Quando questi marcatori acetilici vengono rimossi, HSPD1 diventa più stabile e sostiene EMT e metastasi. Quando HDAC6 viene ridotto — sia con stratagemmi genetici sia con il trattamento con LukS-PV — HSPD1 diventa più acetilata. Questa forma iperacetilata viene riconosciuta dalla macchina di smaltimento cellulare, etichettata con ubiquitina e degradata. Con la diminuzione di HSPD1, le cellule tumorali perdono parte della loro capacità di migrare, invadere e colonizzare i polmoni.
Dalle vie complesse a un messaggio semplice
Per un non specialista, il messaggio è che gli autori hanno mappato un effetto domino all’interno delle cellule del carcinoma epatocellulare: un recettore di superficie (C5aR) aumenta una proteina regolatrice (BCL6), che innalza un enzima (HDAC6) che protegge una chaperon (HSPD1) dall’essere distrutta. Insieme, questi componenti aiutano le cellule tumorali a cambiare forma, a muoversi e a diffondersi. LukS-PV, una proteina batterica riadattata in laboratorio, interrompe questa sequenza proprio alla superficie cellulare, portando in ultima analisi alla degradazione di HSPD1 e a un freno sulle metastasi. Pur essendo ancora a uno stadio sperimentale, questo lavoro suggerisce che farmaci modellati su LukS-PV — o diretti contro BCL6, HDAC6 o HSPD1 — potrebbero offrire nuove strategie per impedire la diffusione dei tumori epatici e migliorare la prospettiva per i pazienti.
Citazione: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Parole chiave: carcinoma epatocellulare, metastasi, transizione epitelio-mesenchimale, HDAC6, terapia con tossine batteriche