Clear Sky Science · it
Matrice extracellulare derivata da cellule staminali mesenchimali per la rigenerazione del tessuto muscoloscheletrico
Aiutare il corpo a ricostruire il proprio scheletro
Con l’aumento dell’aspettativa di vita e l’attività prolungata anche in età avanzata, lesioni e usura di ossa, articolazioni, muscoli e tendini sono diventate una causa importante di dolore e disabilità. Questo articolo esplora una nuova classe di materiali di riparazione “intelligenti” coltivati dalle nostre stesse cellule staminali: strutture di supporto speciali chiamate matrice extracellulare derivata da cellule staminali mesenchimali (mECM). Questi impalcati naturali potrebbero un giorno aiutare il corpo a ricostruire i tessuti muscoloscheletrici danneggiati in modo più sicuro ed efficace rispetto a molti trattamenti attuali.
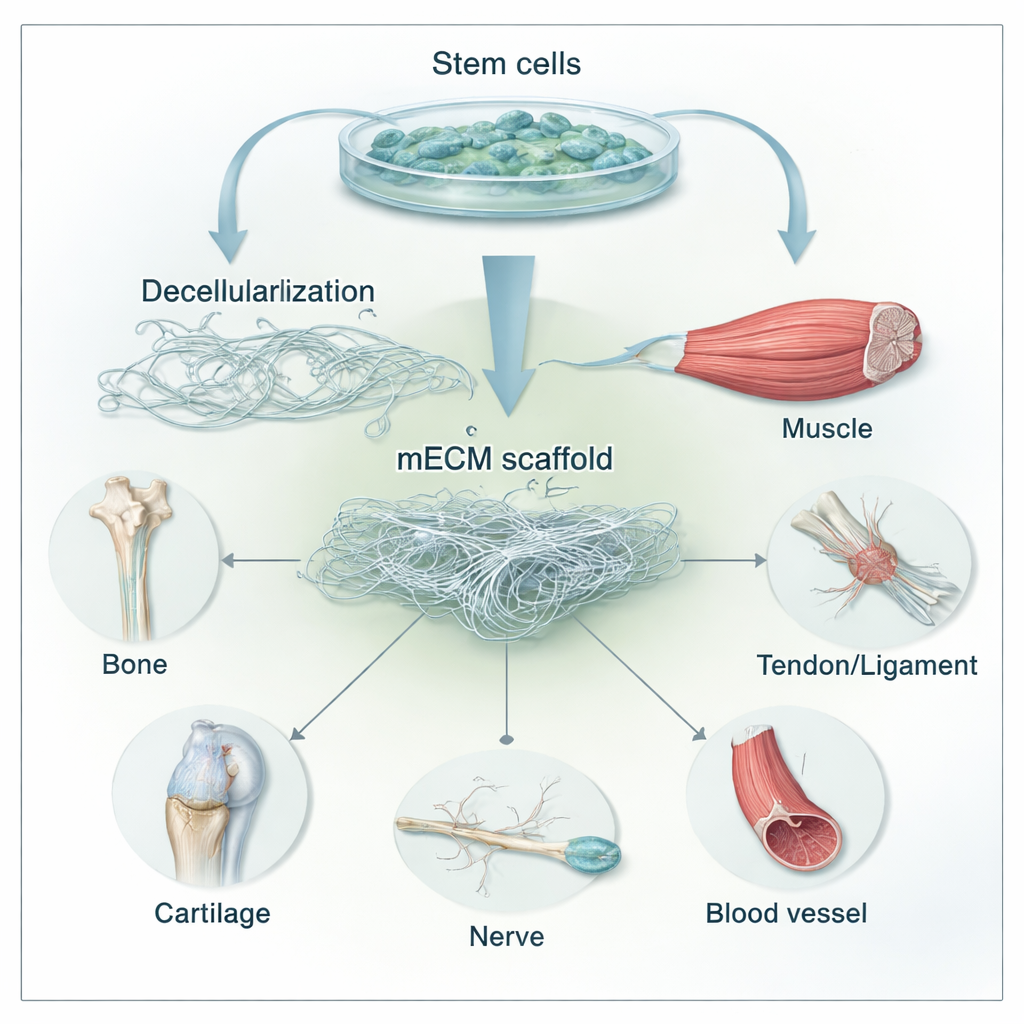
Lo scheletro nascosto del corpo
Ogni cellula del corpo vive all’interno di una rete di supporto nota come matrice extracellulare, o ECM. Non è solo una colla passiva: le sue fibre, i pori e le molecole legate inviano costantemente segnali alle cellule su come crescere, muoversi e maturare. Nell’invecchiamento e nelle malattie, questa matrice si irrigidisce, si usura e perde elasticità, indebolendo direttamente la nostra capacità di riparare ossa e cartilagine. Gli scienziati hanno imparato a rimuovere le cellule da tessuti come pelle, intestino o cartilagine, lasciando impalcature di ECM “decellularizzate” che possono essere impiantate per guidare la guarigione. Ma questi materiali derivati da tessuti possono variare da donatore a donatore, ancora scatenare reazioni immunitarie e sono difficili da personalizzare per pazienti o lesioni diverse.
Coltivare materiale di riparazione su misura dalle cellule staminali
La revisione si concentra sull’ECM ottenuta non da organi interi ma da cellule staminali mesenchimali (MSC), cellule versatili presenti nel midollo osseo, nel tessuto adiposo, nel cordone ombelicale e in altri tessuti. In laboratorio, le MSC vengono lasciate espandersi su una superficie e depositare la propria matrice: un delicato reticolo tridimensionale di collagene, fibronectina, laminina, zuccheri e fattori di crescita. Le cellule vengono poi rimosse delicatamente con detergenti ed enzimi blandi, lasciando una mECM priva di cellule. Poiché le molecole della matrice sono altamente conservate tra le specie e prive di DNA e altri forti stimoli immunitari, questi impalcati sono spesso ben tollerati. È importante che i ricercatori possano modulare la composizione e la rigidità della mECM scegliendo la fonte di cellule staminali (per esempio midollo osseo vs. tessuto adiposo) e “precondizionando” le cellule con segnali diversi prima della decellularizzazione.
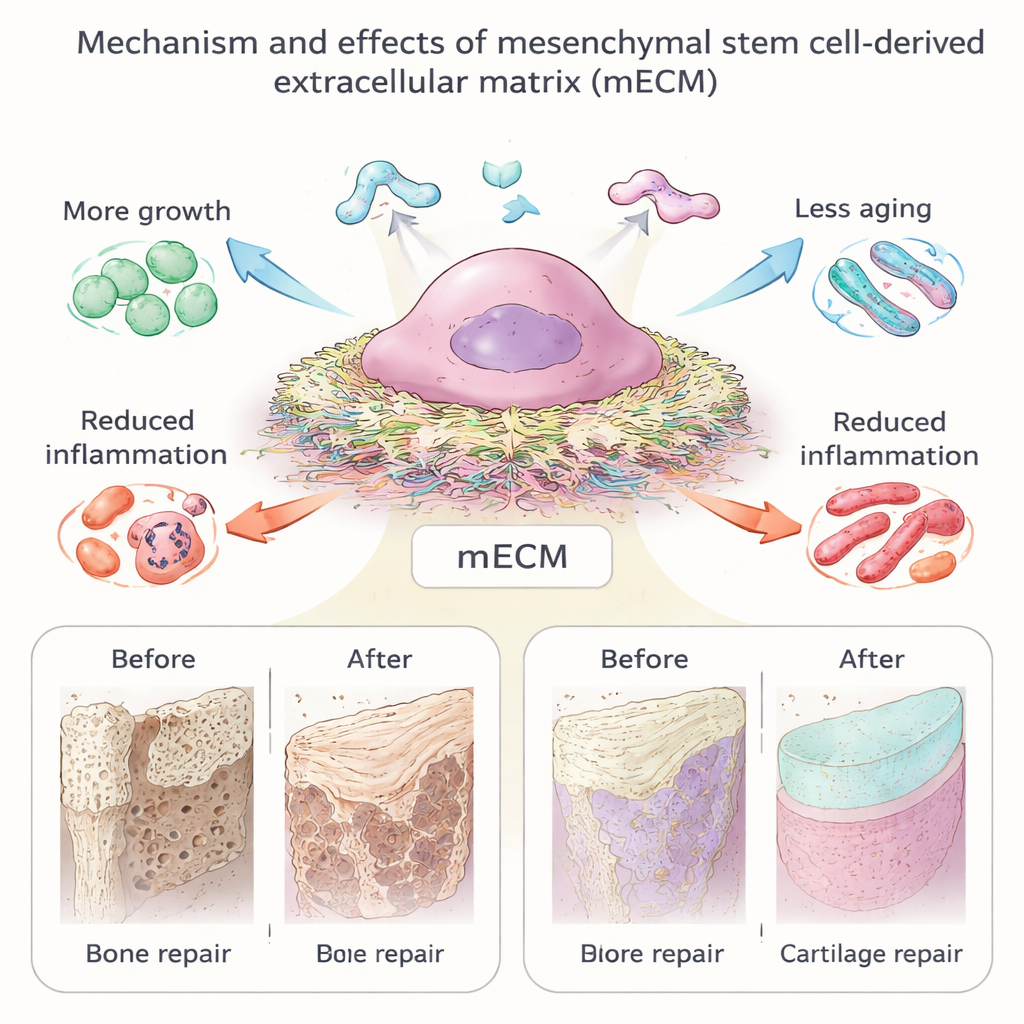
Come questo impalcato vivente comunica con le cellule
Quando cellule fresche vengono seminate su mECM, si comportano in modo molto diverso rispetto a una superficie di plastica liscia. Gli studi mostrano che la mECM aumenta la crescita cellulare mentre aiuta le cellule a mantenersi “più giovani”, ritardando l’insorgenza dell’invecchiamento cellulare e preservando la loro capacità di trasformarsi in osso o cartilagine. La mECM giovane, con meccaniche più morbide e una ricchezza maggiore di acido ialuronico, sembra particolarmente efficace nel ringiovanire cellule più anziane. Componenti specifici, come il collagene di tipo I e la fibronectina, influenzano se le cellule resistono all’invecchiamento, formano osteoclasti che riassorbono l’osso o rispondono all’infiammazione. La matrice attiva anche vie di segnalazione intracellulari legate alla longevità e alla resistenza allo stress, inclusi SIRT1 e NF-κB, e può orientare le cellule immunitarie verso uno stato più calmante e favorevole alla guarigione tissutale. In breve, la mECM funziona sia come nido fisico sia come manuale biochimico di istruzioni per le cellule.
Riparare ossa, cartilagine, muscoli, tendini, nervi e vasi
Poiché la mECM imita così da vicino i tessuti che dovrebbe riparare, è stata testata in molte forme: fogli sottili avvolti attorno a impianti, polveri miscelate in idrogel e microsfere, e rivestimenti su impalcature sintetiche. Nella riparazione ossea, le cellule coltivate su mECM acquisiscono capacità osteogeniche e aiutano a costruire tessuto più forte e meglio vascolarizzato negli animali, anche senza grandi cocktail farmacologici. Nella cartilagine, la mECM supporta la formazione di cartilagine liscia simile alla ialina e aiuta i condrociti (cellule della cartilagine) a evitare di degenerare in stati simili a cicatrici — specialmente quando la matrice proviene da cellule staminali giovani o in fase precoce di differenziamento. Studi iniziali su muscoli e tendini suggeriscono che le matrici derivate da staminali possono attrarre cellule ospiti, ridurre la formazione di cicatrici e meglio allineare le nuove fibre. In nervi e vasi sanguigni, la mECM integrata in tubi guida o nanofibre accelera la ricrescita nervosa e stimola la formazione di nuovi vasi, sottolineando il suo ampio potenziale rigenerativo.
Dal banco di laboratorio ai trattamenti reali
Nonostante risultati incoraggianti, la mECM non è ancora pronta per un uso clinico di routine. Il campo manca ancora di protocolli standard per rimuovere in modo sicuro le cellule preservando i delicati dettagli della matrice, e i veri “ingredienti attivi” che controllano il comportamento cellulare sono compresi solo in parte. Diverse fonti e età delle cellule staminali producono matrici visibilmente diverse, sollevando dubbi su quali combinazioni siano migliori per ciascun tipo di lesione. Produrre mECM su scala industriale è costoso e tecnicamente impegnativo, e gli scienziati devono dimostrare che impianti grandi e duraturi siano sicuri, stabili e meccanicamente sufficienti per siti soggetti a carico come articolazioni e tendini. Gli autori sostengono che progressi in proteomica, bioinformatica e biofabbricazione saranno cruciali per mappare, standardizzare e industrializzare questi impalcati viventi. Se questi ostacoli potranno essere superati, la mECM specifica per il paziente potrebbe diventare un nuovo standard d’oro per riparare lo scheletro del corpo dall’interno.
Citazione: Lv, S., Wang, J., Chen, J. et al. Mesenchymal stem cell-derived extracellular matrix for musculoskeletal tissue regeneration. Commun Biol 9, 147 (2026). https://doi.org/10.1038/s42003-026-09638-3
Parole chiave: matrice extracellulare, cellule staminali mesenchimali, riparazione di ossa e cartilagine, ingegneria tissutale, medicina rigenerativa