Clear Sky Science · it
La migrazione cellulare confinata periodica induce una riorganizzazione cromatinica parzialmente reversibile in linee cellulari tumorali
Come le cellule tumorali schiacciate ricordano lo stress subito
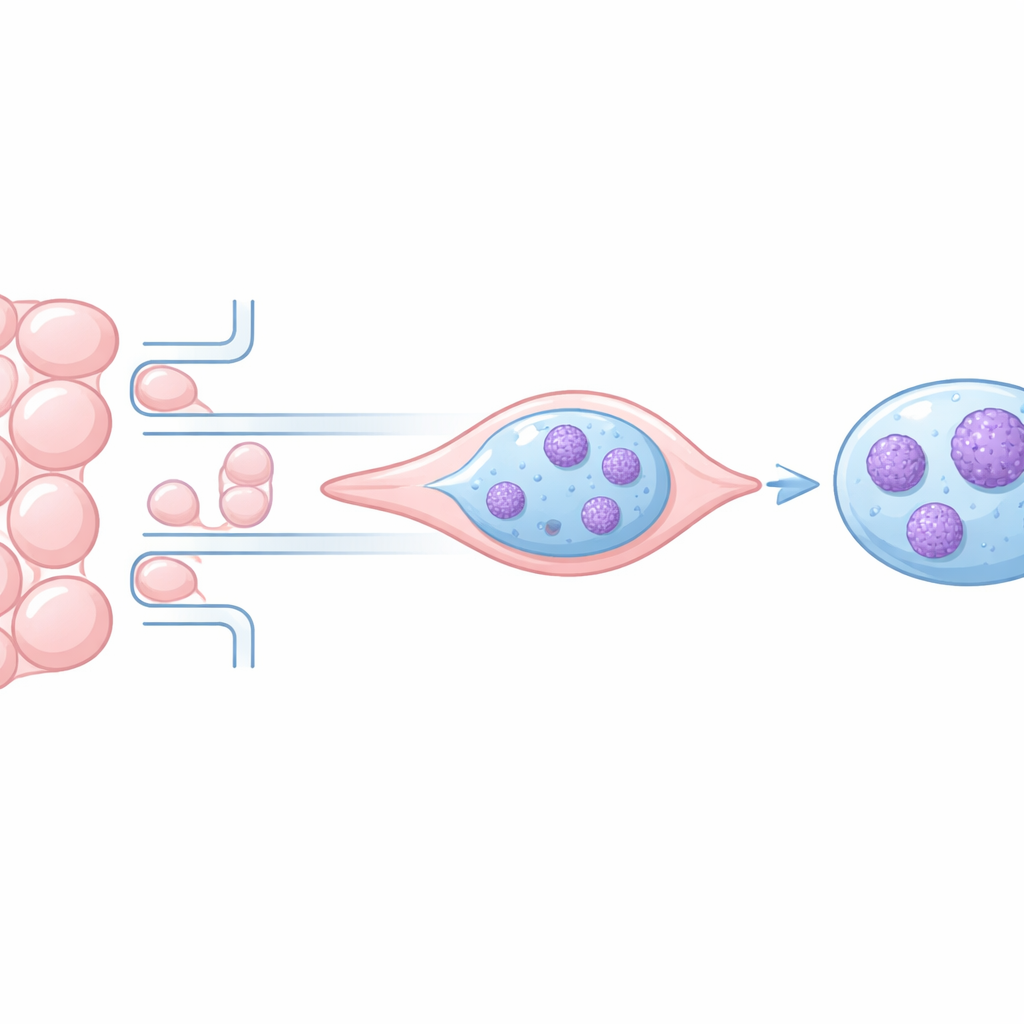
Le cellule tumorali che si staccano da un tumore devono strisciare attraverso piccoli interstizi nei tessuti e nei vasi sanguigni. Per farlo comprimono i loro componenti morbidi—e in particolare il nucleo, che ospita il DNA—attraverso spazi talvolta più stretti del nucleo stesso. Questo studio esplora cosa accade all’impacchettamento del DNA durante quelle compressioni ripetute e pone una domanda centrale: il nucleo torna semplicemente alla normalità, oppure conserva una sorta di “memoria meccanica” che potrebbe favorire la diffusione del cancro?
Perché l’impacchettamento del DNA è importante quando le cellule si muovono
All’interno del nucleo, il DNA è avvolto attorno a proteine e ripiegato nella cromatina, che può essere poco compatta o fortemente condensata. Le regioni meno compatte tendono ad essere attive, ospitando geni frequentemente espressi, mentre le regioni molto compatte sono più silenti. Quando le cellule migrano attraverso passaggi stretti, il nucleo si deforma, e lavori precedenti hanno mostrato che ciò può compattare temporaneamente la cromatina e persino danneggiare il DNA. Non era però chiaro se questi cambiamenti si invertissero completamente o lasciassero segni duraturi che possano modificare l’aggressività delle cellule tumorali.
Un piccolo labirinto per comprimere singole cellule tumorali
I ricercatori hanno costruito un dispositivo microfluidico su misura—un chip trasparente contenente decine di canali microscopici che alternano ripetutamente tratti larghi e stretti. Due diverse linee cellulari tumorali, entrambe ingegnerizzate in modo che la loro cromatina risplenda al microscopio, sono state guidate a percorrere questi canali mediante un attrattore chimico. L’imaging time-lapse ad alta risoluzione ha permesso al team di seguire ogni nucleo cellulare mentre si muoveva, misurando le dimensioni nucleari e mappando, fotogramma per fotogramma, i brillanti ammassi di cromatina altamente condensata in oltre 100 singole cellule.
Cosa succede al nucleo sotto pressione
Ogni volta che una cellula entrava in una costrizione stretta, il suo nucleo si riduceva bruscamente in area proiettata, riflettendo una riduzione reversibile del volume nucleare. Allo stesso tempo, la frazione del nucleo occupata da cromatina altamente condensata aumentava di picco—spesso di due o tre volte—per poi tornare ai livelli di base una volta che la cellula emergesse in una regione più ampia. Questo schema si ripeteva attraverso diverse costrizioni successive e in entrambe le linee cellulari tumorali, suggerendo che la quantità complessiva di cromatina densa è una risposta flessibile e a breve termine allo stress meccanico più che un cambiamento permanente. Tuttavia, un’analisi più attenta dei modelli di fluorescenza ha rivelato che durante la compressione aumentavano tanto i pixel a intensità molto alta quanto quelli a intensità molto bassa, suggerendo una riorganizzazione interna più complessa di una semplice compattazione uniforme.
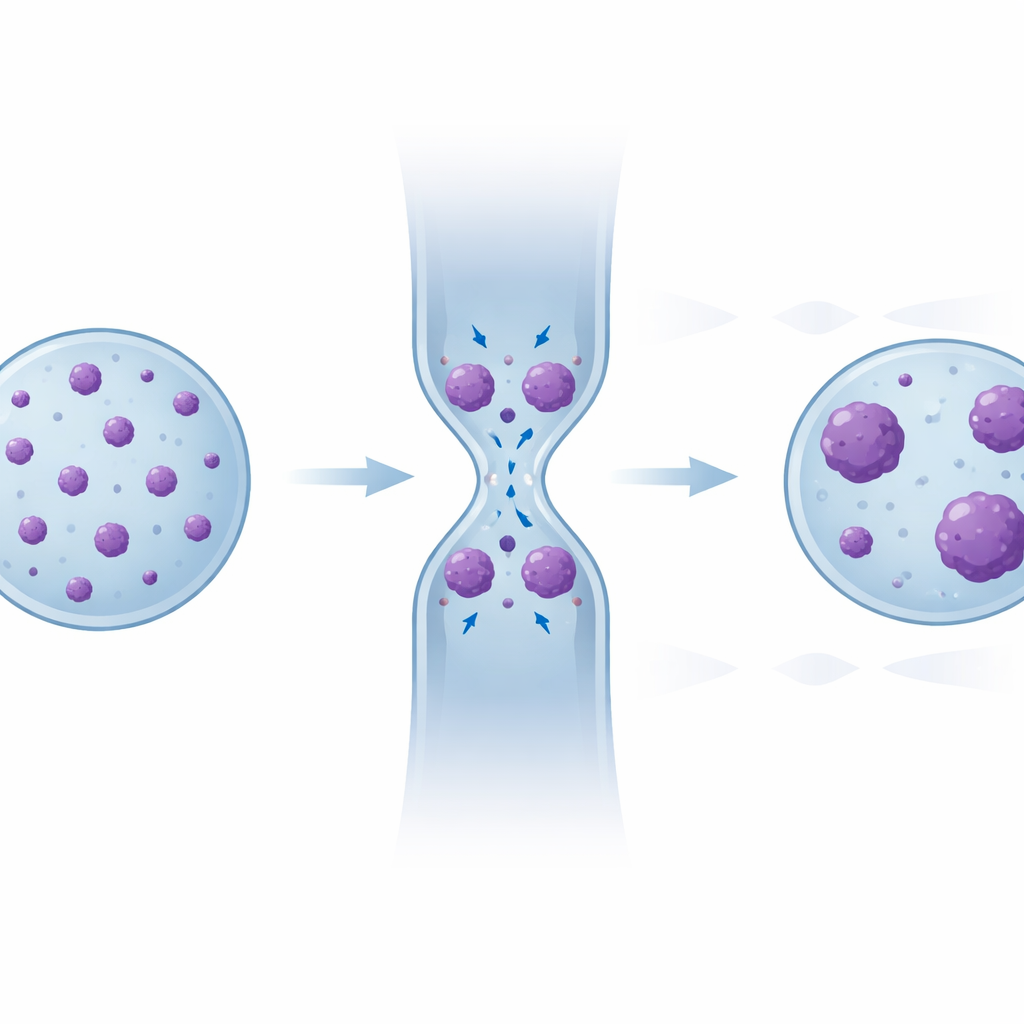
Memoria nascosta nel disegno degli ammassi di DNA
Per svelare quella riorganizzazione nascosta, il team ha esaminato ogni singolo ammasso di cromatina condensata—la sua dimensione e il numero di ammassi per nucleo—prima, durante e dopo il confinamento. Durante la compressione, i piccoli ammassi tendevano a confluire formando ammassi più grandi. Dopo il rilassamento del nucleo, l’area totale condensata tornava al livello iniziale, ma il pattern non si ristabiliva: rispetto allo stato di partenza, le cellule che avevano attraversato più costrizioni mostravano complessivamente meno ammassi, con una distribuzione sbilanciata verso dimensioni maggiori. Confronti statistici hanno confermato che le distribuzioni nelle successive regioni di “recupero” somigliavano sempre più a quelle osservate durante il confinamento. La colorazione immunofluorescente ha inoltre mostrato che molte di queste regioni dense sovrapponevano marcatori noti di cromatina «silente», e un modello al computer che rappresentava la cromatina come un polimero interagente ha riprodotto questa rilassamento parziale ma non completo semplicemente a partire dalla fisica di segmenti di DNA appiccicosi portati a contatto dalla deformazione.
Cosa significa per la diffusione del cancro e per terapie future
In termini pratici, lo studio mostra che quando i nuclei delle cellule tumorali vengono ripetutamente compressi, l’impacchettamento del DNA si comporta come una pallina antistress con memoria. Il nucleo può riprendere le dimensioni originali e la quantità complessiva di cromatina compatta può ritornare a un livello di base, ma il dettaglio del disegno degli ammassi di DNA denso non ritorna completamente allo stato iniziale. Dopo molti cicli di compressione, il nucleo presenta meno regioni dense ma di dimensioni maggiori, il che potrebbe modificare quali geni sono più o meno accessibili. Questa «memoria meccanica» potrebbe aiutare le cellule tumorali a tollerare meglio future deformazioni mentre invadono nuovi tessuti. Comprendere e, in ultima analisi, mirare a questo legame tra forze fisiche e organizzazione del DNA potrebbe aprire nuove strade per limitare le metastasi interrompendo il modo in cui le cellule tumorali si adattano allo stress meccanico.
Citazione: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Parole chiave: migrazione cellulare confinata, condensazione della cromatina, meccanica nucleare, memoria meccanica, metastasi del cancro