Clear Sky Science · it
Regolazione negativa della via NF-κB mediante la ligasi dell’ubiquitina Nedd4-1(NE)
Perché è importante spegnere l�27infiammazione
Il nostro sistema immunitario si affida a rapidi picchi di infiammazione per combattere infezioni e riparare lesioni, ma le stesse forze possono danneggiare i tessuti e favorire il cancro se rimangono attive troppo a lungo. Questo articolo esplora come le cellule umane e di altri primati evitino quel pericolo utilizzando un �22freno�22 intrinseco appena caratterizzato che placa uno dei principali sistemi d�27allarme del corpo una volta completato il suo compito.
Un interruttore d�27allarme centrale nelle nostre cellule
Al centro di questa storia c�27è NF-κB, una famiglia di proteine che funziona come un interruttore maestro per centinaia di geni coinvolti nell�27infiammazione, nella sopravvivenza cellulare e nell�27immunità. Quando le cellule percepiscono segnali di stress come la molecola infiammatoria TNFα, una catena di eventi libera NF-κB dalle sue �22proteine cappelliere�22 nel fluido intracellulare e gli permette di spostarsi nel nucleo, dove accende geni pro-infiammatori e pro-sopravvivenza. Poiché questa via è così potente, le cellule devono regolarne con precisione sia l�27attivazione sia lo spegnimento. L�27incapacità di disattivarla è stata collegata a malattie infiammatorie croniche e a molti tumori.
Un freno presente solo nei primati
I ricercatori si sono concentrati su Nedd4-1, membro di una grande famiglia di enzimi che marcano altre proteine con una piccola molecola chiamata ubiquitina. Questo marchio spesso segnala la distruzione o il riposizionamento delle proteine all�27interno della cellula, rimodellando le reti di segnalazione. Una variante di splicing di Nedd4-1, chiamata Nedd4-1(NE), è stata scoperta in precedenza ed è presente solo nei primati: porta un lungo segmento aggiuntivo nella porzione N-terminale che modifica la sua localizzazione cellulare e le sue specificità di riconoscimento. In contrasto con la forma standard di Nedd4-1, che può in alcuni contesti potenziare l�27attività di NF‑κB tramite altri partner, il gruppo ha scoperto che Nedd4-1(NE) ha l�27effetto opposto: attenua la segnalazione di NF‑κB, specialmente dopo esposizioni prolungate a TNFα.
Due modalità per tenere sotto controllo NF-κB
Per scoprire come funziona questo freno, gli autori hanno impiegato metodi di marcatura per prossimità e pull-down proteici per vedere quali molecole si associano fisicamente a Nedd4-1(NE). Hanno identificato componenti chiave della via NF‑κB, incluso la chinasi IKKβ e il precursore NF‑κB1 (noto anche come p105). Esperimenti di follow-up hanno mostrato che Nedd4-1(NE) aggiunge tag di ubiquitina a IKKβ, portandone alla degradazione. Con meno IKKβ disponibile, il suo bersaglio abituale IκBα non viene più fosforilato e degradato con la stessa efficienza. Di conseguenza, IκBα resta più stabile e mantiene la subunità attiva di NF‑κB, p50, sequestrata nel citosol, impedendole di entrare nel nucleo e attivare i geni infiammatori.
Un passaggio guidato da un adattatore verso il freno
Nedd4-1(NE) agisce anche a valle limitando i livelli dello stesso NF‑κB1. In questo caso l�27enzima non opera da solo: collabora con un altro proteina che tagga con ubiquitina, chiamata KPC1. KPC1 aiuta a processare il precursore NF‑κB1 p105 nella forma attiva p50 e risiede in compartimenti cellulari noti come endosomi tardivi, dove si trova anche Nedd4-1(NE). Il gruppo ha dimostrato che Nedd4-1(NE) può ubiquitinare KPC1 e che questo KPC1 modificato funge da adattatore, reclutando NF‑κB1 verso Nedd4-1(NE) sugli endosomi tardivi. Questo complesso a tre promuove la destabilizzazione sia di p105 sia di p50, riducendo ancora una volta il pool di NF‑κB che può raggiungere il nucleo.
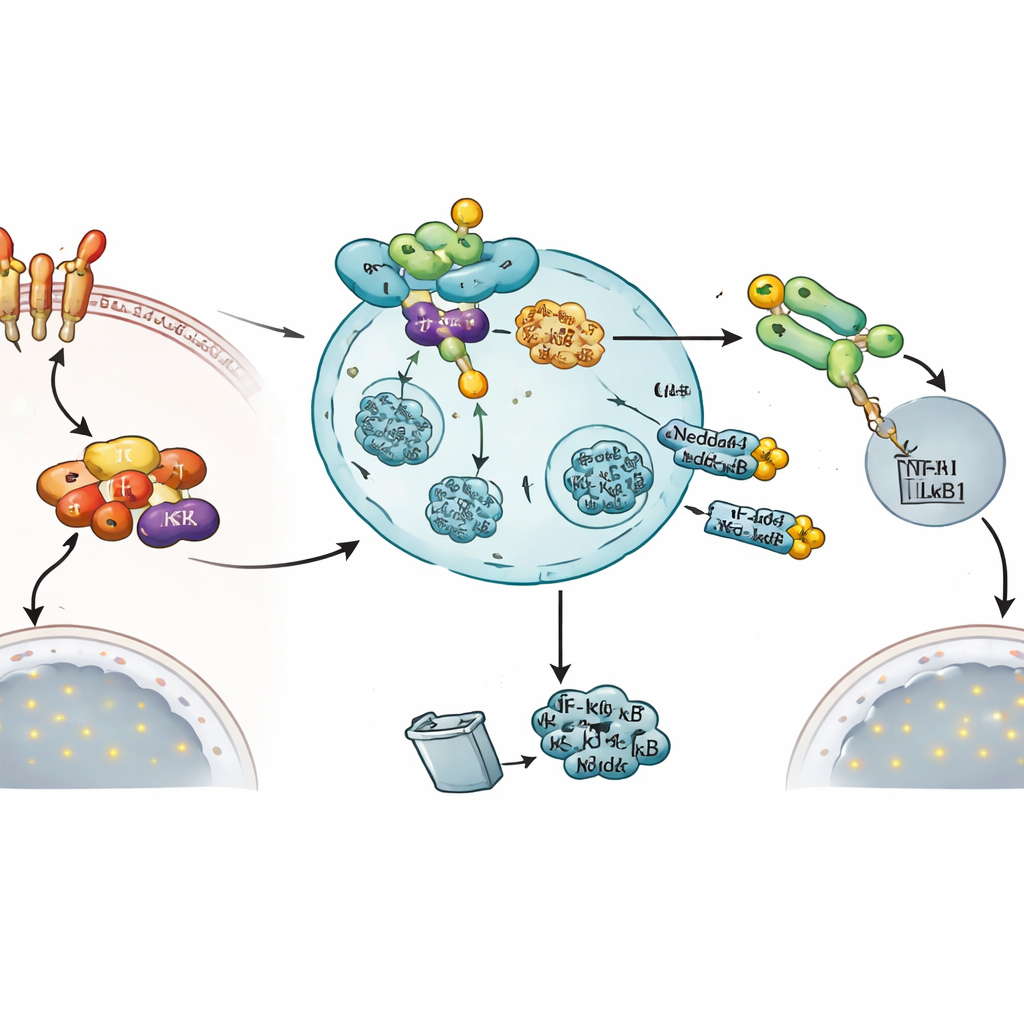
Un circuito di retroazione incorporato per terminare il segnale
Colpisce il fatto che lo stesso segnale che attiva NF‑κB sembra anche indurre questo freno. Quando le cellule sono state trattate con TNFα, i livelli di RNA messaggero di Nedd4-1(NE) sono aumentati in modo pronunciato, mentre la forma standard di Nedd4-1 non è cambiata. Letture funzionali hanno supportato l�27idea che Nedd4-1(NE) sia una valvola di spegnimento: l�27incremento di Nedd4-1(NE) attiva ha ridotto il movimento di NF‑κB1 verso il nucleo, abbassato l�27attività di un gene reporter sensibile a NF‑κB e diminuito l�27espressione di un gene infiammatorio regolato da NF‑κB, TNFAIP3. Nel loro insieme, questi risultati delineano un circuito di feedback negativo in cui l�27attivazione della via NF‑κB alla fine aumenta Nedd4-1(NE), che poi prende di mira due nodi critici—IKKβ e NF‑κB1—to riportare la risposta infiammatoria su livelli più bassi.
Cosa significa per la salute e la malattia
Per un pubblico generale, il messaggio chiave è che le nostre cellule incorporano un meccanismo di sicurezza aggiuntivo, specifico dei primati, per impedire che la segnalazione infiammatoria sfugga al controllo. Taggando selettivamente e riducendo componenti fondamentali del sistema NF‑κB, Nedd4-1(NE) contribuisce a terminare la risposta a TNFα e può favorire l�27equilibrio immunitario a lungo termine. Comprendere questo freno intrinseco potrebbe aprire nuove strade per trattare malattie in cui NF‑κB è cronicamente iperattivo, come i disordini autoimmuni e certi tumori, suggerendo modi per imitare o potenziare questo processo naturale di spegnimento.
Citazione: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Parole chiave: segnalazione NF-kB, infiammazione, ligasi dell�27ubiquitina, Nedd4-1(NE), TNF alfa