Clear Sky Science · it
Notch3 regola la plasticità fenotipica dei periciti nel cancro del colon-retto
Perché i vasi sanguigni intorno ai tumori sono importanti
Il cancro del colon-retto è uno dei tumori più comuni e letali a livello mondiale, eppure la maggior parte delle terapie è diretta direttamente alle cellule tumorali e spesso trascura il sistema di supporto circostante che favorisce la crescita tumorale. Questo articolo si concentra su un gruppo meno noto di cellule di supporto chiamate periciti, che avvolgono i piccoli vasi sanguigni. Svelando come un interruttore di segnalazione chiamato Notch3 modifichi il comportamento dei periciti, gli autori mostrano come l’apporto di sangue al tumore possa essere spinto verso vasi permeabili e caotici che favoriscono il cancro, oppure verso vasi più normali che possono rallentare la malattia e migliorare il trattamento. 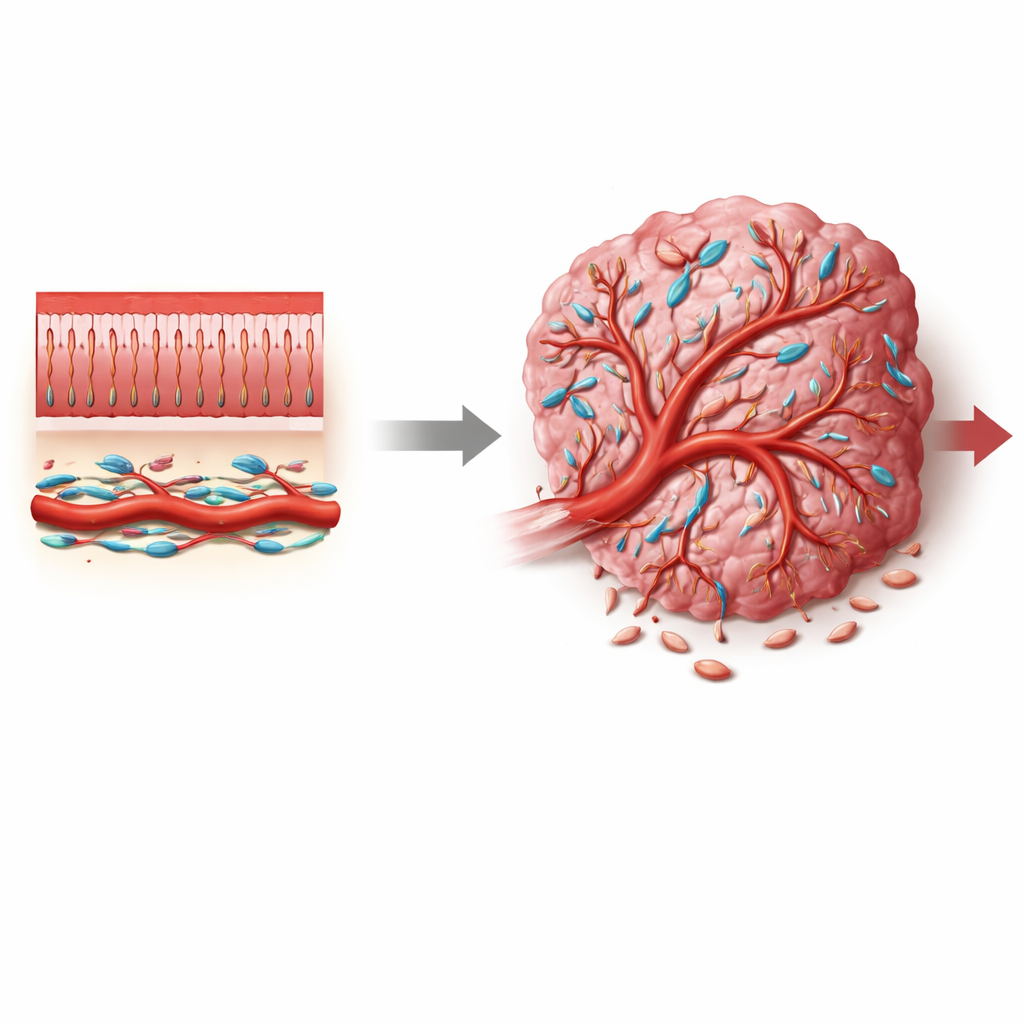
Gli aiutanti nascosti intorno ai vasi tumorali
I vasi sanguigni sono più di semplici tubi cavi. Nei tessuti sani, i piccoli vasi sono strettamente avvolti dai periciti—cellule specializzate che stabilizzano le pareti vascolari, controllano il flusso sanguigno e limitano le perdite. Nei tumori, tuttavia, questi periciti spesso appaiono e si comportano in modo diverso: possono staccarsi, proliferare o cambiare identità, contribuendo alla vascolarizzazione anomala e permeabile tipica dei tumori. Nei tumori del colon-retto, dove il microambiente è affollato di fibroblasti, cellule immunitarie e componenti vascolari, non era chiaro da dove provenissero i periciti associati al tumore, quali stati adottassero e quali segnali molecolari li spingessero verso ruoli che favoriscono il tumore.
Tracciare i periciti durante la formazione del tumore
Per seguire i periciti nel tempo, i ricercatori hanno utilizzato modelli murini di cancro del colon-retto associato a colite in cui potevano “marcare” geneticamente tipi cellulari specifici e osservare il loro destino. Hanno dimostrato che i periciti trovati nei tumori derivano in gran parte da periciti residenti nei tessuti normali che si espandono e proliferano con lo sviluppo del cancro, piuttosto che provenire da fonti distanti come il midollo osseo. Usando l’avanzata tecnica di sequenziamento dell’RNA a singola cellula, hanno catalogato decine di migliaia di cellule stromali da tumori murini e dal colon normale e hanno trovato che i periciti sono significativamente arricchiti nel microambiente tumorale. Hanno inoltre identificato una simile espansione di periciti in diversi dataset di cancro del colon-retto umano, sottolineando che non si tratta solo di un fenomeno specifico del topo.
Un interruttore molecolare che cambia il comportamento dei periciti
Il gruppo ha poi indagato quali segnali plasmino il comportamento dei periciti all’interno dei tumori e ha scoperto che Notch3—un recettore che permette alle cellule di comunicare con i vicini—è particolarmente attivo nei periciti tumorali. L’analisi computazionale della comunicazione cellula–cellula ha suggerito che i periciti sia inviano sia ricevono segnali correlati a Notch, in particolare attraverso partner presenti sulle cellule vascolari. Attivando artificialmente Notch3 nei periciti, i ricercatori hanno osservato che queste cellule proliferano di più ma esprimono meno proteine contrattili tipicamente associate al comportamento stabilizzante dei vasi. I vasi tumorali in questi topi sono diventati più grandi, più permeabili e rivestiti da un numero maggiore di cellule endoteliali in proliferazione, indicando una vascolarizzazione meno stabile. Al contrario, la cancellazione di Notch3 ha ridotto la proliferazione delle cellule endoteliali, ha ridotto le dimensioni dei vasi e ha diminuito le perdite, suggerendo uno spostamento verso vasi più normalizzati senza modificare drasticamente il numero o le dimensioni precoci dei tumori. 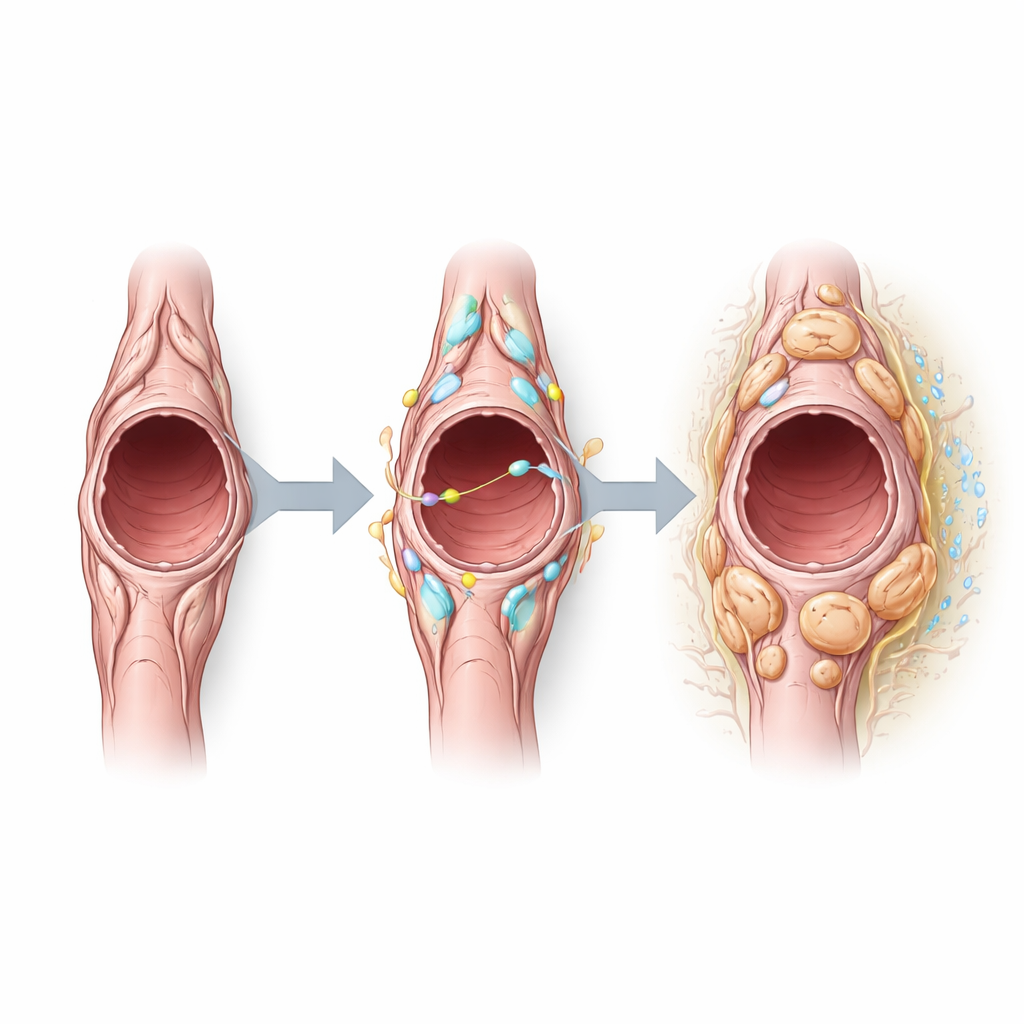
Molte facce dei periciti all’interno dei tumori
Oltre ai cambiamenti semplici di tipo acceso/spento, lo studio ha rivelato che i periciti tumorali esistono in diversi stati distinti. Alcuni sottogruppi mostrano caratteristiche di cellule altamente contrattili, altri producono grandi quantità di matrice extracellulare, alcuni presentano tratti infiammatori e una sotto-popolazione porta persino firme solitamente viste nelle cellule endoteliali. L’attività di Notch3 non era distribuita in modo omogeneo: era arricchita in una popolazione “sintetica” o produttrice di matrice e bassa nel sottogruppo più contrattili. Le analisi di traiettoria hanno suggerito che i periciti possono passare da uno stato contrattili verso uno sintetico e proliferativo all’aumentare dell’attività di Notch3. Quando gli autori hanno esaminato i dati umani sul cancro del colon-retto, hanno trovato uno spettro comparabile di stati dei periciti e hanno nuovamente osservato una maggiore attività di un gene target di Notch3 nei periciti associati al tumore e in quelli proliferanti, rispecchiando i risultati nel topo.
Trasformare il caos vascolare in un’opportunità terapeutica
Nel complesso, il lavoro ritrae Notch3 come una manopola chiave che regola l’identità dei periciti e, attraverso di essi, la struttura e la funzione dei vasi sanguigni tumorali. Un’elevata attività di Notch3 spinge i periciti verso uno stato proliferativo e meno contrattili, associato a vasi ingranditi e permeabili che favoriscono la progressione tumorale. Una bassa attività di Notch3 è associata a periciti più contrattili, cellule endoteliali più calme e a una vascolarizzazione più normalizzata che può contenere la crescita tumorale e migliorare la somministrazione dei farmaci. Mirando specificamente a Notch3 nei periciti, terapie future potrebbero orientare i vasi tumorali lontano dal caos e verso la stabilità, offrendo un nuovo approccio per trattare il cancro del colon-retto avanzato in combinazione con farmaci esistenti.
Citazione: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Parole chiave: cancro del colon-retto, microambiente tumorale, periciti, segnalazione Notch3, vasi sanguigni tumorali