Clear Sky Science · it
TRIM47 endoteliale regola l'integrità della barriera emato-encefalica e la cognizione tramite la via di segnalazione KEAP1/NRF2 nei topi
Perché proteggere i vasi cerebrali più piccoli è importante
La malattia dei piccoli vasi cerebrali è un disturbatore silenzioso nel cervello. Danneggia i vasi sanguigni più minuti, aumenta il rischio di ictus e erode gradualmente memoria e capacità di pensiero, eppure i medici mancano ancora di terapie che affrontino le cause biologiche di fondo. Questo studio esplora una proteina specifica, TRIM47, presente nelle cellule che rivestono i vasi cerebrali, per porre una domanda semplice ma cruciale: aiuta a mantenere intatta la barriera protettiva emato-encefalica, e questo conta per la cognizione?
Un guardiano al confine del cervello
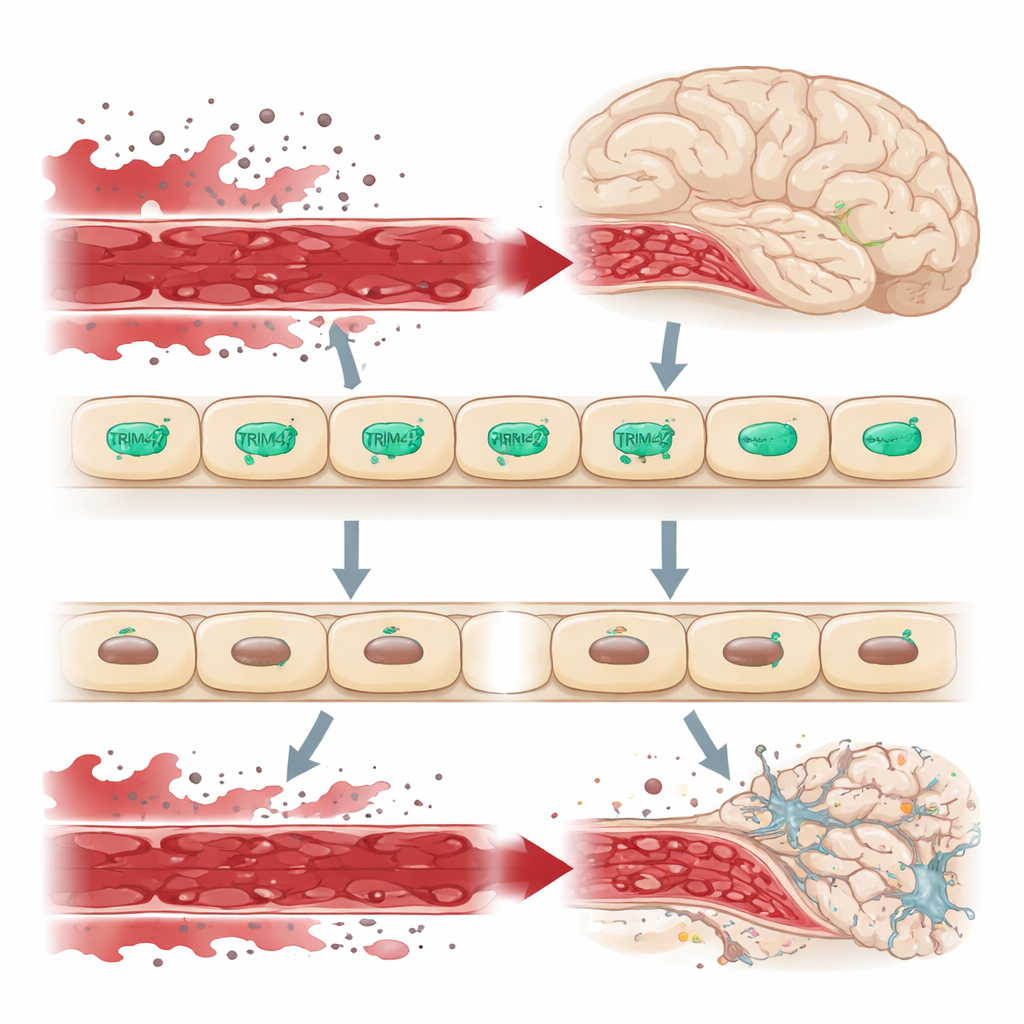
Il cervello è protetto dalla circolazione del resto del corpo dalla barriera emato-encefalica, un rivestimento strettamente sigillato di cellule endoteliali che controlla rigorosamente ciò che può entrare nel tessuto cerebrale. Quando questa barriera perde, molecole dannose provenienti dal sangue filtrano nel cervello, stressando neuroni e cellule di supporto e contribuendo a condizioni come la demenza. Studi genetici su ampie popolazioni umane avevano indicato un tratto di DNA contenente il gene TRIM47 come regione di rischio per la malattia dei piccoli vasi cerebrali. TRIM47 è particolarmente attivo nelle cellule endoteliali cerebrali, suggerendo che potrebbe essere un guardiano importante di questa barriera.
Come TRIM47 protegge le cellule dallo stress ossidativo
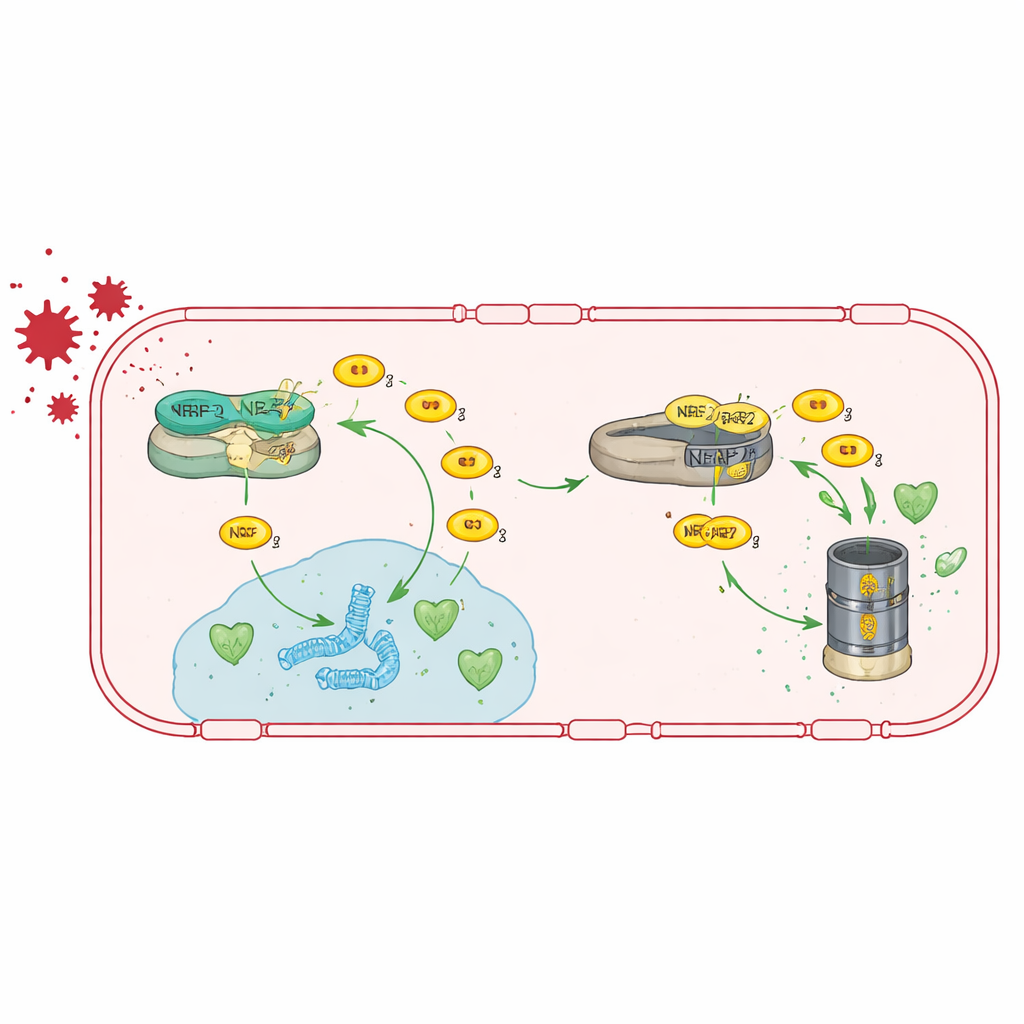
Gli autori hanno prima studiato cellule endoteliali cerebrali umane coltivate in laboratorio e hanno ridotto i livelli di TRIM47 usando interferenza con RNA. Questo ha scatenato ampi cambiamenti nell'attività genica, con la rete maggiormente influenzata centrata su NRF2, un regolatore maestro delle difese antiossidanti della cellula. In condizioni normali, NRF2 è tenuto sotto controllo da un'altra proteina, KEAP1, che lo indirizza verso la degradazione. Il gruppo ha dimostrato che TRIM47 si lega a KEAP1 e aiuta a impedire che NRF2 venga distrutto. Con TRIM47 presente, NRF2 può accumularsi, spostarsi nel nucleo e attivare geni che disintossicano le specie reattive dell'ossigeno. Quando TRIM47 viene perso, i livelli di NRF2 diminuiscono, i geni antiossidanti sono meno attivi e le cellule endoteliali diventano più vulnerabili allo stress ossidativo.
Dai vasi che perdono ai problemi di memoria nei topi
Per vedere come questo meccanismo si manifesta in un cervello vivo, i ricercatori hanno ingegnerizzato topi privi del gene Trim47 in tutto l'organismo e un'altra linea in cui Trim47 poteva essere eliminato solo nelle cellule endoteliali. Gli animali adulti di entrambi i modelli hanno sviluppato chiari problemi nell'apprendimento spaziale e nella memoria, fallendo compiti come il labirinto a Y e il Morris water maze nonostante un movimento normale. L'esame dei loro cervelli ha rivelato che la barriera emato-encefalica era diventata permeabile: piccoli traccianti fluorescenti e proteine del sangue sono sfuggiti dai vasi nel tessuto circostante. Proteine chiave della “sigillatura” che formano giunzioni strette e di adesione tra le cellule endoteliali, in particolare Claudin-5 e Occludin, risultavano ridotte. Gli astrociti vicini, le cellule di supporto a forma di stella che reagiscono rapidamente a lesioni, sono diventati attivati, sebbene a questo stadio vi fosse poco segno di infiammazione diffusa o perdita di neuroni.
Riattivare la via antiossidante
Poiché TRIM47 lavora principalmente aumentando l'attività di NRF2, il gruppo ha testato se fosse possibile aggirarne la perdita stimolando direttamente NRF2. Hanno somministrato ai topi privi di Trim47 una dieta contenente tert-butylidrossichinone (tBHQ), un composto noto per stabilizzare NRF2 e attivare i suoi geni bersaglio. Questo trattamento ha ripristinato l'attività dei geni antiossidanti nelle cellule endoteliali cerebrali, ha riportato l'espressione dei geni delle giunzioni strette verso valori normali e ha ridotto la perdita della barriera emato-encefalica. In modo notevole, ha anche normalizzato l'attivazione degli astrociti e ha recuperato le prestazioni degli animali nei test di memoria, suggerendo che rafforzare questa via antiossidante può invertire sia i problemi vascolari sia quelli cognitivi, almeno nei topi.
Indizi dal sangue umano e prossimi passi
Per collegare gli esperimenti nei topi alla malattia umana, i ricercatori hanno analizzato proteine correlate alla via NRF2 in campioni di sangue di migliaia di persone sottoposte a risonanza magnetica cerebrale. I livelli di diverse proteine regolate da NRF2 erano associati a marcatori di imaging della malattia dei piccoli vasi, come spazi perivascolari dilatati e alterazioni della materia bianca. Ciò supporta l'idea che la segnalazione TRIM47–NRF2 sia rilevante nelle persone, non solo negli animali sperimentali, e che queste proteine potrebbero fungere da biomarcatori della gravità o della progressione della malattia.
Cosa significa per la salute cerebrale
Nel complesso, il lavoro ritrae TRIM47 come una guardia molecolare che aiuta i vasi sanguigni cerebrali a resistere ai danni ossidativi stabilizzando il sistema antiossidante NRF2. Quando TRIM47 manca o è compromessa, la barriera emato-encefalica si indebolisce, si accumulano danni cerebrali sottili e la memoria comincia a fallire. Riattivare la via NRF2 può riparare la barriera e riportare la cognizione nei topi, evidenziando questo asse di segnalazione come un promettente bersaglio terapeutico per le forme vascolari di demenza. Sebbene il tBHQ in sé non sia adatto come farmaco per gli esseri umani, composti più sicuri che potenziano NRF2 o strategie che imitino il ruolo protettivo di TRIM47 potrebbero un giorno contribuire a preservare la salute cerebrale rafforzando i suoi vasi più piccoli e fragili.
Citazione: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Parole chiave: malattia dei piccoli vasi cerebrali, barriera emato-encefalica, TRIM47, via NRF2, demenza vascolare