Clear Sky Science · it
È necessaria una via inter‑subunitaria per il legame entropicamente guidato e negativamente cooperativo dei nucleotidi ciclici nel canale HCN2
Come i minuscoli interruttori pacemaker del cuore percepiscono i segnali chimici
Ogni battito cardiaco e molti ritmi cerebrali dipendono da canali microscopici che si aprono e si chiudono nelle membrane delle nostre cellule. Questi canali, chiamati canali pacemaker HCN, sono controllati non solo dalla tensione elettrica ma anche da piccole molecole messaggere note come nucleotidi ciclici. Questo studio pone una domanda apparentemente semplice ma dalle vaste implicazioni: come si legano queste minuscole molecole al canale HCN2 in modo coordinato, e come possono difetti sottili in quel processo contribuire a disturbi come l’epilessia?
Un dimmer molecolare per i ritmi del corpo
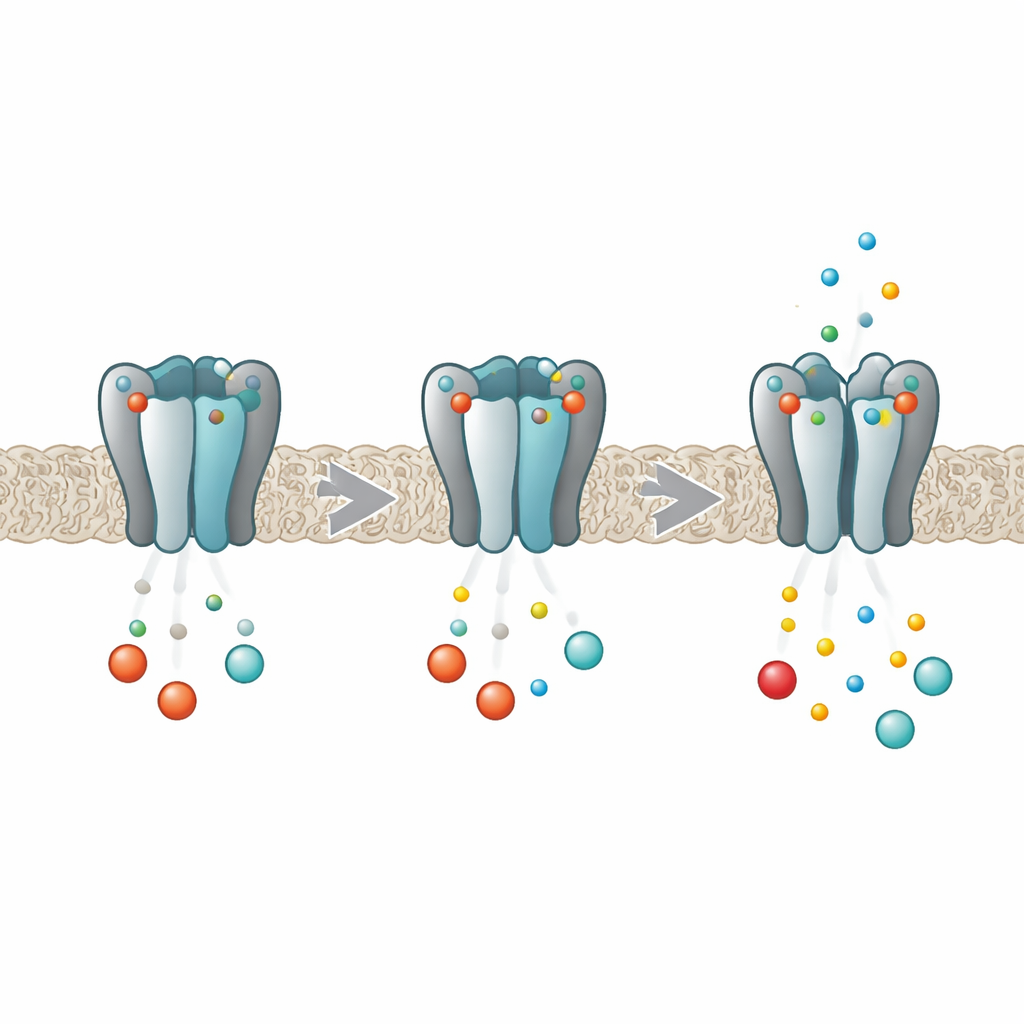
I canali HCN funzionano come dimmer per l’attività elettrica nelle cellule del cuore e del cervello. Ogni canale è composto da quattro subunità proteiche identiche che insieme formano un poro centrale attraverso cui scorrono gli ioni. All’interno di ciascuna subunità si trova una tasca che può legare nucleotidi ciclici come cAMP e cGMP. Quando questi messaggeri si legano, facilitano l’apertura del poro, aumentando la corrente pacemaker. Lavori precedenti hanno mostrato che nella variante HCN2 il legame non avviene in modo indipendente in ciascuna tasca; piuttosto, i quattro siti si influenzano a vicenda in modo che la prima molecola si leghi più facilmente delle successive, un comportamento noto come cooperatività negativa. Il nuovo lavoro si è proposto di scoprire esattamente come le quattro subunità comunicano tra loro durante questo processo.
Subunità che percepiscono i vicini
I ricercatori hanno combinato simulazioni al computer con misure in laboratorio su pezzi isolati del canale HCN2. Utilizzando lunghe simulazioni di dinamica molecolare, hanno osservato come la regione a coda del canale — la parte che contiene le tasche per i nucleotidi ciclici e il cosiddetto C‑linker che connette al poro — flette e oscilla al variare del numero di molecole di cAMP o cGMP legate. Hanno scoperto che quando un messaggero si fissava in una subunità, non stabilizzava semplicemente quella subunità da sola. Al contrario, modificava sottilmente la stabilità dei vicini, rendendoli talvolta più rigidi, talvolta più flessibili, pur senza grandi cambiamenti nella forma complessiva della proteina. Queste influenze tra vicini dipendevano da quanti siti erano occupati e da dove si trovavano attorno all’anello, in accordo con quanto previsto dalla cooperatività negativa.
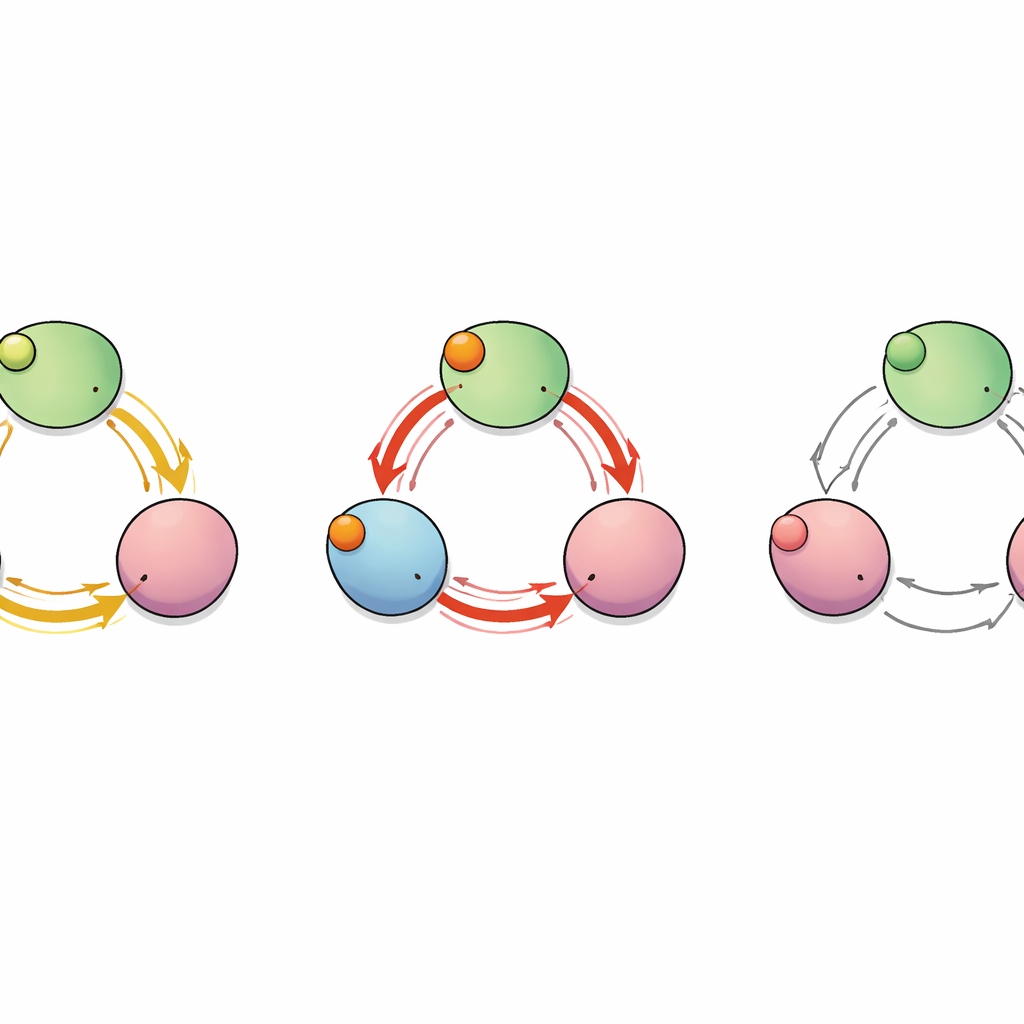
Un percorso nascosto tra le subunità
Per mappare come il “segnale” del legame viaggia attraverso la proteina, il team ha trattato il canale come una rete di amminoacidi interagenti. Hanno calcolato quali residui si muovevano in modo correlato durante le simulazioni e hanno utilizzato strumenti della teoria dei grafi per identificare i percorsi di comunicazione più brevi ed efficienti dalle tasche di legame ai segmenti del C‑linker che controllano il poro. Questa analisi ha rivelato diverse rotte possibili, ma due hanno prevalso: una che rimane all’interno di una singola subunità e un’altra che salta da una subunità alla sua vicina. Lungo questa via inter‑subunitaria, un singolo residuo — un glutammato nella posizione 488 (E488) — si è comportato da hub critico attraverso cui passavano molti dei percorsi più brevi, suggerendo che potrebbe essere un punto di rilè chiave per il legame cooperativo.
Mutazioni che interrompono la conversazione
Gli autori si sono quindi rivolti a esperimenti con le code purificate del canale per testare l’importanza di questo percorso. Hanno modificato E488 e la tirosina vicina in posizione 459 (Y459), che si trova sulla subunità adiacente dove la via arriva. Utilizzando la diffusione dinamica della luce, hanno confermato che le proteine mutanti si assemblavano ancora in complessi a quattro subunità, ma non mostravano più il forte irrigidimento indotto dal ligando tra le subunità osservato nella proteina normale. La titolazione calorimetrica isoterma, che misura i piccoli calori di legame, ha rivelato un cambiamento ancora più marcato: l’HCN2 selvatico mostrava due eventi di legame distinti, un primo passo ad alta affinità guidato principalmente da un aumento di entropia (maggiore movimento interno), seguito da tre passi a affinità più bassa. Al contrario, i mutanti in E488 o Y459 mostravano un unico modo di legame di affinità modesta che mancava di questo favorevole impulso entropico e aveva perso la tipica cooperatività negativa.
Perché cambiamenti sottili di entropia contano
Mettendo insieme questi elementi, lo studio dipinge il quadro del canale HCN2 come un anello dinamico di quattro subunità connesse da specifici “percorsi di conversazione”. Quando il primo nucleotide ciclico si lega, modifica i moti di parti distanti dell’anello attraverso E488 e Y459, rendendo meno favorevoli i successivi eventi di legame e sintonizzando la risposta del poro. Questo effetto non è guidato da grandi riorganizzazioni strutturali ma da spostamenti nella flessibilità interna — cambi di entropia invisibili nelle istantanee statiche ma cruciali per la funzione. Le mutazioni che interrompono i residui chiave lungo questa via inter‑subunitaria zittiscono la conversazione, annullano la cooperatività negativa e sono collegate a malattie come l’epilessia generalizzata idiopatica. Per il lettore non specialista, la conclusione è che gli interruttori vitali per cuore e cervello dipendono da sottili “sussurri” molecolari tra le subunità proteiche, e comprendere questi sussurri aiuta a spiegare sia i ritmi normali sia ciò che accade quando si guastano.
Citazione: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Parole chiave: canale ionico HCN2, legame dei nucleotidi ciclici, cooperatività negativa, comunicazione allosterica, mutazione associata all’epilessia