Clear Sky Science · it
Una piccola molecola attiva allostericamente la secrezione dipendente da SecA
Trasformare il molo di spedizione batterico in sovraccarico
I batteri sopravvivono esportando costantemente proteine attraverso minuscoli passaggi nelle loro membrane. Queste esportazioni li aiutano a costruire pareti cellulari, secernere tossine e adattarsi allo stress—processi al centro di molte infezioni. Questo studio descrive una piccola molecola, chiamata HSI#6, che fa qualcosa di insolito: invece di bloccare questa macchina di esportazione, la trasforma in una modalità iperattiva e meno selettiva. Capire come funziona questo interruttore potrebbe sia rivelare nuove strategie antibatteriche sia offrire al settore biotecnologico un modo per aumentare la secrezione di proteine su richiesta.
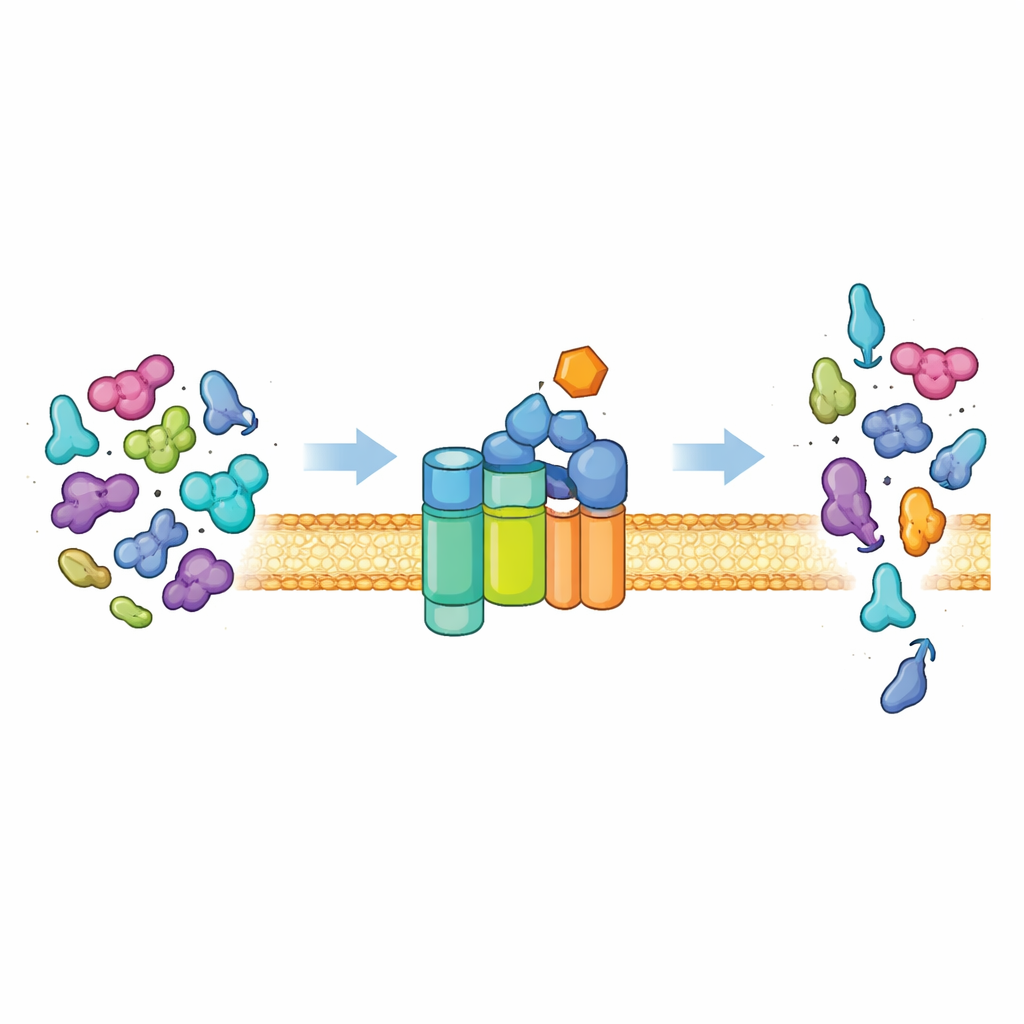
La porta d’uscita delle proteine della cellula
La maggior parte dei batteri esporta proteine fuori dalla cellula usando una via universale nota come sistema Sec. Al centro c’è un canale di membrana (SecYEG) e una proteina motore (SecA) che consuma carburante cellulare (ATP) per spingere catene proteiche non ripiegate attraverso il canale. In condizioni normali, questo sistema è pignolo. Esporta principalmente “preproteine” che portano speciali etichette di indirizzo, note come peptidi segnale, oltre a caratteristiche aggiuntive nel loro dominio principale. Queste caratteristiche sono necessarie per trasformare SecA da uno stato tranquillo e a bassa attività in un motore potente. Solo le proteine che presentano la giusta combinazione di segnali possono sbloccare la piena attività, garantendo che la cellula esporti il carico corretto e mantenga le proteine citoplasmatiche ordinarie al sicuro all’interno.
Una piccola molecola che sveglia il motore
I ricercatori hanno scoperto HSI#6 in uno screening di composti che interferiscono con la secrezione proteica batterica e la crescita. Test biochimici hanno mostrato che HSI#6 si lega direttamente a SecA con affinità micromolare e modifica l’efficienza con cui utilizza l’ATP. In soluzione, fa sì che SecA trattenga l’ATP più saldamente; quando SecA è associata al canale, HSI#6 migliora sia il legame con l’ATP sia la velocità di consumo dell’ATP. Questo schema è l’impronta di un attivatore allosterico: una molecola che si lega in un sito della proteina ma altera l’attività in un altro sito lontano. Diversamente dai clienti proteici naturali, HSI#6 non deve comportarsi come un carico per stimolare il motore—semplicemente regola la dinamica interna di SecA in modo che l’intero traslocasi diventi cataliticamente pronto.
Da filtro selettivo a nanomacchina promiscua
Una volta che HSI#6 è legato, il sistema Sec non insiste più sui soliti segnali di esportazione. In esperimenti in provetta, il composto ha circa raddoppiato la secrezione di una preproteina standard e ha reso il complesso più resistente all’azoturo di sodio, un noto inibitore di SecA. Ancora più significativo, HSI#6 ha permesso alla macchina normale, di tipo selvatico, di muovere proteine che sono completamente prive di peptidi segnale, così come proteine che normalmente risiedono nel citoplasma. Nelle cellule batteriche vive, lo stesso effetto è stato osservato usando reporter basati sulla fosfatasi alcalina: quando proteine citoplasmatiche sono state fuse a un enzima secreto, la presenza di HSI#6 ha causato un netto aumento dell’attività secreta senza modificare la quantità di proteina prodotta. In altre parole, HSI#6 disaccoppia efficacemente l’esportazione dai normali controlli di identità dei clienti, trasformando il sistema Sec in una pompa di esportazione a largo spettro per qualsiasi proteina sufficientemente non ripiegata.
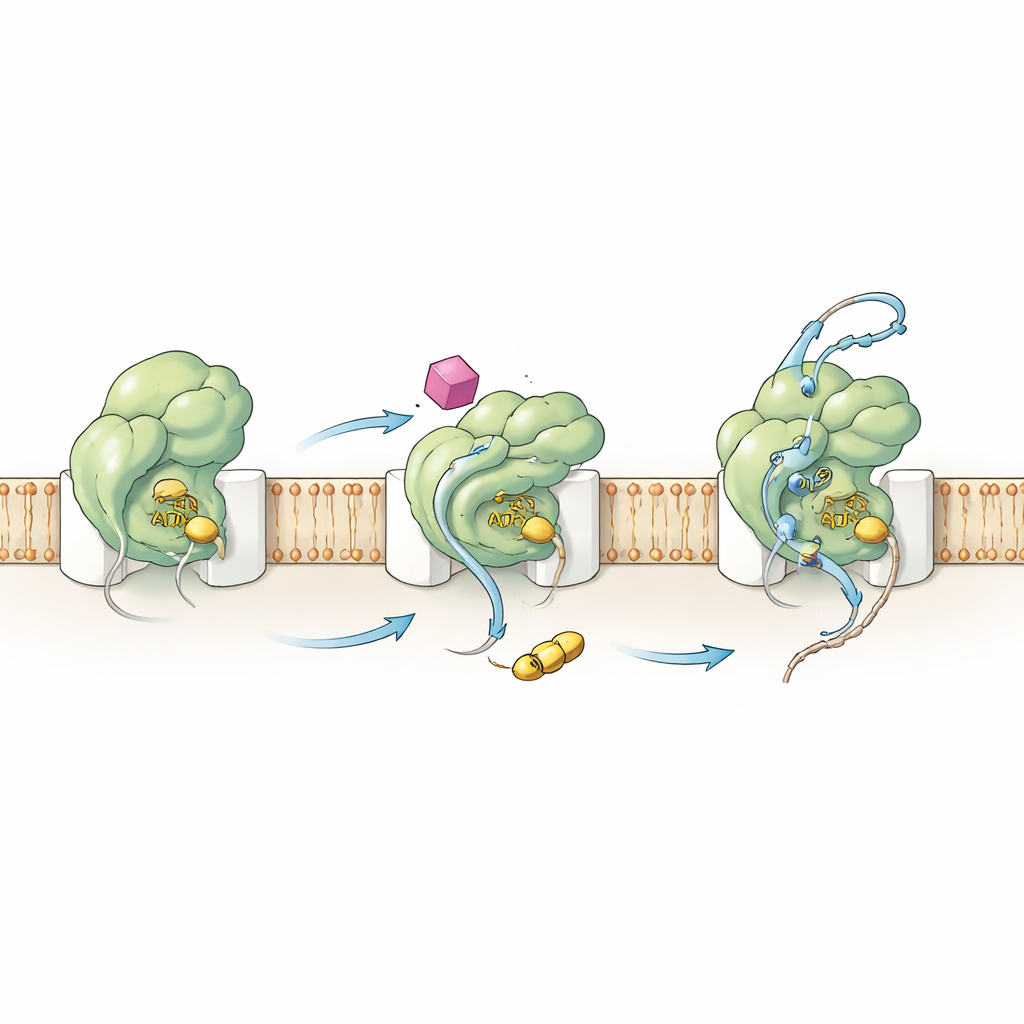
Riprogrammare il motore dall’interno
Per comprendere come HSI#6 inneschi questo comportamento, il team ha esaminato sia la chimica sia i movimenti di SecA. Misure cinetiche hanno mostrato che il composto sposta il passaggio chiave di attivazione a monte: il complesso SecA–canale diventa cataliticamente attivo anche prima che un cliente proteico si leghi. HSI#6 aiuta anche SecA a rilasciare il carburante esausto (ADP), un passaggio normalmente lento e limitante, e quindi favorisce un più rapido ciclo dell’ATP. Usando spettrometria di massa con scambio idrogeno–deuterio, gli autori hanno mappato come HSI#6 rimodella la flessibilità di diverse regioni di SecA. Il composto allenta selettivamente parti della proteina che percepiscono i clienti e si connettono al canale, mentre irrigidisce una regione di impalcatura che probabilmente ospita il suo sito di legame. Il modello di movimenti risultante somiglia a uno stato già impegnato, “acceso”, della traslocasi, suggerendo che HSI#6 stabilizzi una forma attivata—favorendo possibilmente anche una SecA monomerica legata al canale—senza alcun cliente presente.
Perché questo è importante per la medicina e la biotecnologia
Dimostrando che una piccola molecola può attivare allostericamente SecA e privarla della sua normale selettività verso i clienti, questo lavoro rivela un nuovo modo di controllare una macchina batterica centrale. Per le malattie infettive, una secrezione forzata e incontrollata potrebbe indebolire i patogeni drenando energia e perturbando i loro programmi di esportazione finemente regolati, rendendo gli attivatori simili a HSI#6 punti di partenza attraenti per la progettazione di antibiotici—o guide per creare futuri inibitori che blocchino le stesse caratteristiche regolatorie. Per la biotecnologia, lo stesso principio potrebbe essere riutilizzato per aumentare la secrezione di proteine ricombinanti utili, senza la necessità di peptidi segnale ingegnerizzati o complesse modifiche genetiche. In sostanza, lo studio dimostra che il “molo di spedizione” proteico batterico può essere riprogrammato chimicamente, aprendo nuove strade sia per combattere i microrganismi sia per sfruttarli come fabbriche microscopiche.
Citazione: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Parole chiave: secrezione proteica batterica, traslocasi SecA, attivazione allosterica, regolatori a piccole molecole, scoperta di farmaci antibatterici