Clear Sky Science · it
Un pseudochinasi a istidina modula la crescita polare e la forma cellulare in Streptomyces venezuelae
Come i batteri costruiscono corpi delicatamente ramificati
I batteri filamentosi del genere Streptomyces vivono nel suolo e formano reti ramificate di filamenti che ricordano i funghi microscopici. Questi batteri sono una fonte naturale primaria di antibiotici e il loro successo dipende da quanto precisamente controllano dove e come crescono le loro cellule. Questo studio scopre una proteina precedentemente sconosciuta che aiuta Streptomyces a mantenere stabili le punte in crescita e ordinate le loro diramazioni, offrendo nuovi spunti su come vengono costruite e mantenute forme cellulari complesse.
Crescere solo alle punte
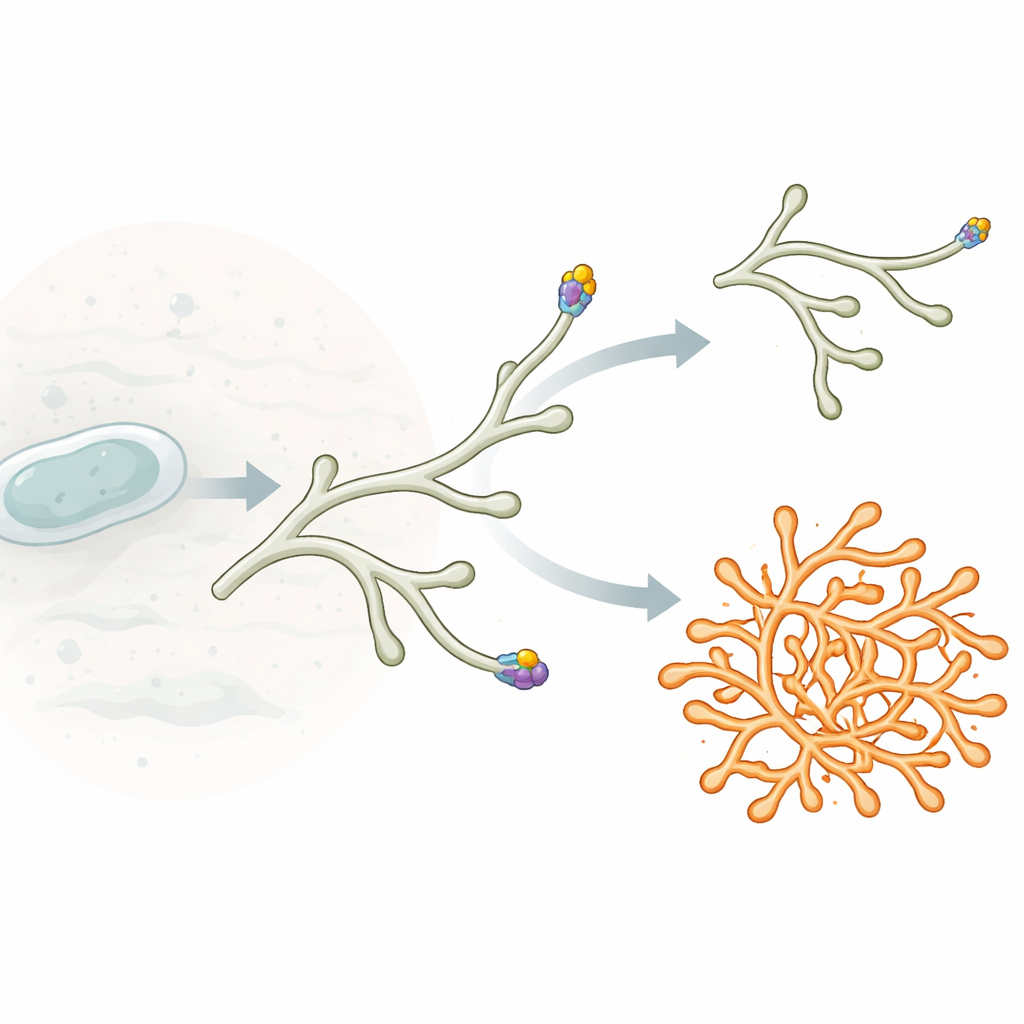
A differenza di molti batteri a bastoncello familiari che si espandono lungo tutta la loro lunghezza, Streptomyces crescono principalmente alle loro punte. Ogni filamento, o ifa, si allunga aggiungendo nuovo materiale di parete cellulare solo in una piccola zona alla estremità. Questa zona di crescita è organizzata da un assemblaggio proteico chiamato polarisoma. Al suo centro si trova una proteina chiamata DivIVA, che tende ad accumularsi alle estremità cellulari curve e segnala dove deve essere inserito nuovo materiale di parete. Quando piccoli ammassi di DivIVA si staccano dalla punta principale e si posizionano lungo il fianco di un’ifa, possono maturare in nuove zone di crescita, dando origine a diramazioni laterali e a una rete miceliale finemente ramificata.
Un nuovo regolatore di forma alla punta
Gli autori hanno cercato componenti finora sconosciuti del polarisoma di Streptomyces. Tirando giù DivIVA da estratti cellulari e osservando con cosa co-purificava, hanno scoperto una grande proteina, ora nominata PsmA (da polar growth and shape modulator A). PsmA somiglia, nel layout dei domini, a una comune enzima di segnalazione batterica chiamata chinasi a istidina, con regioni simili a sensori, un nucleo catalitico centrale e un dominio ricevitore collegati da un lungo segmento flessibile. Tuttavia, un’analisi più attenta ha mostrato che PsmA manca di aminoacidi chiave necessari per trasferire gruppi fosfato e non mostra attività chinasi rilevabile, classificandola come una “pseudochinasi” che probabilmente agisce più come partner strutturale o impalcatura che come enzima classico.
Quando manca il controllore di forma
Per sondare il ruolo di PsmA, i ricercatori hanno eliminato il suo gene in Streptomyces venezuelae. Le colonie del mutante erano più piccole e più dense, con una superficie increspata. Al microscopio, le ife vegetative risultavano più spesse, più irregolari e mostravano una diramazione alle punte drasticamente aumentata. Invece di estendersi in modo regolare e produrre occasionalmente rami laterali, molte punte si dividevano in due o più estremità in crescita, creando un micelio iperramificato e compatto. È importante notare che la capacità di formare filamenti aerei e spore rimaneva in gran parte intatta, indicando che PsmA agisce principalmente durante la crescita vegetativa alla punta piuttosto che nella fase più tardiva di sporulazione.
Mantenere la zona di crescita coesa
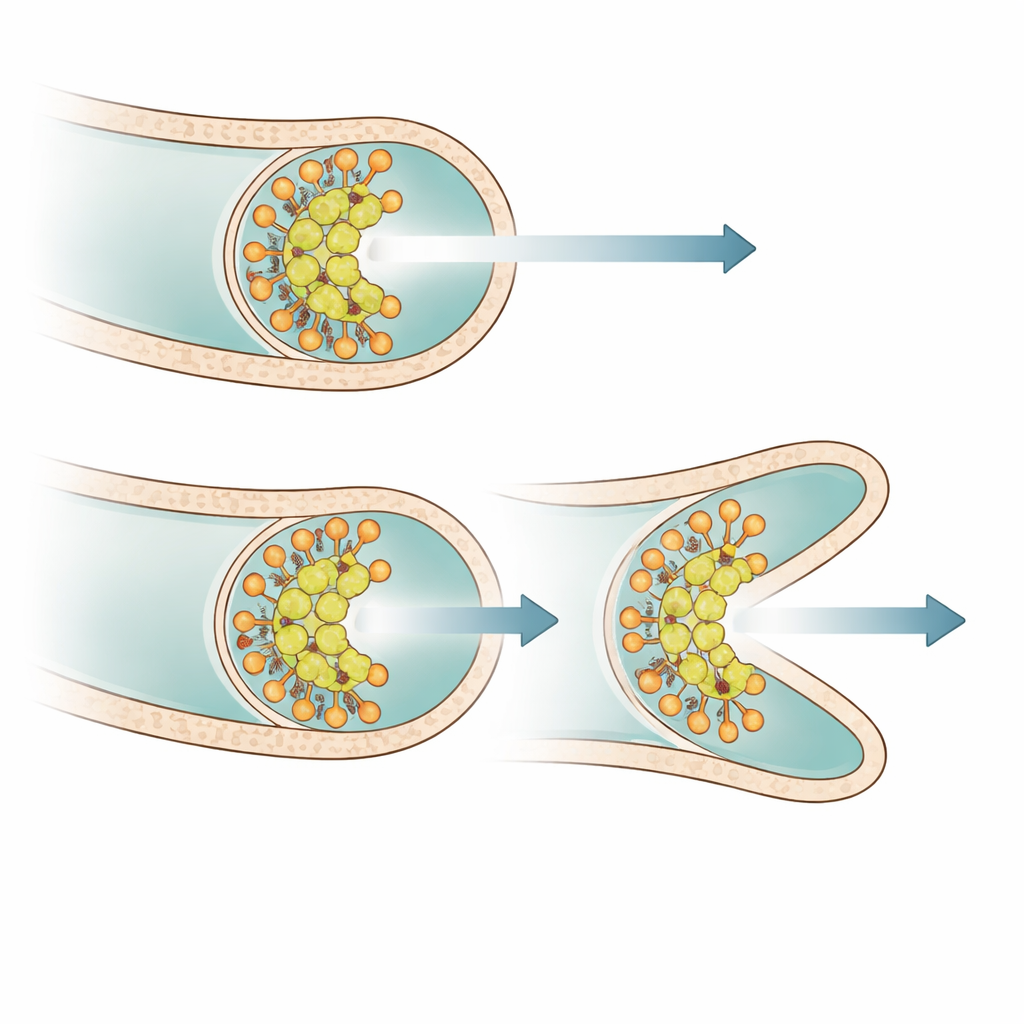
Marcando le proteine con fluorescenza, gli autori hanno visualizzato dove si localizza PsmA nelle cellule vive. PsmA formava punti concentrati proprio all’apice delle ife in crescita, sovrapponendosi strettamente a DivIVA e a un’altra proteina di punta, Scy, ma distinto da FilP, che si localizza appena dietro la punta. In assenza di PsmA, gli ammassi di DivIVA alle estremità ifali diventavano più ampi e irregolari nella forma. L’imaging temporale ha rivelato che questi ammassi distorti tendevano molto più frequentemente a dividersi in due parti di dimensioni simili. Ciascuna parte quindi promuoveva la crescita della propria punta, portando a biforcazioni molto vicine alla punta originale e spiegando il modello di iperramificazione. Quando la produzione di PsmA è stata riattivata nel mutante, gli ammassi di DivIVA si sono rapidamente ristretti, la forma della punta è diventata più liscia e la divisione eccessiva si è ridotta.
Agire in parallelo con altri fattori di punta
PsmA non è l’unica proteina che aiuta a stabilizzare le punte di Streptomyces. Lavori precedenti avevano identificato Scy e FilP, due proteine allungate a spirale alfa che si associano a DivIVA e influenzano il comportamento della punta. Doppi mutanti privi sia di PsmA che di Scy o FilP mostravano difetti di crescita ancora più gravi e miceli più densi e aggrovigliati rispetto a qualsiasi singolo mutante, pur rimanendo vitali. Questo schema suggerisce che PsmA agisca in larga parte in parallelo a Scy e FilP: tutti e tre contribuiscono in modi parzialmente indipendenti a mantenere coesa la zona di crescita e a impedirne la frammentazione in più punte concorrenti.
Cosa significa per l’architettura batterica
Nel complesso, i risultati presentano PsmA come un partner non enzimatica che affina la stabilità e la dinamica del polarisoma basato su DivIVA alle punte ifali di Streptomyces. Piuttosto che agire attraverso vie di segnalazione classiche che attivano o disattivano geni, PsmA sembrerebbe operare direttamente all’estremità in crescita, probabilmente come organizzatore strutturale che aiuta gli ammassi di DivIVA a mantenere una zona di crescita focalizzata e singola. Quando PsmA manca, la macchina della punta diventa troppo instabile, si divide troppo spesso e produce una diramazione eccessiva. Comprendere questo tipo di controllo architettonico locale non solo approfondisce la nostra conoscenza fondamentale della biologia cellulare batterica, ma può anche informare sforzi per manipolare i modelli di crescita di Streptomyces a fini biotecnologici e per la produzione di antibiotici.
Citazione: Singh Mavi, P., Flärdh, K. A histidine pseudokinase modulates polar growth and cell shape in Streptomyces venezuelae. Commun Biol 9, 345 (2026). https://doi.org/10.1038/s42003-026-09620-z
Parole chiave: Streptomyces, polarità cellulare, morfogenesi batterica, pseudochinasi, diramazione ifale