Clear Sky Science · it
La restrizione alimentare notturna altera la spermatogenesi nei topi tramite l’omeostasi di KYNA derivata dal microbiota intestinale
Perché il momento in cui mangi potrebbe contare per i futuri padri
Molti sanno che evitare gli spuntini notturni o provare il digiuno intermittente può fare bene al peso e alla glicemia. Ma questo studio sui topi pone una domanda diversa: limitare il cibo a certe ore potrebbe danneggiare la fertilità maschile se la tempistica entra in conflitto con l’orologio interno del corpo? Tracciando come gli schemi di alimentazione rimodellano i batteri intestinali e un mediatore chimico poco noto, i ricercatori rivelano una catena di eventi che sfocia in meno spermatozoi e di qualità peggiore.
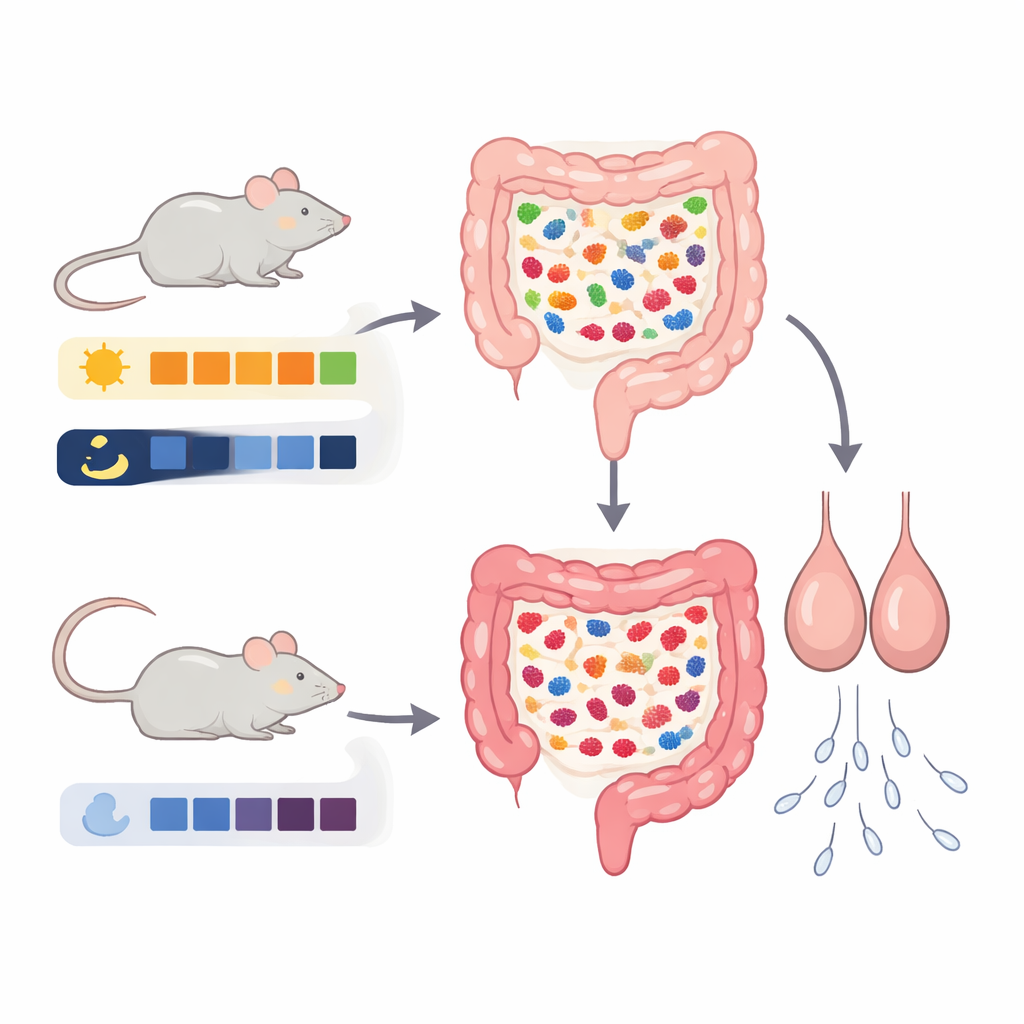
Finestre di alimentazione e l’orologio interno del corpo
Il gruppo ha lavorato con topi maschi e ha impostato tre schemi alimentari. Un gruppo mangiava liberamente. Un secondo gruppo poteva mangiare solo diurno, e un terzo solo di notte. È importante: questi topi non erano a dieta; potevano mangiare quanto volevano, ma in orari diversi. Dopo quattro settimane, i topi nutriti solo di notte mostravano testicoli più piccoli e una concentrazione e motilità dello sperma peggiori, pur non consumando meno cibo complessivamente. I livelli di ormoni legati allo stress cambiarono, ma l’ormone del sonno rimase sostanzialmente invariato, suggerendo che il danno derivi più dalle risposte metaboliche e di stress a pasti mal sincronizzati che da una semplice perturbazione dell’orologio maestro cerebrale.
Cosa andava storto all’interno dei testicoli
Osservando da vicino il tessuto testicolare al microscopio, gli scienziati riscontrarono che i topi nutriti di notte avevano meno cellule spermatiche in via di sviluppo a metà del processo di maturazione, mentre le cellule staminali iniziali e le cellule di supporto risultavano per lo più invariate. Le misure di danno chimico legato allo stress ossidativo erano più alte, suggerendo che l’ambiente testicolare fosse diventato più ostile e meno equilibrato. Interessante notare che gli stadi finali della modellazione dello spermatozoo—la formazione dell’acrosoma sulla testa dello spermatozoo—non risultarono fortemente compromessi. Questo indica che i punti deboli quando l’alimentazione è disallineata rispetto ai ritmi corporei sono le fasi iniziali e intermedie della produzione di spermatozoi.
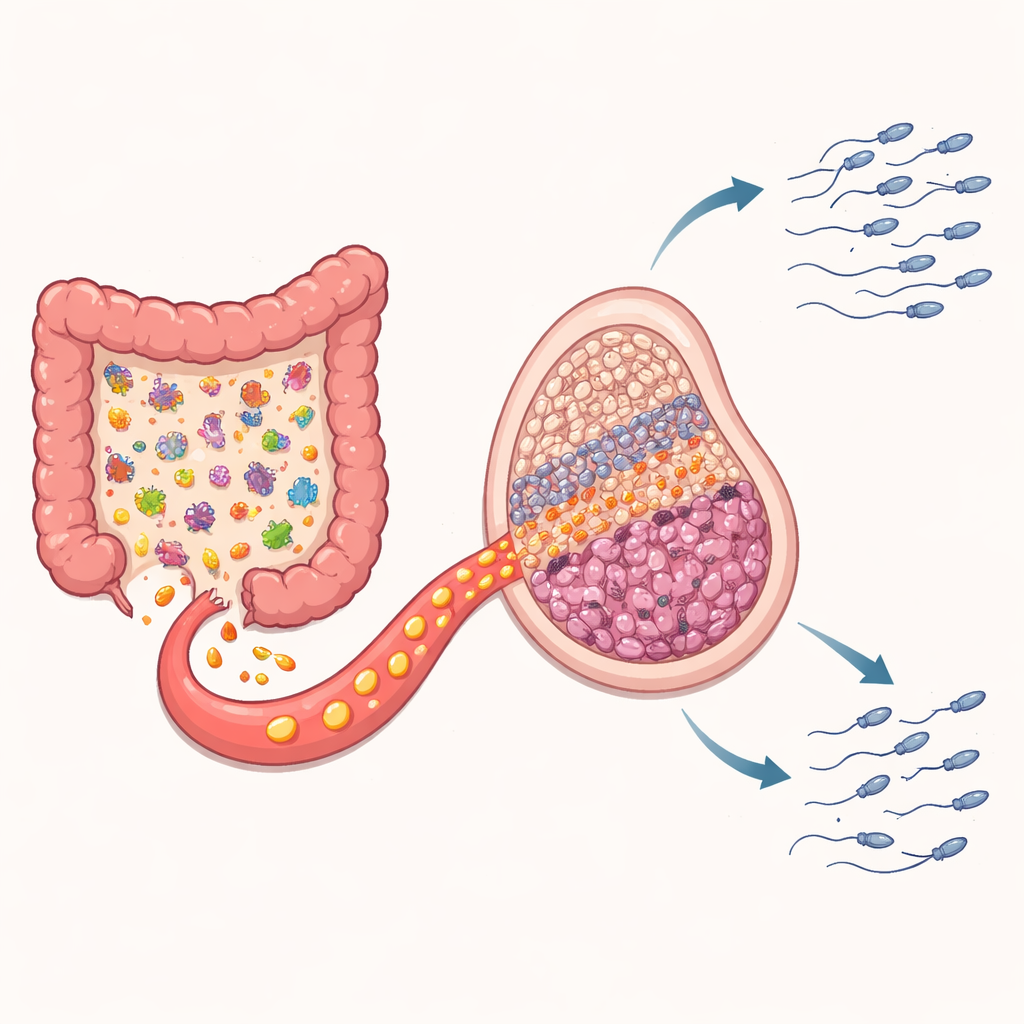
Il ruolo nascosto dell’intestino e un mediatore chimico chiave
Poiché i microbi intestinali sono noti per variare con la tempistica dei pasti e per inviare segnali in tutto il corpo, i ricercatori hanno esaminato le comunità intestinali degli animali. I topi nutriti solo di notte mostrarono un riassetto distinto dei batteri intestinali rispetto sia al gruppo a volontà sia a quello con restrizione diurna. Alcune specie, in precedenti studi associate a infiammazione e scarsa qualità dello sperma, divennero più abbondanti. Quando il team ha profilato centinaia di piccole molecole prodotte nell’intestino, una è emersa in modo significativo: l’acido chinurenico, o KYNA, un prodotto di degradazione dell’amminoacido triptofano. I livelli di KYNA erano più alti nell’intestino e nel sangue solo nei topi nutriti di notte. Analisi statistiche hanno collegato questo aumento di KYNA alla sovracrescita di specifici gruppi batterici, sostenendo l’idea che i microbi alterati guidassero il cambiamento.
Testare se il KYNA danneggia direttamente lo sperma
Per capire se il KYNA fosse un semplice spettatore o un agente attivo, gli scienziati somministrarono KYNA per via orale a topi sani per quattro settimane, a dosi studiate per imitare i livelli incrementati osservati con l’alimentazione notturna. I risultati furono sorprendentemente simili a quelli del gruppo nutrito di notte: riduzione della dimensione dei testicoli, meno spermatozoi in sviluppo e conteggi e motilità dello sperma inferiori, mentre i livelli di testosterone rimasero in gran parte stabili. In colture cellulari, il KYNA si rivelò direttamente tossico per cellule simili a quelle spermatiche in sviluppo a dosi più elevate, ma fu meno aggressivo verso le cellule produttrici di ormoni. Nel tessuto testicolare, il KYNA ridusse l’attività di un tipo di recettore e attivò fortemente un’altra via nota, da precedenti studi, per innescare la morte cellulare nelle cellule germinali. Nel complesso, questi risultati sostengono che l’eccesso di KYNA, generato nell’intestino e trasportato dal sangue, svolga un ruolo centrale nell’arrestare la produzione di spermatozoi.
Cosa significa per gli uomini e il timing dei pasti
Per i lettori comuni, il messaggio non è che tutte le pratiche di alimentazione a tempo limitato siano dannose. Anzi, i topi con restrizione alla dieta diurna in questo studio non mostrarono gli stessi problemi riproduttivi, e alcune prove nell’uomo suggeriscono benefici metabolici da digiuni temporizzati con cura. Piuttosto, il lavoro evidenzia che il “quando” mangiamo può influenzare la fertilità maschile, almeno nei topi, rimodellando il microbiota intestinale e aumentando un mediatore chimico che saboterebbe silenziosamente la formazione degli spermatozoi. Sebbene siano necessari ulteriori studi per confermare quanto ciò si applichi agli uomini, vista la diversità tra specie e la complessità dello stile di vita, lo studio aggiunge una nota di cautela: allineare i modelli alimentari ai ritmi quotidiani naturali e mantenere una comunità intestinale sana potrebbe essere importante non solo per peso e glicemia, ma anche per proteggere la capacità di diventare padri.
Citazione: Yang, D., Xie, D., Li, C. et al. Nighttime-restricted feeding disrupts spermatogenesis in mice via gut microbiota-derived KYNA homeostasis. Commun Biol 9, 354 (2026). https://doi.org/10.1038/s42003-026-09619-6
Parole chiave: fertilità maschile, digiuno a tempo limitato, microbioma intestinale, acido chinurenico, ritmo circadiano