Clear Sky Science · it
LncRNA P4HA2-AS1 promuove la fibrosi interstiziale renale tramite ubiquitinazione K63 mediata da TRIM32 di ULK1 e disfunzione autofilica
Perché la cicatrizzazione renale è importante
La malattia renale cronica colpisce centinaia di milioni di persone nel mondo e spesso avanza silenziosamente finché dialisi o trapianto non diventano l’unica opzione per sopravvivere. Al centro di questo declino c’è un processo chiamato cicatrizzazione, in cui il tessuto renale normale viene gradualmente sostituito da materiale rigido e non funzionale. Questo studio pone una domanda semplice ma cruciale: quali interruttori molecolari all’interno delle cellule renali le spingono verso questa dannosa cicatrizzazione, e tali interruttori possono essere disattivati?
Un interruttore RNA nascosto nelle cellule renali
I nostri reni filtrano il sangue grazie a una rete elaborata di minuscoli tubuli. Quando questi tubuli vengono danneggiati da ostruzione del flusso urinario, iperglicemia o improvvisa perdita di apporto di sangue, possono rispondere depositando tessuto cicatriziale tra le cellule. I ricercatori hanno analizzato i reni di topo sottoposti a diversi tipi di lesione e li hanno confrontati con reni sani mediante sequenziamento dell’RNA, una tecnica che legge quali geni sono attivi. Hanno scoperto che una molecola poco conosciuta chiamata P4HA2-AS1, un RNA lungo non codificante che non produce proteine, era costantemente elevata nei reni danneggiati che formano cicatrici e nelle cellule renali umane sottoposte a stress in laboratorio. Questo RNA si trovava principalmente nella parte citoplasmatica delle cellule, suggerendo che potrebbe controllare altre proteine lì.
Ridurre l’RNA per proteggere il rene
Per verificare se P4HA2-AS1 sia solo un marcatore o un effettivo motore del danno, il gruppo ha ridotto i suoi livelli nei topi e in colture di cellule renali umane. In un modello murino consolidato in cui un uretere viene legato per causare ostruzione a lungo termine, abbassare questo RNA tramite un vettore virale mirato ha attenuato molti segni della fibrosi: i tubuli sono rimasti più integri, c’è stata meno deposizione di collagene e altre proteine di cicatrice tra le cellule e i marcatori della funzionalità renale nel sangue sono migliorati. In colture di cellule renali umane, la riduzione di P4HA2-AS1 ha anche attenuato la risposta a un forte segnale pro-fibrotico, il TGF‑β, portando a una minore produzione di fibronectina, collagene e altri fattori pro-fibrotici. Questi esperimenti mostrano che questo RNA non è semplicemente un marker del danno ma alimenta attivamente il processo di cicatrizzazione.
Autofagia: dalla pulizia al danno
I ricercatori hanno quindi indagato come questo RNA eserciti il suo effetto dannoso. I dati di espressione genica e di imaging hanno indicato l’autofagia, il sistema di riciclo intrinseco della cellula che degrada proteine e organelli danneggiati. In condizioni normali, l’autofagia è un processo di manutenzione benefico, ma quando è iperattivato per troppo tempo può spingere i reni danneggiati verso una riparazione maladattativa e la fibrosi. Nelle cellule renali stressate, P4HA2-AS1 ha aumentato il flusso attraverso il percorso autofagico, determinando un accumulo di vescicole di riciclo. Quando l’RNA è stato bloccato, questo riciclo eccessivo è tornato verso la normalità, sia nelle cellule sia nei reni dei topi ostruiti. Topi privi di ULK1, un enzima centrale per l’avvio dell’autofagia, sono risultati anch’essi protetti dalla fibrosi, e in questi animali la sovraespressione di P4HA2-AS1 non ha più potuto aggravare il danno, collegando solidamente gli effetti dell’RNA a questo percorso.
Una catena molecolare in tre parti
Approfondendo, il team ha usato tecniche biochimiche di “pesca” per identificare proteine che si legano fisicamente a P4HA2-AS1. Una è emersa in particolare: TRIM32, un enzima che marca altre proteine con piccoli “segnali” molecolari chiamati ubiquitine. L’RNA si lega a TRIM32 e lo protegge dalla degradazione, aumentando i suoi livelli all’interno delle cellule renali. TRIM32 stabilizzato, a sua volta, attacca una specifica catena di ubiquitina a ULK1. Piuttosto che destinare ULK1 alla degradazione, questa catena funziona come una potenziazione, aumentando la capacità di ULK1 di avviare l’autofagia. Quando gli scienziati hanno rimosso TRIM32 nei topi o lo hanno silenziato nelle cellule renali, sia la fibrosi sia l’autofagia eccessiva sono diminuite. Reintrodurre TRIM32 in cellule in cui P4HA2-AS1 era stato bloccato ha parzialmente ristabilito la risposta fibrotica, dimostrando che questo enzima è un anello centrale nella catena.
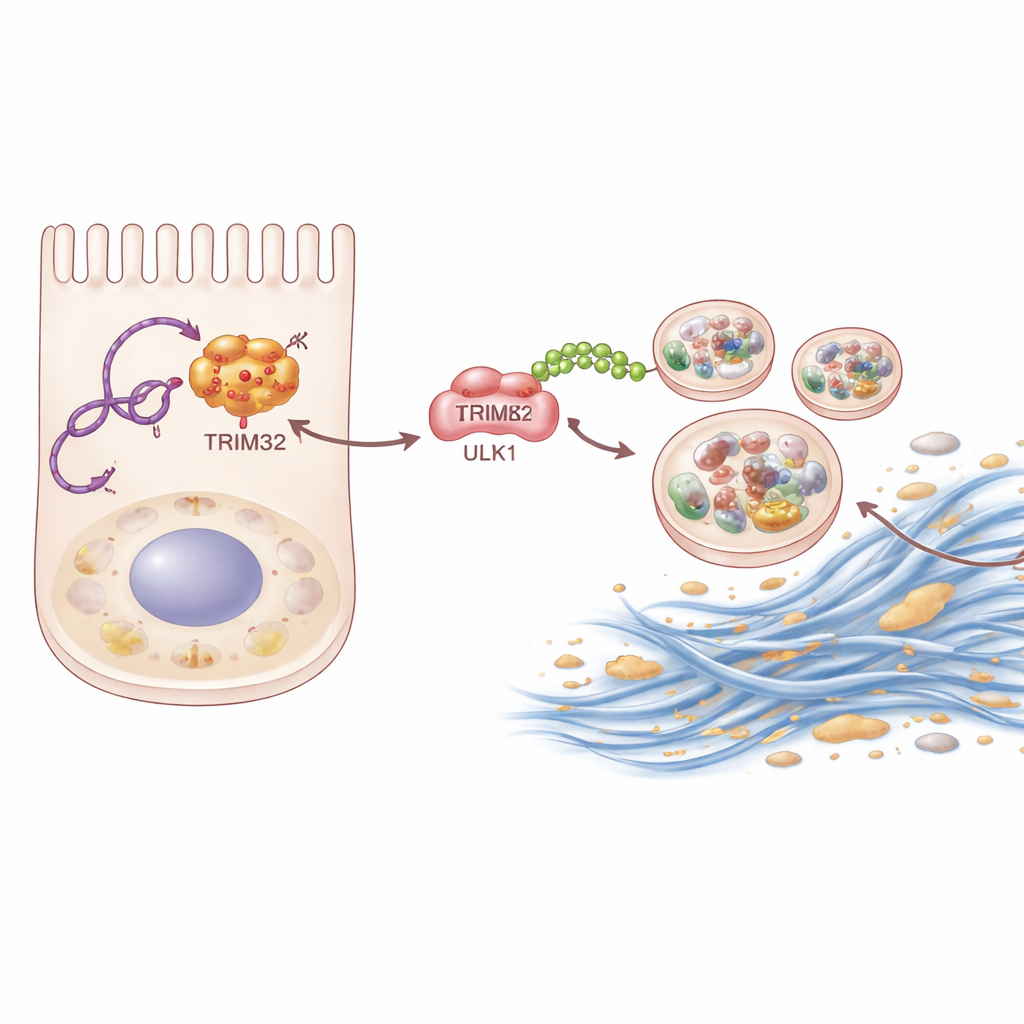
Nuove strade verso reni meno rigidi
Nel complesso, il lavoro rivela una via molecolare finora sconosciuta che collega RNA lungo non codificante, marcatura proteica e riciclo cellulare all’accumulo di tessuto cicatriziale renale. Nei reni danneggiati, P4HA2-AS1 aumenta, stabilizza TRIM32, potenzia ULK1 e spinge l’autofagia oltre la sua sfera utile, favorendo infine l’accumulo di proteine fibrotiche e la perdita di funzione. Per il pubblico generale, il messaggio è che la cicatrizzazione renale non è una scatola nera inevitabile: è guidata da interruttori identificabili che potrebbero essere bersagli farmacologici. Mirare all’asse P4HA2-AS1–TRIM32–ULK1 — abbassando l’RNA anomalo, moderando TRIM32 o regolando l’attività di ULK1 — potrebbe un giorno offrire nuovi trattamenti per rallentare o prevenire la progressione della malattia renale cronica.
Citazione: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Parole chiave: malattia renale cronica, fibrosi renale, autofagia, RNA lungo non codificante, tubuli renali