Clear Sky Science · it
Inibitori della trascrittasi inversa consentono la generazione in vitro di spermatidi fertili da testicoli fetali di topo
Trasformare le cellule germinali precoci in spermatozoi funzionanti
I trattamenti per l’infertilità e la ricerca di base dipendono dalla comprensione di come le cellule germinali immature nel testicolo si trasformino in spermatozoi. Questo studio dimostra che è ora possibile indurre testicoli fetali di topo molto precoci, prelevati subito dopo la determinazione del sesso dell’embrione, a completare questa trasformazione interamente in provetta. Regolando con cura l’ambiente chimico e il livello di ossigeno, i ricercatori hanno non solo prodotto cellule mature simili a spermatozoi, ma le hanno anche impiegate per generare prole sana e fertile.
Perché è difficile riprodurre lo sviluppo precoce del testicolo
La produzione di spermatozoi al di fuori del corpo è già stata ottenuta usando tessuto testicolare di topi neonati o più grandi, ma l’efficienza era bassa e i tentativi con tessuto fetale molto più precoce sono per lo più falliti. A questo stadio giovane, il testicolo sta ancora assemblando la sua architettura interna e le cellule germinali stanno subendo ampi cambiamenti nel modo in cui il loro DNA è impacchettato e segnato. Riprodurre questa complicata coreografia in coltura è impegnativo, e le colture precedenti raramente progredivano oltre i primi passaggi quando si partiva da testicoli raccolti intorno al giorno embrionale 12.5, poco dopo la determinazione del sesso.
Prendere in prestito farmaci antivirali per proteggere le cellule in sviluppo
Il team si è concentrato su un ostacolo nascosto: elementi di DNA mobili chiamati retrotrasposoni, che possono copiarsi e inserirsi in nuove posizioni del genoma. Nei testicoli normali in vivo questi elementi sono strettamente controllati, in particolare nelle cellule germinali. In coltura, tuttavia, gli autori hanno riscontrato che l’attività dei retrotrasposoni era molto più alta, mentre i geni di difesa della cellula erano meno attivi. Questo squilibrio era correlato a uno scarso sviluppo degli spermatozoi. Poiché i retrotrasposoni utilizzano un enzima trascrittasi inversa, simile a quello di alcuni virus, i ricercatori hanno testato diversi farmaci originariamente progettati come inibitori della trascrittasi inversa. Un mix specifico di tre farmaci, denominato AEC, ha approssimativamente raddoppiato la frazione di cellule spermatogeniche e ha più che triplicato la quota di cellule aploidi simili a spermatozoi nei testicoli neonatali coltivati rispetto ai controlli non trattati.
Da piccoli testicoli fetali a spermatozoi funzionali
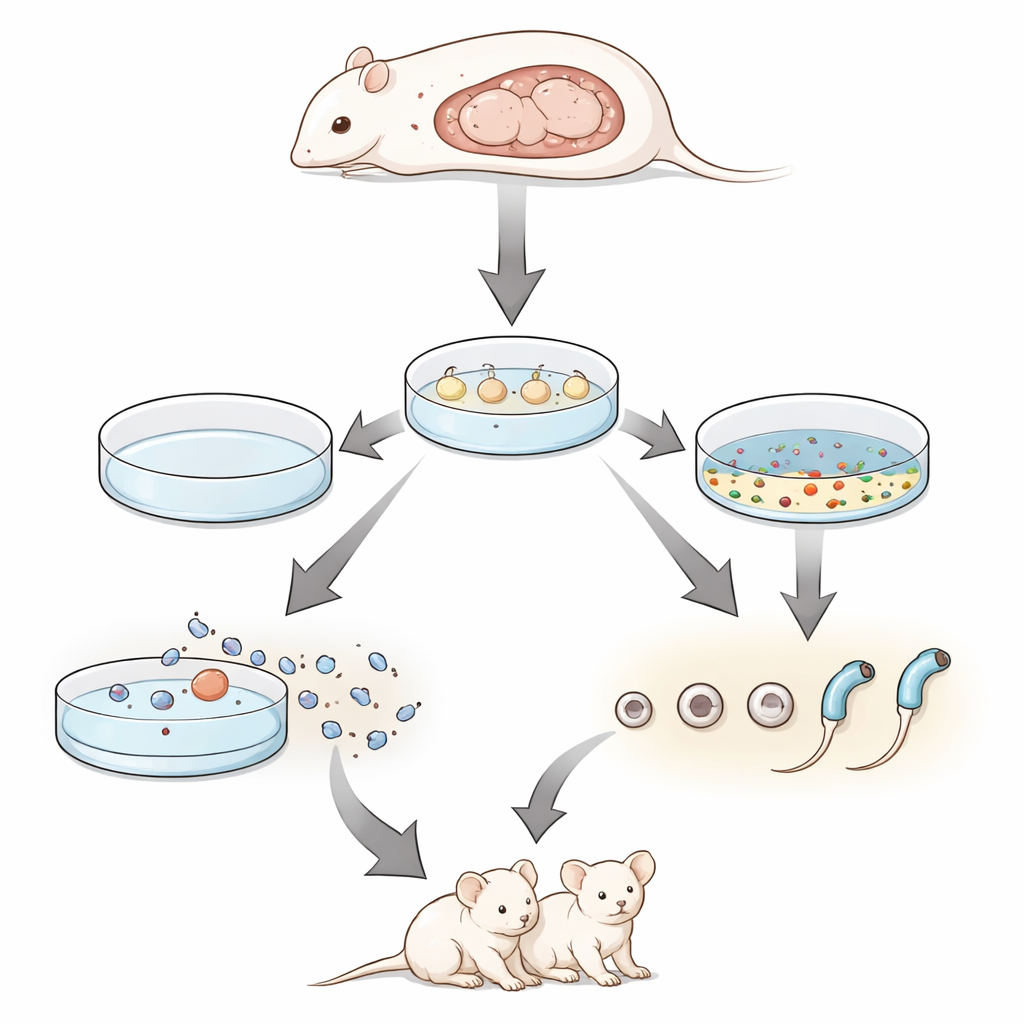
Dotati di questo cocktail farmacologico, gli scienziati si sono rivolti ai testicoli fetali. In tessuto prelevato poco prima della nascita, gli inibitori hanno incrementato la comparsa di spermatidi avanzati. Ancora più sorprendente, quando hanno coltivato testicoli di embrioni al giorno 12.5, uno stadio che non era mai stato mostrato completare la spermatogenesi in vitro, sono riusciti ora a generare spermatidi rotondi ed elongati. I maggiori benefici si sono osservati quando hanno combinato il mix di inibitori con un’atmosfera a basso contenuto di ossigeno che imita meglio le condizioni in sviluppo nel corpo. In queste condizioni ipossiche, circa un terzo dell’area tissutale mostrava marcatori di sviluppo germinale avanzato e spermatozoi dotati di flagello potevano essere recuperati dalle colture.
Verificare se gli spermatidi prodotti in laboratorio funzionano davvero
Per capire se queste cellule derivate in vitro fossero veramente funzionali, il team ha usato una tecnica chiamata iniezione di spermatidi rotondi. Hanno isolato spermatidi rotondi dai testicoli fetali coltivati e li hanno iniettati in ovociti di topo che erano stati delicatamente attivati. Gli embrioni risultanti sono stati trasferiti in madri surrogate. Da soli due frammenti di testicolo coltivati, la procedura ha prodotto più cuccioli vivi, molti dei quali portavano un gene marcatore fluorescente che confermava la loro origine in coltura. Quando questi animali di prima generazione sono stati accoppiati, hanno prodotto cucciolate di dimensioni normali e figli sani di seconda generazione, dimostrando che gli spermatidi derivati in laboratorio potevano sostenere non solo lo sviluppo fino alla nascita ma anche la fertilità completa.
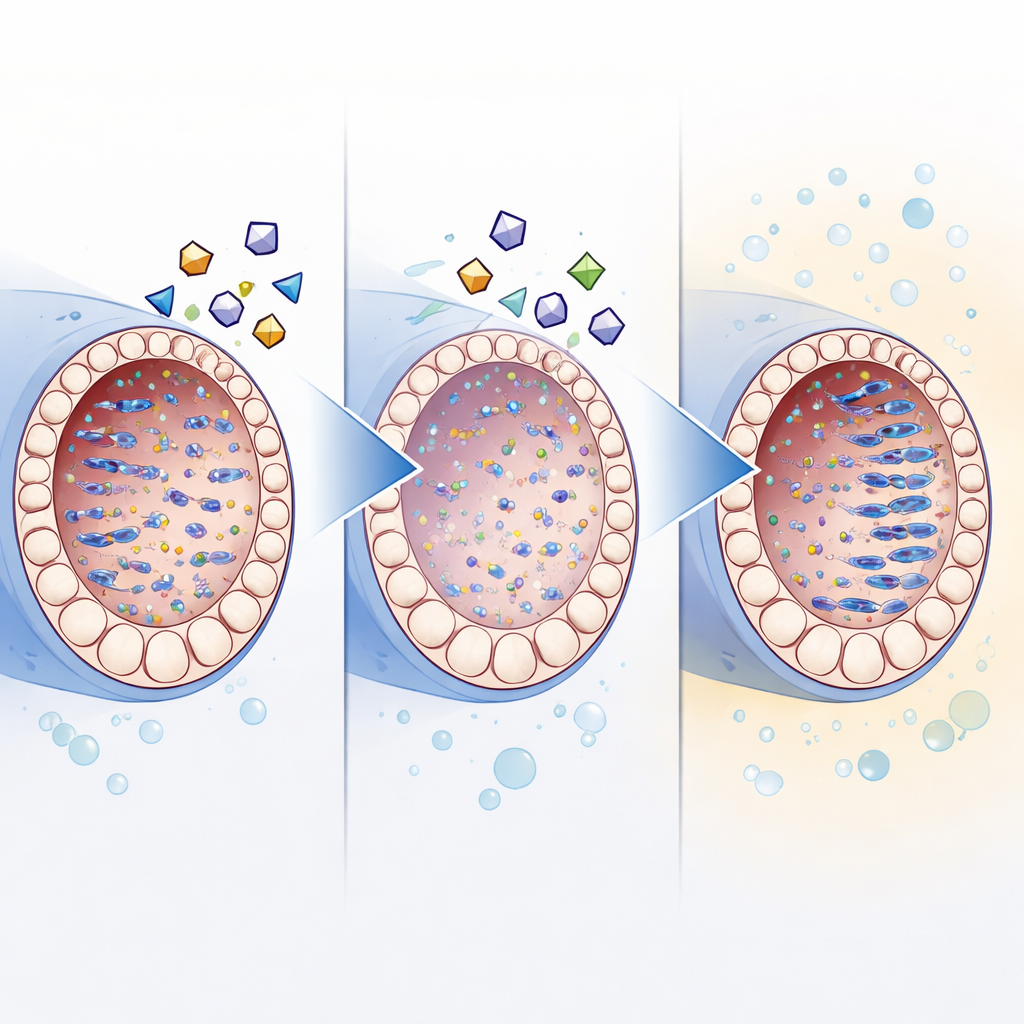
Come il blocco del DNA mobile potrebbe abilitare terapie future
Ulteriori esperimenti hanno supportato l’idea che gli inibitori della trascrittasi inversa aiutino principalmente mantenendo sotto controllo il DNA mobile. Rispetto a testicoli di pari età in vivo, i testicoli coltivati mostravano livelli più elevati di proteine dei retrotrasposoni e copie extra del loro DNA, insieme a una ridotta espressione dei meccanismi di silenziamento naturali della cellula. L’aggiunta del cocktail di inibitori ha ridotto questo accumulo, migliorando al contempo la maturazione delle cellule germinali. Sebbene i farmaci rallentassero leggermente la crescita tissutale complessiva, i tentativi di compensare questo effetto con additivi a base di siero non hanno aumentato la produzione di spermatozoi, suggerendo che crescita e differenziazione corretta devono essere bilanciate con attenzione.
Cosa significa per la scienza della riproduzione
Questo lavoro dimostra che anche testicoli fetali molto immaturi contengono già tutti gli ingredienti necessari per costruire una fabbrica di spermatozoi funzionante, a condizione che l’ambiente protegga i loro genomi e imiti aspetti chiave della vita uterina. Combinando farmaci in stile antivirale con basso ossigeno, i ricercatori hanno creato un sistema di coltura che ricapitola la spermatogenesi completa a partire da uno degli stadi più precoci finora testati e produce prole che cresce e si riproduce normalmente. Pur essendo lo studio condotto su topi e ancora lontano dall’uso clinico, apre una finestra potente sui primissimi passi dello sviluppo delle cellule germinali maschili e offre indizi che potrebbero un giorno aiutare a preservare o ripristinare la fertilità in pazienti i cui gameti sono danneggiati precocemente nella vita.
Citazione: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Parole chiave: spermatogenesi in vitro, coltura di testicolo fetale, inibitori della trascrittasi inversa, retrotrasposoni, fertilità maschile